氢氧化铝的制取和性质探究 知识点题库
氢氧化铝可作为治疗胃酸过多的内服药,这是利用了氢氧化铝的
A . 弱碱性
B . 弱酸性
C . 两性
D . 氧化性
下列物质的制备操作,可以达到实验目的是( )
A . 向FeCl3溶液中不断加入NaOH溶液制备Fe(OH)3胶体
B . 用铁和Cl2加热制取FeCl3
C . 用铜粉和硫粉混合加热制备CuS
D . 向铝盐溶液中不断滴入烧碱溶液制备Al(OH)3
将等体积的AlCl3溶液和NaOH溶液混合后,沉淀物中铝元素的物质的量与溶液中铝元素的物质的量相等,则原AlCl3溶液与NaOH溶液的物质的量浓度之比可能是( )
A . 1:3
B . 2:5
C . 1:5
D . 2:7
能实现Al3++3AlO2-+6H2O==4Al(OH)3过程的是
A . 向铝盐溶液中不断滴加氢氧化钠溶液
B . 向偏铝酸盐溶液中不断加入盐酸
C . 向偏铝酸钠溶液中不断通入二氧化碳气体
D . 向氢氧化钠溶液中不断滴加铝盐溶液
将4mol金属Al全部转化为Al(OH)3 , 消耗HClamol,NaOHbmol,则a+b的最小值为( )
A . 4
B . 6
C . 8
D . 16
下列解释事实的化学方程式不正确的是( )
A . 金属钠在空气中加热,生成淡黄色固体:2Na+O2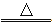 Na2O2
B . 向硫酸铝溶液中加入氨水制备氢氧化铝:Al3++3NH3•H2O═Al(OH)3 ↓+3NH4+
C . 铁在潮湿的环境中生锈:3Fe+4H2O═Fe3O4+4H2↑
D . 二氧化氮溶于水有硝酸生成:3NO2 +H2O═2HNO3+NO
Na2O2
B . 向硫酸铝溶液中加入氨水制备氢氧化铝:Al3++3NH3•H2O═Al(OH)3 ↓+3NH4+
C . 铁在潮湿的环境中生锈:3Fe+4H2O═Fe3O4+4H2↑
D . 二氧化氮溶于水有硝酸生成:3NO2 +H2O═2HNO3+NO
 Na2O2
B . 向硫酸铝溶液中加入氨水制备氢氧化铝:Al3++3NH3•H2O═Al(OH)3 ↓+3NH4+
C . 铁在潮湿的环境中生锈:3Fe+4H2O═Fe3O4+4H2↑
D . 二氧化氮溶于水有硝酸生成:3NO2 +H2O═2HNO3+NO
Na2O2
B . 向硫酸铝溶液中加入氨水制备氢氧化铝:Al3++3NH3•H2O═Al(OH)3 ↓+3NH4+
C . 铁在潮湿的环境中生锈:3Fe+4H2O═Fe3O4+4H2↑
D . 二氧化氮溶于水有硝酸生成:3NO2 +H2O═2HNO3+NO
下列通过制取硫酸铝、氢氧化铝,获得氧化铝的装置和原理能达到实验目的的是( )
A . 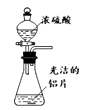 制硫酸铝
B .
制硫酸铝
B . 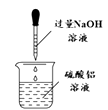 制氢氧化铝
C .
制氢氧化铝
C . 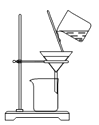 过滤氢氧化铝
D .
过滤氢氧化铝
D . 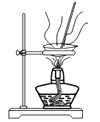 灼烧制氧化铝
灼烧制氧化铝
 制硫酸铝
B .
制硫酸铝
B .  制氢氧化铝
C .
制氢氧化铝
C .  过滤氢氧化铝
D .
过滤氢氧化铝
D .  灼烧制氧化铝
灼烧制氧化铝
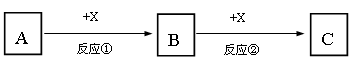
A、B、C、X均为中学常见的纯净物,它们之间有如下转化关系(反应条件及副产物已略去)。
-
(1) 若A、B、C均为含有同种非金属元素的化合物,A为使湿润的红色石蕊试纸变蓝的气体,B接触空气立刻变为C,则反应①的化学方程式为。
-
(2) 若A、B、C为焰色反应均呈黄色的化合物,X为无色无味气体,则反应②的离子方程式为。
-
(3) 若A、B、C均为含有同种金属元素的化合物,X是强碱,则反应②的离子方程式为。
-
(4) 若A为单质Fe,X为稀硝酸,若向B的溶液中加入氢氧化钠溶液,现象为。
-
(5) 若A和X均为单质,B为可使品红溶液褪色的气体,则反应②的化学方程式为。
向AlCl3溶液中逐滴加入NaOH溶液,开始观察到的现象是,反应的离子方程式为,继续加入过量的NaOH溶液,观察到的现象是,反应的离子方程式为。
下列说错误的是( )
A . 金属钠有强还原性,能和硫酸铜溶液反应,析出金属铜
B . 用Al(OH)3治疗胃酸过多
C . 过氧化钠可用于呼吸面具中作为氧气的来源
D . 绚丽缤纷的烟花中添加了含钾、钙、钠、铜等金属元素化合物
已知固体甲为非金属,I、F均为常见的金属,E为气体单质;固体乙为一种红棕色固体;G为白色胶状沉淀,既能溶解于盐酸,又能溶解于氢氧化钠溶液.A在常温下为气态,与氧气完全反应时的体积比是 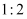 .W是由三种处在不同短周期的元素组成的化合物,与水反应生成A和G时的化学计量数之比为
.W是由三种处在不同短周期的元素组成的化合物,与水反应生成A和G时的化学计量数之比为 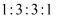 .各物质有如下图所示的转化关系(部分反应的产物未全部表示).试回答下列题:
.各物质有如下图所示的转化关系(部分反应的产物未全部表示).试回答下列题:
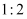 .W是由三种处在不同短周期的元素组成的化合物,与水反应生成A和G时的化学计量数之比为
.W是由三种处在不同短周期的元素组成的化合物,与水反应生成A和G时的化学计量数之比为 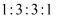 .各物质有如下图所示的转化关系(部分反应的产物未全部表示).试回答下列题:
.各物质有如下图所示的转化关系(部分反应的产物未全部表示).试回答下列题: 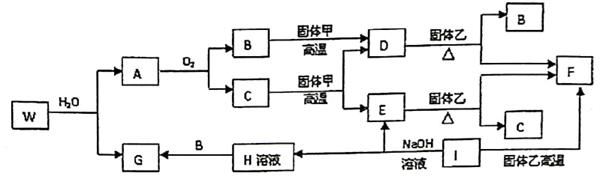
-
(1) B的电子式为,固体甲、乙的化学式分别是、;
-
(2) 上述转化中,①
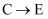 ②
② 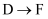 ③
③ 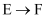 ④
④ 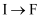 ⑤
⑤  ⑥
⑥ 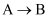 其中属于置换反应的是(填序号);
其中属于置换反应的是(填序号);
-
(3) 写出W和水反应的化学方程式,
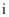 和
和  溶液反应的离子方程式.
溶液反应的离子方程式.
下列物质中不能用化合反应的方法制得的是( )
①SiO2 ②H2SiO3 ③Al(OH)3 ④Fe(OH)3 ⑤FeCl2
A . ①③
B . ②③
C . ①④
D . ④⑤
下列说法正确的是( )
A . 节日里燃放的五彩缤纷的烟花是某些金属元素化学性质的展现
B . 将等物质的量的氧化钠和过氧化钠分别投入到足量且等质量的水中,得到溶质质量分数分别是 a%和 b%的两种溶液,则a 和 b 的关系是 a=b
C . 用坩埚钳夹住一小块用砂纸仔细打磨过的铝箔在酒精灯上加热,熔化后的液态铝滴落下来, 说明金属铝的熔点较低
D . 用如图装置进行实验,将装置①中的 AlCl3 溶液滴入装置②浓氢氧化钠溶液,溶液中可观察到有大量白色沉淀产生 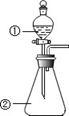

把
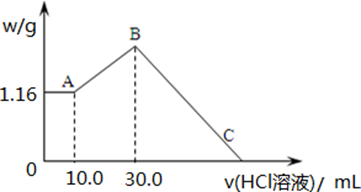
NaOH、MgCl2、AlCl3 三种固体组成的混合物溶于足量水后,产生 1.16g 白色沉淀, 再向所得浊液中逐渐加入
2.00mol/LHCl 溶液,加入HCl
溶液的体积与生成沉淀的关系如图所示。
-
(1) A 点沉淀物的化学式为。B 点纵坐标为。
-
(2) A 点至B 点改为通入二氧化碳气体,至少须标准状况下二氧化碳mL。此时发生反应的离子方程式为。
-
(3) B 点含溶质的物质的量是mol。C 点(此时沉淀恰好完全溶解)HCl 溶液的体积为mL。
用含有少量镁的铝片制取纯净的Al(OH)3 , 可能有的步骤为:① 加盐酸溶解;② 加过量苛性钠溶液;③ 过滤;④ 通入过量CO2;⑤ 加过量纯碱溶液,实验操作最合理的组合及顺序是( )
A . ①⑤④③
B . ②③④③
C . ②③⑤③
D . ①⑤③
下列关于金属及其化合物说法错误的是( )
A . 氧化铝用作耐火材料
B . 小苏打用于食品膨松剂
C . 纯碱用于中和胃酸过多
D . 氧化铁可用作涂料
下列说法不正确的是( )
A . 金属材料包括纯金属和它们的合金
B . 生铁是目前用量最大、用途最广的合金
C . 铝可用作包装材料和建筑材料
D . 氢氧化铝可用作治疗胃酸过多的药物
下列解释事实的离子方程式正确的是( )
A . 用 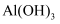 治疗胃酸过多症:
治疗胃酸过多症:  B . 用饱和
B . 用饱和  溶液将
溶液将  转变为
转变为 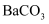 :
:  C . 用
C . 用  溶液腐蚀铜制印刷线路板:
溶液腐蚀铜制印刷线路板: 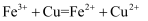 D . 有效成分为
D . 有效成分为 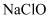 的消毒液与有效成分为浓
的消毒液与有效成分为浓 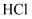 的洁厕灵混用产生黄绿色气体:
的洁厕灵混用产生黄绿色气体: 
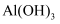 治疗胃酸过多症:
治疗胃酸过多症:  B . 用饱和
B . 用饱和  溶液将
溶液将  转变为
转变为 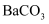 :
:  C . 用
C . 用  溶液腐蚀铜制印刷线路板:
溶液腐蚀铜制印刷线路板: 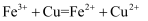 D . 有效成分为
D . 有效成分为 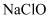 的消毒液与有效成分为浓
的消毒液与有效成分为浓  的洁厕灵混用产生黄绿色气体:
的洁厕灵混用产生黄绿色气体: 
下列衣食住行项目与所述的化学知识有关联的是( )
| 选项 | 项目 | 化学知识 |
| A | 衣:羊毛衫不能用碱性洗涤剂洗涤 | 蛋白质在碱性条件下易水解 |
| B | 食:SO2可用作葡萄糖抗氧化剂 | SO2具有氧化性 |
| C | 住:Al2O3在建筑中可用作耐高温材料 | Al2O3具有两性 |
| D | 行:NH3处理汽车尾气中的氮氧化物 | NH3沸点低、易液化 |
A . A
B . B
C . C
D . D
用如图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是( )
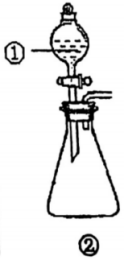
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀盐酸 | 碳酸钠与氢氧化钠的混合溶液 | 立即产生大量气泡 |
B | 硫酸亚铁溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪至无色 |
C | 氯化铝溶液 | 浓氢氧化钠溶液 | 立即产生大量白色沉淀 |
D | 氯水 | 硫酸亚铁及硫氰化钾溶液 | 溶液受成红色 |
A . A
B . B
C . C
D . D
最近更新



