臭氧 知识点
臭氧 知识点题库
(1)该反应的化学方程式为: ;
(2)该反应中氧化剂的名称为 ,还原产物的化学式为 ;
(3)若消耗0.1mol氧化剂,反应中转移电子的物质的量为
(1)臭氧的摩尔质量是 .
(2)2mol 臭氧的质量是 ,其中含有O3的分子数目是 ,含有O原子数目是
(2)用双氧水制取氧气的反应方程式
(3)C与浓硫酸反应的化学方程式
-
(1) 臭氧几乎可与除铂、金、铱、氟以外的所有单质反应.如:6Ag(s)+O3(g)=3Ag2O(s);△H=﹣235.8kJ•mol﹣1 . 已知2Ag2O(s)=4Ag(s)+O2(g);△H=+62.2kJ•mol﹣1 , 则常温下反应2O3(g)=3O2(g)为 反应(填“自发”或“非自发”).
-
(2) 臭氧在水中易分解,臭氧的浓度减少一半所需的时间如下表所示.
pH
t/min
T/℃
3.0
4.0
5.0
6.0
20
301
231
169
58
30
158
108
48
15
50
31
26
15
7
pH增大能加速O3分解,表明对O3分解起催化作用的是 (填微粒符号).
-
(3) 科学家P.Tatapudi等人首先使用在酸性条件下电解水的方法制得臭氧.臭氧在阳极周围的水中产生,电极反应3H2O﹣6e﹣=O3↑+6H+ , 阴极附近的氧气则生成过氧化氢,其电极反应式为
-
(4) 为测定大气中臭氧(O3)含量,将0℃、1.01×105Pa的空气V L慢慢通过足量KI溶液,使臭氧完全反应;然后将所得溶液用a mL c mol•L﹣1的Na2S2O3溶液进行滴定恰好到达终点.
①该滴定过程中可选择的指示剂为 .
②O3与KI溶液反应生成两种单质,则反应的化学方程式 .
③空气中臭氧的体积分数为 (用含“a、c、V”的字母表示).
(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
臭氧(O3)是优良的水消毒剂.但当水中含溴离子(Br﹣)时,臭氧可氧化溴离子(Br﹣)为溴酸盐(BrO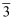 ).而溴酸盐(BrO
).而溴酸盐(BrO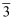 )是对人体有致癌作用的化合物,我国规定饮用水中BrO
)是对人体有致癌作用的化合物,我国规定饮用水中BrO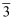 含量在10 μg/L以下.测定BrO
含量在10 μg/L以下.测定BrO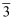 浓度可用离子色谱法.
浓度可用离子色谱法.
-
(1)
O3氧化溴离子的原理如下:
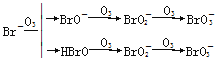
已知HBrO是一种弱酸,O3与HBrO反应很慢,BrO
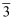 主要是由BrO﹣与O3反应生成.对影响生成BrO
主要是由BrO﹣与O3反应生成.对影响生成BrO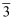 速率的因素提出如下假设:(请你完成假设②和假设③)
速率的因素提出如下假设:(请你完成假设②和假设③)假设①:反应的温度 .
假设②: .
假设③:
-
(2) 设计实验验证假设①.验证实验操作:
a.配制250mL 50mg/L KBr溶液,加入15mL某种pH=7的缓冲溶液(维持溶液的pH基本不变),并将溶液分为2份.
b. .
实验中要测定的量是 .实验结论是
(1)臭氧层是地球生命的保护神,臭氧比氧气具有更强的氧化性.实验室可将氧气通过高压放电管来制取臭氧:3O 2O3若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为 (保留一位小数).
2O3若在上述反应中有30%的氧气转化为臭氧,所得混合气的平均摩尔质量为 (保留一位小数).
(2)O3与Cl2具有相似的性质,均可用于自来水的消毒.已知二者在消毒时均被还原为最低价态,则1mol O3与 L(标准状况下)Cl2的消毒能力相当.
①活性炭
②氯水
③二氧化硫
④臭氧
⑤过氧化钠
⑥双氧水.



