蒸发和结晶、重结晶 知识点题库
下列属于分离、提纯固态有机物的操作的是( )
A . 蒸馏
B . 萃取
C . 重结晶
D . 分液
选择合适的实验方法,将序号填在横线上。
A.加热蒸发 B.升华 C.重结晶
D.分液 E.蒸馏 F.过滤
①分离饱和食盐水与沙子混合物。
②从硝酸钾和氯化钠的混合溶液中获得硝酸钾。
③分离水和汽油混合物。
④分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的混合物。
下列是初中化学常见的四个实验,回答下列问题;

-
(1) )A实验中集气瓶内预先装少量水的目的是 .实验结束后,瓶内液体的pH 7.(填“>”、“<”或“﹦”)
-
(2) B实验中导致实验结果偏小的原因是 (只写一个).
-
(3) C实验中该操作将导致所配溶液溶质质量分数 (填“偏大”、“偏小”或“不变”).
-
(4) D实验中待 时,应停止加热.
粗盐提纯中几次用到玻璃棒,每次使用的作用各是什么?
下列实验操作中正确的是( )
A . 分液操作时,先将分液漏斗中的下层液体放出,再将上层液体接着放出
B . 用蒸发方法使NaCl从溶液中析出时,应将蒸发皿中NaCl溶液全部加热蒸干
C . 蒸馏实验中温度计的水银球应插入液态混合物中
D . 过滤时玻璃棒的末端应轻轻靠在三层滤纸上
10%的MgSO4溶液120g蒸去95.4g H2O,剩下的刚好形成MgSO4•xH2O晶体,则x值是( )
A . 8
B . 7
C . 6
D . 4
下列分离方法中,和物质的溶解度无关的是( )
A . 升华
B . 萃取
C . 纸层析法
D . 蒸发结晶
下列分离提纯方法正确的是( )
A . 除去NaCl固体中少量的Na2CO3:加水溶解,加入足量的CaCl2溶液,过滤,蒸发,结晶
B . 除去NaCl固体中少量的KNO3:加水溶解,燕发结晶,趁热过滤
C . 除去CO2气体中少量的HCl通过感有饱和Na2CO3溶液的洗气瓶洗气
D . 除去CO2气体中少量的CO:通入适量O2后点燃
下列有关实验的叙述正确的是( )
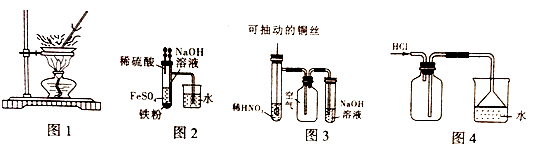
A . 用图1装置将氯化铁溶液直接蒸干得到氯化铁固体
B . 利用图2装置可制备Fe(OH)2
C . 图3微热稀HNO3片刻,溶液中有气泡产生,广口瓶内始终保持无色
D . 利用图4可收集氯化氢并进行尾气吸收
下列从混合物中分离出其中的某一成分,所采取的分离方法正确的是( )
A . 利用氯化钾与碳酸钙的溶解性差异,可用溶解、过滤的方法除去碳酸钙
B . 由于碘在酒精中的溶解度大,所以可用酒精把碘水中的碘萃取出来
C . CO2中混有HCl,可通过盛有NaOH溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶得到纯净干燥的CO2
D . 从海水中获取氯化钠,可采取蒸馏的方法
以某含镍废料(主要成分为NiO,还含有少量FeO、Fe2O3、CoO、SiO2等)为原料制备NixOy和碳酸钻的工艺流程如下:

-
(1) “酸溶”时需将含镍废料粉碎,目的是;含有CoCO3的玻璃常用作实验室观察钾元素的焰色反应,该玻璃的颜色为。
-
(2) “氧化”中添加NaClO3的作用是,为证明添加NaClO3已足量,可用 (写化学式)溶液进行检验。
-
(3) “调pH”过程中生成黄钠铁钒沉淀(NaFe3(SO4)2(OH)6),其离子方程式为。
-
(4) “沉钴”过程的离子方程式__。若“沉钴钻”开始时c(Co2+)=0.10 mol/L,则控制pH≤__时不会产生Co(OH)2沉淀。(已知Ksp[Co(OH)2]=4.0×10-15 , lg2=0.3)。
-
(5) 从NiSO4溶液获得NiSO4·6H2O晶体的操作依次是:加热浓缩溶液至有晶膜出现,,过滤,洗涤,干燥。“锻烧”时剩余固体质量与温度变化曲线如图,该曲线中B段所表示氧化物(NixOy)的化学式为。

根据下列实验操作和现象所得出的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向盛有某盐溶液的试管中滴入氢氧化钠溶液后,加热,试管口处湿润的红色石蕊试纸变蓝 | 该盐中含 |
| B | 向溴水中通入某无色气体,溴水褪色 | 该气体可能是CH2=CH2 |
| C | 一定量的铜与硝酸充分反应后,有铜剩余,再加入少量稀硫酸,铜继续溶解,并有气泡放出 | Cu与稀硫酸发生了反应 |
| D | 向淀粉溶液中加少量稀硫酸,加热4~5min。冷却后向其中加入新制Cu(OH)2悬浊液,加热至沸腾,无砖红色沉淀 | 淀粉没有发生水解 |
A . A
B . B
C . C
D . D
某实验小组只领取下列仪器或用品:铁架台、铁圈、铁架、三角架、石棉网、烧杯、分液漏斗、酒精灯、玻璃棒、量筒、蒸发皿、蒸馏烧瓶、火柴、滤纸、漏斗。只应用上述仪器或用品,不能进行的实验操作是( )
A . 蒸发
B . 萃取
C . 过滤
D . 蒸馏
在硫酸铜晶体(CuSO4·nH2O)结晶水含量测定的操作中,导致n值偏小的是( )
A . 坩埚未干燥
B . 在空气中冷却
C . 加热过程中晶体爆溅
D . 加热时间过长部分变黑
某同学设计利用下图装置制备硫酸锰,下列说法错误的是( )

A . 装置I烧瓶中放入的药品X为Na2SO3固体,浓硫酸在反应中表现出酸性
B . 装置II中用“多孔球泡”可增大SO2的吸收速率,SO2在反应中做还原剂
C . 装置III烧杯里装的是NaOH溶液,用于吸收未反应的SO2气体
D . 从装置II反应后的溶液获取MnSO4·H2O可以采用蒸发结晶的方法
实验室模拟侯氏制碱法制取纯碱和氯化铵溶液,下列选项有关操作错误的是( )
| 选项 | A. | B. | C. | D. |
| 实验操作 | | | | |
| 实验目的 | 制取氨气将其溶于饱和食盐水 | 用碳酸钠与稀硫酸制二氧化碳 | 过滤获得碳酸钠晶体 | 蒸发浓缩氯化铵溶液 |
A . A
B . B
C . C
D . D
实验室提供的仪器有:试管、导管、酒精灯、容量瓶、玻璃棒、烧杯、蒸发皿、分液漏斗(非玻璃仪器任选),选用上述仪器不能完成的实验是( )
A . 用苯萃取溴水中的溴
B . 配制0.5 mol/L的硫酸
C . 制备乙酸乙酯
D . 硫酸铜溶液的浓缩结晶
下列实验操作中错误的是( )
A . 过滤时,玻璃棒的末端轻轻靠在三层滤纸处
B . 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口
C . 蒸发氯化钠溶液时,将溶液全部蒸干后,再停止加热
D . 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出
无水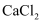 具有强烈的吸湿性,在空气中易潮解,可用作干燥剂、脱水剂、混凝防冻剂等。以工业碳酸钙矿石(含有少量
具有强烈的吸湿性,在空气中易潮解,可用作干燥剂、脱水剂、混凝防冻剂等。以工业碳酸钙矿石(含有少量 、
、 、
、 、
、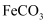 等杂质)生产无水氯化钙的主要流程如下:
等杂质)生产无水氯化钙的主要流程如下:
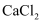 具有强烈的吸湿性,在空气中易潮解,可用作干燥剂、脱水剂、混凝防冻剂等。以工业碳酸钙矿石(含有少量
具有强烈的吸湿性,在空气中易潮解,可用作干燥剂、脱水剂、混凝防冻剂等。以工业碳酸钙矿石(含有少量 、
、 、
、 、
、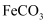 等杂质)生产无水氯化钙的主要流程如下:
等杂质)生产无水氯化钙的主要流程如下:
-
(1) 为了提高步骤①的反应速率,可以采取的措施是。
-
(2) 加入试剂b的目的是使溶液酸化,试剂b可以选择____(选填字母)试剂。A . 硫酸 B . 硝酸 C . 氢硫酸 D . 盐酸
-
(3) 写出步骤②的离子方程式:。
-
(4) 步骤⑤涉及的操作方法有蒸发浓缩、。
-
(5) 已知
 、
、 、
、 生成氢氧化物沉淀或沉淀溶解的pH如下:
生成氢氧化物沉淀或沉淀溶解的pH如下: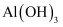



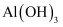
开始沉淀
3.7
6.5
1.5
12.4
开始溶解
7.8
沉淀完全
5.3
9.7
3.3
13.8
完全溶解
10.0
可以通过加入试剂a调节溶液Ⅱ的pH,调节溶液Ⅱ的pH的目的是,调节pH的范围为。
-
(6) 已知某一温度时
 , 向
, 向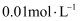 的
的 溶液中加入NaOH固体,假设溶液的体积不变,要使
溶液中加入NaOH固体,假设溶液的体积不变,要使 沉淀完全,溶液中
沉淀完全,溶液中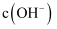 最小为
最小为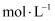 。
。
对氨基苯磺酸( )通常是一种白色固体,难溶于冷水、易溶于热水,在染料、农药等行业均有应用。实验室制备对氨基苯磺酸的部分流程如下图所示。下列说法错误的是( )
)通常是一种白色固体,难溶于冷水、易溶于热水,在染料、农药等行业均有应用。实验室制备对氨基苯磺酸的部分流程如下图所示。下列说法错误的是( )
 )通常是一种白色固体,难溶于冷水、易溶于热水,在染料、农药等行业均有应用。实验室制备对氨基苯磺酸的部分流程如下图所示。下列说法错误的是( )
)通常是一种白色固体,难溶于冷水、易溶于热水,在染料、农药等行业均有应用。实验室制备对氨基苯磺酸的部分流程如下图所示。下列说法错误的是( )![]()
A . 可通过控制滴液漏斗活塞而控制浓硫酸的滴速
B . 试剂X可选用冰水
C . 操作Ⅱ所需的玻璃仪器为烧杯、漏斗、玻璃棒
D . 操作Ⅲ具体指溶解、过滤、洗涤、蒸馏
最近更新