分液和萃取 知识点题库
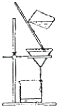 B .
B . 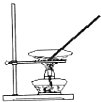 C .
C . 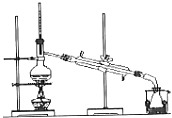 D .
D . 
选项 | 目 的 | 分离方法 | 原 理 |
A | 除去丁醇中的乙醇 | 蒸馏 | 丁醇与乙醇的沸点相差较大 |
B | 分离乙酸乙酯和乙醇 | 分液 | 乙酸乙酯和乙醇的密度不同 |
C | 除去KNO3固体中混杂的NaCl | 重结晶 | NaCl在水中的溶解度很大 |
D | 分离溶于水中的碘 | 乙醇萃取 | 碘在乙醇中的溶解度较大 |

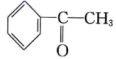 )广泛用于皂用香精和烟草香精中,实验室可用苯和乙酸酐(
)广泛用于皂用香精和烟草香精中,实验室可用苯和乙酸酐( 步骤一:在A中加入30mL干燥的苯和30g无水AlCl3粉末,在剧烈搅拌下,缓慢滴入7mL乙酸酐,控制反应温度为30℃,反应过程中释放出HCl气体,HCl释放停止后,再加热至90~95℃,回流反应1h,形成黑黄色液体。装置如图1所示。

步骤二:将冷却后的反应瓶置于冰水浴中(如图2所示),加入15mL苯,慢慢加入混合的盐酸冰水,静置分层,分液,无机相用乙醚萃取,与有机相合并,有机相用10%NaOH液洗涤,分液,弃去无机层,有机层用9mL水洗,分液,弃去无机层,有机层用MgSO4干燥。
步骤三:分离提纯苯乙酮。
回答下列问题:
-
(1) 仪器A的名称是。写出苯与乙酸酐生成苯乙酮的化学方程式:。
-
(2) 仪器B中盛装无水CaCl2 , 其作用是。
-
(3) 步骤二中多次使用到的操作是。
-
(4) 已知常压下:
熔点/℃
沸点/℃
苯
5.5
80.1
乙醚
-116.3
34.6
苯乙酮
19.6
202
则步骤三分离提纯苯乙酮使用的操作是;为了收集纯净的苯乙酮馏分,分离苯乙酮应使用下面的图装置。
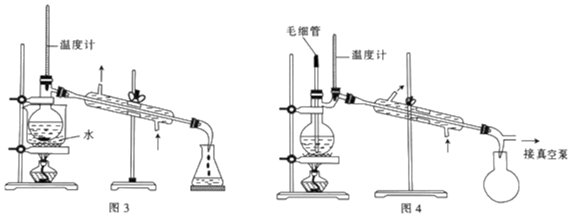
| 目的 | 分离方法 | 原理 | |
| A | 分离水和乙醇 | 蒸馏 | 水和乙醇的沸点不同 |
| B | 分离溶于水中的碘单质 | 四氯化碳萃取 | 碘单质在四氯化碳中的溶解度远大于在水中的溶解度,四氯化碳难溶于水 |
| C | 除去CO2中少量HCl气体 | 通入足量NaHCO3溶液中洗气 | HCl会与NaHCO3溶液反应且产生更多CO2 |
| D | 除去NaCl固体中混有的少量KNO3杂质 | 加水溶解配成热的浓溶液,冷却结晶,过滤 | NaCl和KNO3溶解度随温度变化有较大差异 |

-
(1) 从氯化钾溶液中得到氯化钾固体,选择装置。
-
(2) 氯化钠固体中混有碘,选择装置。
-
(3) 河水样品中加了少量明矾,选择装置。
-
(4) 除去自来水中的
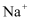 、
、  杂质离子,选择装置。
杂质离子,选择装置。
-
(5) 装置E在分液时为使液体顺利滴下,除打开活塞外,还应进行的具体操作是。
-
(1) I.实验室按如下实验流程提取海带中的碘。
海带→灼烧→过滤→氧化→萃取、分液→I2的CCl4溶液
上述实验流程中不需要用到的仪器是(从下列图中选择,写出名称)。

-
(2) “氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为。
-
(3) 海带灰中含有的其他可溶性无机盐。是在(从以上流程中选填实验操作名称)中实现与碘分离。
-
(4) II.定量探究
 +2I-=2
+2I-=2 +I2的反应速率与反应物浓度的关系。
+I2的反应速率与反应物浓度的关系。查阅资料:该反应速率与c(S2O82-)和c(I-)的关系v=kcm(
 )cn(I-),k为常数。
)cn(I-),k为常数。实验任务:测定不同浓度下的反应速率确定所m、n的值。
实验方法:按下表体积用量V将各溶液混合,(NH4)2S2O8溶液最后加入,记录开始反应至溶液出现蓝色所用的时间t。实验过程中发生如下反应:
 +2I-=2
+2I-=2 +I2(慢)I2+2
+I2(慢)I2+2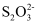 =2I-+
=2I-+ (快)
(快)实验记录表:
实验编号
A
B
C
D
E
0.2mol·L-1(NH4)2S2O8溶液/mL
10
5
2.5
10
10
0.2mol·L-1KI溶液/mL
10
10
10
5
2.5
0.05mol·L-1Na2S2O3溶液/mL
3
3
3
3
3
0.2mol·L-1KNO3溶液/mL
0
V1
V2
V3
V4
0.2mol·L-1(NH4)2SO4溶液/mL
0
V5
V6
V7
V8
0.2%淀粉溶液/mL
1
1
1
1
1
t/s
t1
t2
t3
t4
t5
加入KNO3、(NH4)2SO4溶液的目的是控制实验条件,其中V1,V4,V5。
-
(5) 当溶液中(填化学式)耗尽后溶液出现蓝色。根据实验A的数据,反应速率v(
 -)=mol·L-1·s-1(列出算式)。
-)=mol·L-1·s-1(列出算式)。
-
(6) 根据实验数据可确定m、n的值。n=1的判断依据是(用t的关系式来表示)。



