除杂 知识点题库
物质 | 密度(g/ml﹣3) | 沸点(℃) | 水溶性 | 溶解性 |
甲 | 0.7893 | 78.5 | 溶 | 溶于乙 |
乙 | 1.220 | 100.7 | 溶 | 溶于甲 |
则采用的分离方法是( )
①用乙醇和浓硫酸除去乙酸乙酯中的少量乙酸
②用NaOH溶液除去苯中的少量苯酚
③用饱和NaHCO3溶液除去CO2中的少量SO2
④用加热的方法提取NH4Cl固体中混有的少量碘
⑤用醋和澄清石灰水验证蛋壳中含有碳酸盐
⑥用米汤检验食用加碘盐中含碘
⑦用碘酒验证汽油中含有不饱和烃.
物质 | 试剂 | 分离方法 | |
① | 溴苯(溴) | 氢氧化钠溶液 | 分液 |
② | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
③ | 乙酸乙酯(乙酸) | NaOH溶液 | 分液 |
④ | Cl2(HCl) | 饱和NaCl溶液 | 洗气 |
-
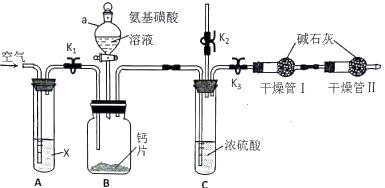
(1) A装置的作用为,仪器a的名称为。
-
(2) B 装置内发生反应的化学方程式为,实验中不用盐酸与钙片反应的原因是。
-
(3) 组装好仪器后,检查装置的气密性,接下来进行的操作是:打开K1、K2 , 关闭K3 , 通空气一段时间, (填操作),打开仪器a活塞,滴入氨基磺酸溶液,待B装置中无气泡产生,关闭仪器a活塞。再次打开K1通空气一段时间,第二次通入空气目的是。如果不使用干燥管Ⅱ,测定结果(填“偏高”“偏低”“不变”)。
-
(4) 取某补钙剂样品m克进行测定,测得干燥管Ⅰ在实验前后重量分别为m1克和m2克,则样品中钙的质量分数为。

(注:SiCl4的沸点为57.6 ℃,金属氯化物的沸点均高于150 ℃)
-
(1) 向反应器中通入Cl2前,需通一段时间N2 , 主要目的是。
-
(2) 高温反应后,石墨中氧化物杂质均转变为相应的氯化物。气体Ⅰ中的碳氧化物主要为。由气体Ⅱ中某物得到水玻璃的化学反应方程式为。
-
(3) 步骤①为:搅拌、。所得溶液Ⅳ中的阴离子有。
-
(4) 由溶液Ⅳ生成沉淀Ⅴ的总反应的离子方程式为,
100kg初级石墨最多可能获得Ⅴ的质量为kg。
-
(5) 石墨可用于自然水体中铜件的电化学防腐,完成如图防腐示意图,并作相应标注。

-
(1) 写出NaHSO4在水中的电离方程式。
-
(2) 粗盐中含可溶性CaCl2、MgCl2及一些硫酸盐,要除去这些杂质,可选用以下试剂:①Na2CO3、②NaOH、③BaCl2 , 则试剂加入的先后顺序是(填序号)。
-
(3) 实验证明铜不能在低温下与O2反应,也不能与稀H2SO4共热发生反应,但工业上却是将废铜屑倒入热的稀H2SO4中并通入空气来制备CuSO4溶液的,则铜屑在此状态下被溶解的化学方程式为。
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 将氯化铁溶液加热灼烧 | 有固体析出 | 该固体是氯化铁 |
| B | 氯化铜溶液中有氯化铁杂质,加入氧化铜除杂 | 有红褐色物质析出 | 调节pH使铁离子水解平衡右移 |
| C | 将充满NO2的密闭玻璃球浸泡在热水中 | 红棕色变深 | 反应2NO2 |
| D | 向1 mL 0.1 mol/L的AgNO3溶液中加入4滴0.1 mol/L的NaCl溶液,再加10滴0.1 mol/L的NaI溶液,再振荡 | 先生成白色沉淀,后产生黄色沉淀 | Ksp(AgI)<Ksp(AgCl) |
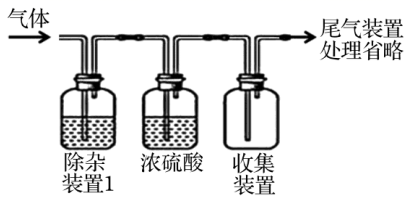
选项 | 气体(杂质) | 除杂装置1 |
A |
| NaOH溶液 |
B |
| 饱和食盐水 |
C |
| 饱和碳酸钠溶液 |
D |
| 酸性高锰酸钾溶液 |
| 原物(杂质) | 除杂试剂 | 除杂方法 | |
| A | CO2(H2S) | CuSO4溶液 | 洗气 |
| B | 碳粉(MnO2) | 浓盐酸 | 加热后过滤 |
| C | 乙酸(乙醇) | 饱和Na2CO3溶液 | 蒸馏 |
| D | 硝基苯(NO2) | NaOH溶液 | 分液 |
 、
、 、
、 、
、 、
、 等离子,用该废液制备碱式碳酸铜的工艺流程如图所示。下列说法错误的是( )
等离子,用该废液制备碱式碳酸铜的工艺流程如图所示。下列说法错误的是( )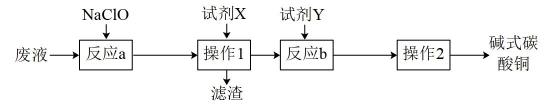
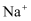 、
、 、
、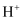 、
、 B . 若试剂X为氧化铜或氢氧化铜,则滤渣中含有
B . 若试剂X为氧化铜或氢氧化铜,则滤渣中含有 等成分
C . 若Y为
等成分
C . 若Y为 , 则反应b为:
, 则反应b为: D . “操作1”和“操作2”二者操作过程完全相同
D . “操作1”和“操作2”二者操作过程完全相同
选项 | 物质(杂质) | 除杂实验 |
A | CH3COOC2H5(CH3COOH) | 加入饱和Na2CO3溶液充分振荡,分液、洗涤、干燥 |
B | KNO3(NaCl) | 加AgNO3溶液,过滤,洗涤 |
C | Na2CO3 (NaHCO3) | 加热分解 |
D | C2H5OH(H2O) | 加CaO充分混合,蒸馏 |
 N2O4的△H>0
N2O4的△H>0






