含碳化合物的性质和应用 知识点题库
如何解决好碳排放问题是关系到人类可持续发展的重大课题之一。目前,采用较多的方法是对二氧化碳进行捕集封存和富集再利用。下列与二氧化碳有关的叙述正确的是( )
A . CO2是形成酸雨的主要物质
B . CO2导致温室效应,是一种大气污染物
C . CO2(g)+C(s)  2CO(g)
2CO(g)  H>0,高温有利于该反应自发进行
D . 实验室常用大理石与稀盐酸或稀硫酸反应制取二氧化碳
H>0,高温有利于该反应自发进行
D . 实验室常用大理石与稀盐酸或稀硫酸反应制取二氧化碳
 2CO(g)
2CO(g)  H>0,高温有利于该反应自发进行
D . 实验室常用大理石与稀盐酸或稀硫酸反应制取二氧化碳
H>0,高温有利于该反应自发进行
D . 实验室常用大理石与稀盐酸或稀硫酸反应制取二氧化碳
合成气(CO、H2)是一种重要的化工原料气。合成气制取有多种方法,如煤的气化、天然气部分氧化等。回答下列问题:
-
(1) I.合成气的制取
煤的气化制取合成气。
已知:①H2O(g)=H2O(l) △H=-44kJ/mol;
②部分物质的燃烧热:

则反应C(s)+H2O(g)
 CO(g)+H2(g)的△H=kJ/mol。
CO(g)+H2(g)的△H=kJ/mol。 -
(2) 天然气部分氧化制取合成气。
如果用O2(g)、H2O(g)、CO2(g)混合物氧化CH4(g),欲使制得的合成气中CO和H2的物质的量之比为1︰2,则原混合物中H2O(g)与CO2(g)的物质的量之比为。
-
(3) Ⅱ.利用合成气合成乙醇
在一定条件下,向容积为2L的恒容密闭容器中投入2molCO和4molH2 , 发生反应:2CO(g)+4H2(g)
 CH3CH2OH(g)+H2O(g)。
CH3CH2OH(g)+H2O(g)。写出该反应的平衡常数表达式__。
-
(4) 下列情况能作为判断反应体系达到平衡的标志是 (填序号)。A . 压强不再变化 B . 平均摩尔质量不再变化 C . 密度不再变化
-
(5) 反应起始压强记为p1、平衡后记为p2 , 平衡时H2的转化率为。(用含p1、p2的代数式表示)
-
(6) Ⅲ.合成乙醇的条件选择
为探究合成气制取乙醇的适宜条件,某科研团队对不同温度、不同Rh质量分数的催化剂对CO的吸附强度进行了研究,实验数据如图。CO的非离解吸附是指CO尚未乙醇化,离解吸附是指CO已经乙醇化。

结合图像从低温区、高温区分析温度对CO吸附强度的影响;以及催化剂对CO吸附强度的影响。
-
(7) 用Rh作催化剂,合成气制取乙醇的适宜温度是。
《本草纲目》中的“石碱”条目下写道:“采蒿蓼之属……晒干烧灰,以原水淋汁……久则凝淀如石……浣衣发面,甚获利也。”下列说法中错误的是( )
A . “石碱”的主要成分易溶于水
B . “石碱”俗称烧碱
C . “石碱”可用作洗涤剂
D . “久则凝淀如石”的操作为结晶
下列各项操作中,发生“先沉淀后溶解”现象的为( )
①向饱和Na2CO3溶液中通入过量的CO2
②向Fe(OH)3胶体中逐滴滴入过量的稀H2SO4
③向石灰水中通入CO2至过量
④CaCl2溶液中通入CO2至过量
A . ①④
B . ②③
C . ①②④
D . ③
如图为含有同一种元素的a、b、c、d四种物质的转化关系。其中a是单质,b、c是氧化物,d是酸,各步转化均为一步实现,则a可能是①C、②S中( )
![]()
A . 只有①
B . 只有②
C . ①②
D . 都不符合
下列物质(对应X—Y—Z)不能通过一步反应完成如图转化的是( )

A . CH2=CH2-C2H5Br-C2H5OH
B . FeO-Fe(OH)2-Fe(OH)3
C . H2S-SO2-H2SO4
D . NaOH-Na2CO3-NaHCO3
下列几种气体(括号内为溶剂或反应物溶液)按如图所示装置进行实验,不能看到喷泉现象的是( )
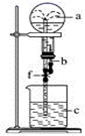
A . HCl(H2O)
B . CO2(H2O)
C . SO2(NaOH溶液)
D . NH3(KCl溶液)
能实现下列物质间直接转化的元素是( )
单质 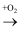 氧化物
氧化物  酸或碱
酸或碱  盐
盐
①碳②硫③铜 ④铁
A . ①②
B . ②③
C . ③④
D . ②④
2021年1月20日中国科学院和中国工程院评选出2020年世界十大科技进展,排在第四位的是一种可借助光将二氧化碳转化为甲烷的新型催化转化方法:CO2+4H2=CH4+2H2O,这是迄今最接近人造光合作用的方法。CO2加氢制CH4的一种催化机理如图,下列说法正确的是( )

A . 反应中La2O3是中间产物
B . 反应中La2O2CO3可以释放出带负电荷的CO2·
C . H2经过Ni活性中心裂解产生活化态H·的过程中ΔS>0
D . 使用TiO2作催化剂可以降低反应的焓变,从而提高化学反应速率
某同学为了检验浓硫酸与木炭粉在加热条件下反应(C+2H2SO4(浓)  CO2↑+2SO2↑+2H2O)产生的所有气体产物,选用了如下图所示的实验装置。
CO2↑+2SO2↑+2H2O)产生的所有气体产物,选用了如下图所示的实验装置。
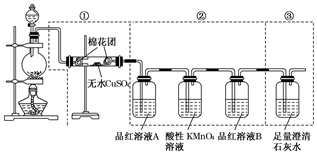
-
(1) ①中无水硫酸铜的作用是。
-
(2) ②中酸性KMnO4溶液的作用是。
-
(3) ②中两次用到品红溶液,它们的作用分别是A,B。
-
(4) ③中出现的现象是,
发生反应的离子方程式是。
下列说法正确的是( )
A . 茅台酒中含有1000多种元素
B . 洁厕灵与漂白液混合使用效果更好
C . 某产品广告词说“本产品不含任何化学物质”
D . 四氯化碳可用作灭火剂
在下图的烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是( )
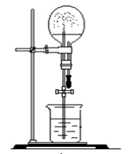
A . 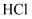 和
和  B .
B .  和
和  溶液
C .
溶液
C . 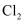 和饱和
和饱和  溶液
D .
溶液
D .  和
和 
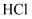 和
和  B .
B .  和
和  溶液
C .
溶液
C . 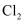 和饱和
和饱和  溶液
D .
溶液
D .  和
和 
甲、乙、丙、丁均为中学化学中常见的单质或化合物,它们之间的转化关系如图所示(部分产物已略去),下列各组物质中不能实现如图所示关系转化的是( )
| 选项 | 甲 | 乙 | 丙 | 丁 | 物质间的转化 |
| A | CuO | CO2 | CO | C | |
| B | Fe | Fe(NO3)2 | Fe(NO3)3 | HNO3 | |
| C | AlCl3 | Al(OH)3 | NaAlO2 | NH3·H2O | |
| D | CO2 | NaHCO3 | Na2CO3 | NaOH |
A . A
B . B
C . C
D . D
甲、乙、丙有如图所示的转化关系(“→”表示反应一步实现,部分物质和反应条件已略去)。下列各组物质按照甲、乙、丙的顺序不符合要求的是( )
![]()
A . C、CO、CO2
B . KOH、K2CO3、KNO3
C . CO2、CaCO3、CaCl2
D . Fe2O3、FeCl3、Fe(OH)3
2021年国务院政府工作报告指出,扎实做好碳达峰、碳中和各项工作。以下符合碳中和目的的是( )
A . 完全不排放CO2
B . 只用风能、太阳能等清洁能源
C . CO2排放量相对为零
D . 用碱吸收所有生成的CO2
向下列溶液中通入过量  , 最终会有固体析出的是( )
, 最终会有固体析出的是( )
 , 最终会有固体析出的是( )
, 最终会有固体析出的是( )
A . 澄清石灰水
B . 氯化钙溶液
C . 饱和碳酸钠溶液
D . 硝酸钡溶液
氧化物在生产生活中有广泛应用。下列有关氧化物的性质与用途具有对应关系的是( )
A . CO有还原性,可用于高炉炼铁
B . SiO2硬度高,可用作半导体材料
C . Al2O3具有两性,可用作耐火材料
D . ClO2易溶于水,可用于自来水消毒
膦(PH3)在常温下是一种无色有大蒜臭味的有毒气体,可用作高效熏蒸杀虫剂。以氟磷灰石[主要成分为Ca10(PO4)6Fx]、焦炭、石英砂为原料制备膦的一种工艺流程如下图所示。

查阅资料:
①白磷(P4)外观为白色或浅黄色半透明性固体,暴露空气中在暗处产生绿色磷光和白烟,在湿空气中约40℃着火,不溶于水。
②H3PO2属于一元中强酸、强还原剂,加热到130℃时分解成磷酸和磷化氢。
回答下列问题:
-
(1) Ca10(PO4)6Fx中,x的值为。
-
(2) 将固体原料精细研磨的目的是, 如果固体原料恰好完全反应,所得还原产物与氧化产物的物质的量之比为。
-
(3) 从P4(g)和CO的气体混合物中分离得到P4 (s),应选择下列试剂中的_______(填标号)。A . 冷水 B . 热水 C . 空气
-
(4) P4(s)与足量氢氧化钾溶液反应的离子方程式为。
-
(5) H3PO2在130℃时分解的化学方程式为。
-
(6) 已知:11PH3+24CuSO4+12H2O=8Cu3P+3H3PO4+24H2SO4 , 该反应原理可用于磷化氢中毒时,口服硫酸铜溶液催吐、解毒。消耗1. 1mol PH3时转移电子数目为。
2022年1月,国务院办公厅印发了《中央生态环境保护整改工作办法》,凸显了国家治理环境的决心和力度。下列说法错误的是( )
A . 工业上用氨水消除燃煤烟气中的 B . 纳米铁粉主要通过物理吸附除去污水中的
B . 纳米铁粉主要通过物理吸附除去污水中的 等重金属离子
C . 中国空间站宇航员采用多次蒸馏的方法,从尿液中分离出纯净水,实现了水的再生循环
D . 中国科学院在国际上首次实现了从
等重金属离子
C . 中国空间站宇航员采用多次蒸馏的方法,从尿液中分离出纯净水,实现了水的再生循环
D . 中国科学院在国际上首次实现了从 到淀粉的全合成,有利于促进“碳中和”
到淀粉的全合成,有利于促进“碳中和”
 B . 纳米铁粉主要通过物理吸附除去污水中的
B . 纳米铁粉主要通过物理吸附除去污水中的 等重金属离子
C . 中国空间站宇航员采用多次蒸馏的方法,从尿液中分离出纯净水,实现了水的再生循环
D . 中国科学院在国际上首次实现了从
等重金属离子
C . 中国空间站宇航员采用多次蒸馏的方法,从尿液中分离出纯净水,实现了水的再生循环
D . 中国科学院在国际上首次实现了从 到淀粉的全合成,有利于促进“碳中和”
到淀粉的全合成,有利于促进“碳中和”
二氧化碳的过量排放可对海洋环境造成影响,原理如图所示。下列叙述错误的是( )

A . 海水酸化引起 浓度增大
B . 海水酸化促进CaCO3的溶解、珊瑚礁减少
C . CO2引起海水酸化主要因为
浓度增大
B . 海水酸化促进CaCO3的溶解、珊瑚礁减少
C . CO2引起海水酸化主要因为
 H++
H++ D . 使用太阳能等新能源有利于改善海洋环境
D . 使用太阳能等新能源有利于改善海洋环境
 浓度增大
B . 海水酸化促进CaCO3的溶解、珊瑚礁减少
C . CO2引起海水酸化主要因为
浓度增大
B . 海水酸化促进CaCO3的溶解、珊瑚礁减少
C . CO2引起海水酸化主要因为
 H++
H++ D . 使用太阳能等新能源有利于改善海洋环境
D . 使用太阳能等新能源有利于改善海洋环境
最近更新




