同位素及其应用 知识点题库
最近科学家确认世界上还存在的另一种“分子足球”N60 , 它与C60的结构相似。下列说法正确的是( )
A . N60是一种新型化合物
B . N60和N2是同素异形体
C . N60和14N都是氮的同位素
D . N60和N2是同分异构体
在①178O、1②188O、③2311Na、④2412Mg、⑤146C、⑥147N中:
-
(1) 和互为同位素(填序号,下同);
-
(2) 和的质量数相等,但不能互称同位素;
-
(3) 和的中子数相等,但质子数不等,所以不是同一种元素.
下列叙述正确的是( )
A . 40K和40Ca原子中质子数和中子数都不相等
B . 金刚石和石墨的性质相同
C . H2和D2互为同位素
D . 某物质只含一种元素,该物质一定是纯净物
下列各组物质:①金刚石和石墨; ②H、D和T;③苯和乙苯;④CH3(CH2)2CH3和(CH3)2CHCH3中,互为同位素的是(填序号,下同),互为同素异形体的是,互为同系物的是,属于同分异构体的是.
2007年10月24日,“嫦娥一号”开始了它的探月历程,它的一项重要任务是探测月球表面土壤里的一种非常有用的资源﹣﹣可控核聚变的原料3He,3He是一种安全高效而又清洁无污染的物质,据统计,月球上的3He可以满足人类1万年以上的供电需求,月球土壤的3He含量可达500万吨.关于3He的叙述正确的是( )
A . 3He和4He两种核素互为同素异形体
B . 3He和4He两种核素互为同位素
C . 核聚变时,原子核发生了变化,发生了化学反应
D . 在3He中存在:质子数=中子数=核外电子数
-
(1) 元素周期律是元素原子随着元素核电荷数的递增发生周期性变化的必然结果;是元素周期律的具体体现。含有17个质子、18个中子的原子在元素周期表中的位置为:。
-
(2) ①168O、178O、188O ②H2O、D2O ③石墨、金刚石 ④H、D、T 四组微粒或物质中,互为同位素的是;(填序号,下同)互为同素异形体的是。
-
(3) 现有①SiO2、②碘、③Na2SO4、④NH4Cl四种晶体,按下列要求回答(用序号填空):
晶体熔化时需要破坏共价键的是;熔点最低的;晶体中只存在一种微粒间作用力是。
-
(1) 原子、元素、核素、同位素等都属于重要的化学基本概念。下列八种化学符号:

①涉及到的元素有种,核素共有种;
②互为同位素的是,;
-
(2) 在H、O、C、Na四种元素中,选择适当的元素组成符合下列要求的物质,将它们的化学式填写在以下空格中。(注意:每种物质只能出现一次)
酸性氧化物
碱性氧化物
酸
碱
电解质
非电解质
-
(3) 下列各组物质的分离或提纯,应选用下述方法的哪一种?(填选项字母)
A.分液 B.过滤 C.萃取
D.蒸馏 E.蒸发结晶 F.高温分解
①分离CCl4和H2O:;
②除去澄清石灰水中悬浮的CaCO3:;
③除去CaO固体中少量的CaCO3固体:;
④从碘水中提取碘:;
⑤分离CCl4(沸点为76.75℃)和甲苯(沸点为110.6℃)的液体混合物:。
下列说法中正确的是 ( )
A . H2和D2互为同位素
B . H2N—CH2—COOH和H3C—CH2—NO2互为同分异构体
C . 正丁烷、异丁烷、戊烷沸点依次增大
D . Fe2+和Fe3+互为同素异形体
12C和14C互为( )
A . 同分异构体
B . 同位素
C . 同系物
D . 同素异形体
 、
、  、
、  中数字1、2、3表示( )
中数字1、2、3表示( )
A . 中子数
B . 质量数
C . 核外电子数
D . 质子数
下列各组物质的分类正确的是( )
①混合物:氯水、氨水、水玻璃、水银、福尔马林、聚乙烯
②电解质:明矾、冰醋酸、石膏、纯碱
③CO2、NO2、P2O5均为酸性氧化物,Na2O、Na2O2为碱性氧化物
④同位素:1H+、2H2、3H
⑤同素异形体:C60、C80、金刚石、石墨
⑥同系物:CH2O2、C2H4O2、C3H6O2、C4H8O2
⑦同分异构体:乙二酸二乙酯、乙二酸乙二酯
⑧根据酸分子中含有的H原子个数将酸分为一元酸、二元酸、多元酸
⑨在熔化状态下能导电的化合物为离子化合物.
A . ②⑤⑨
B . ①②⑤⑦⑨
C . ②④⑤⑥⑦⑨
D . 全部符合题意
自门捷列夫发现元素周期律以来,人类对自然的认识程度逐步加深,元素周期表中的成员数目不断增加。回答下列问题:
-
(1) 2016年
 确认了四种新元素,其中一种为
确认了四种新元素,其中一种为 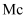 ,中文名为“镁”。元素
,中文名为“镁”。元素 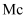 可由反应端
可由反应端  得到。该元素的质子数为,
得到。该元素的质子数为,  与
与  互为
互为
-
(2)
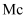 位于元素周期表中第
位于元素周期表中第  族,同族元素N的一种氢化物为
族,同族元素N的一种氢化物为  ,写出该化合物分子的电子式.该分子内存在的共价键类型有.
,写出该化合物分子的电子式.该分子内存在的共价键类型有.
-
(3) 该族中的另一元素P能显现多种化合价,其中
 价氧化物的分子式为
价氧化物的分子式为 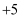 价简单含氧酸的分子式为
价简单含氧酸的分子式为
下列各项中有关判断正确的是( )
A . ①醋酸除水垢 ②石油分馏 ③煤的气化 ④海水中提取碘,过程中只涉及物理变化的是②③
B . ①CH4 和C3H8 ②O2 和O3 ③35Cl 和37Cl ④H2 和D2 , 属于同位素的微粒组是③④
C . ①金刚石熔化②氯化氢溶于水③氢氧化钾熔化④冰融化,上述过程与化学键断裂无关的是①④
D . ①酒精 ②冰醋酸 ③硝酸钾 ④醋酸钠,上述物质溶于水时会破坏水的电离平衡,且属于强电解质的仅是④
中国科学技术大学的钱逸泰教授等以CCl4和金属钠为原料,在700oC时反应制造出纳米级金刚石粉末和另一种化合物。该成果发表在世界权威的《科学》杂志上,立即被科学家们高度评价为“稻草变黄金”。同学们对此有下列一些“理解”,你认为其中错误的是( )
A . 这个反应是氧化还原反应
B . 制造过程中元素种类没有改变
C . 另一种化合物为NaCl
D . 金刚石属于碳的一种同位素
下列化学用语描述正确的是( )
A . 可用于考古断代的一种核素的符号:  B . 氚的原子结构模型:
B . 氚的原子结构模型:  C . 18O2ˉ离子的结构示意图:
C . 18O2ˉ离子的结构示意图:  D . 14C和14N互为同位素
D . 14C和14N互为同位素
 B . 氚的原子结构模型:
B . 氚的原子结构模型:  D . 14C和14N互为同位素
D . 14C和14N互为同位素
关于同位素、同素异形体、同系物、同分异构体说法错误的是( )
A . 碳原子数不同的烷烃互为同系物
B . 葡萄糖与蔗糖互称为同分异构体
C . 金刚石、石墨与C60互称为同素异形体
D . 同一种元素的同位素原子化学性质几乎相同
开发利用核能可以减少对化石能源的依赖。UO2是一种常用的核燃料,其铀元素中  需达到5%。该核燃料的一种制备流程如下:
需达到5%。该核燃料的一种制备流程如下:
 需达到5%。该核燃料的一种制备流程如下:
需达到5%。该核燃料的一种制备流程如下: 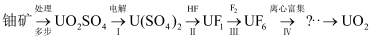
-
(1) 天然铀主要含99.3%
 和0.7%
和0.7%  ,
,  和
和  互为。
互为。
-
(2) I中,将含有硫酸的UO2SO4溶液通入电解槽,如下图所示。

①A电极是(填“阴极”或“阳极”),其电极反应式是。
②U4+有较强的还原性。用质子交换膜隔开两极区溶液可以,从而提高U4+的产率。
-
(3) III中使用的F2可通过电解熔融KF、HF混合物制备,不能直接电解液态HF的理由是HF属于化合物,液态HF几乎不电离。
-
(4) IV中利用了相对分子质量对气体物理性质的影响。铀的氟化物的熔沸点如下:
UF4
UF6
熔点/℃
1036
64(150kPa)
沸点/℃
1417
56.5升华
①离心富集
 时,采用UF6的优点:
时,采用UF6的优点:a.F只有一种核素
 ,且能与U形成稳定的氟化物;
,且能与U形成稳定的氟化物;b.。
②
 和
和  的相对分子质量之比约为(列出计算表达式)。
的相对分子质量之比约为(列出计算表达式)。
下列说法错误的是( )
A . CH4与CH3CH2CH3互为同系物
B . 金刚石和石墨互为同素异形体
C . 正丁烷与异丁烷互为同分异构体
D .  H2和
H2和 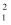 H2互为同位素
H2互为同位素
 H2和
H2和 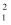 H2互为同位素
H2互为同位素
12C与14C互为( )
A . 同素异形体
B . 同分异构体
C . 同位素
D . 同系物
三种原子的原子结构可用下图形象地表示。下列叙述正确的是( )

A . ①②③质量数相同
B . ①②③性质完全相同
C . ①②③互为同位素
D . ①②③分别代表H、He、Li原子
最近更新



