氯离子的检验 知识点题库
①混合物加水得无色透明溶液;
②向上述溶液中滴加BaCl2溶液,有白色沉淀生成,将该沉淀滤出,并将滤液分成两份;
③上述白色沉淀可完全溶于稀盐酸;
④往一份滤液中滴加氯水并加入CCl4 , 振荡后静置CCl4层呈无色(氯水能将I-氧化为I2);
⑤往另一份滤液中加入AgNO3溶液,有白色沉淀生成,该沉淀不溶于稀硝酸。
由此可推断出:
-
(1) 写出③中白色沉淀可完全溶于稀盐酸的离子方程式。
-
(2) 写出⑤中生成白色沉淀的离子方程式。
-
(3) 该固体中一定含有;无法确定是否含有的是。
-
(4) 确定该物质是否存在的方法是。
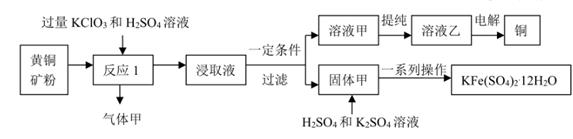
已知:气体甲是一种能使品红溶液褪色的黄绿色气体单质;固体甲是一种碱式盐,不溶于水,可溶于酸,甲中含有两种阳离子,且物质的量之比为1:3,取10.02g固体甲充分反应上理论得到铁钾矾30.18g
-
(1) 黄铜矿粉碎的目的是 。
-
(2) 反应1中,不宜先加H2SO4溶液,否则会产生一种具有臭鸡蛋气味的剧毒气体,试写出产生该变化对应的化学方程式: 。
-
(3) 固体甲中加入硫酸溶解,补充K2SO4溶液后,从溶液中提取铁钾矾晶体的一系列操作包括: 。
-
(4) 固体甲的化学式为。
-
(5) 反应1过程的离子方程式为:。
试设计实验检验浸取液中的主要阴离子:。
| 选项 | 实验 | 现象 | 结论 |
| A | 用铂丝试题蘸取少量某溶液进行焰色反应 | 火焰呈黄色 | 证明该溶液中存在Na+ , 不含K+ |
| B | 向某溶液中加入稀硝酸酸化的BaCl2溶液 | 产生白色沉淀 | 该溶液中一定存在SO42-或者Ag+ |
| C | 以铁为电极电解饱和食盐水,并将阳极产生的气体通入淀粉-KI溶液 | 变蓝 | 验证电解饱和食盐水阳极有氯气生成 |
| D | 滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口 | 试纸不变蓝 | 不能确定原溶液中含NH4+ |
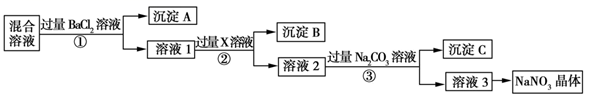
请回答下列问题:
-
(1) 写出实验流程中下列物质的化学式:试剂X,沉淀A。
-
(2) 上述实验流程中①②③步均要进行的实验操作是(填操作名称)。
-
(3) 上述实验流程中加入过量Na2CO3溶液的目的是。
-
(4) 按此实验方案得到的溶液3中肯定含有(填化学式)杂质。为了解决这个问题,可以向溶液3中加入适量的(填化学式),之后若要获得NaNO3晶体,需进行的实验操作是(填操作名称)。
①滴加Mg(NO3)2溶液; ②过滤; ③滴加AgNO3溶液; ④滴加Ba(NO3)2溶液
 中的几种,请填写下列空白:
中的几种,请填写下列空白:
-
(1) 不用做任何实验就可以肯定原溶液中不存在的离子是。
-
(2) 取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是。
-
(3) 取(2)中滤液,加入过量的氢氧化钠溶液,出现白色沉淀,说明原溶液中肯定有,写出加入氢氧化钠溶液发生的离子方程式:,。
-
(4) 原溶液中可能大量存在的阴离子是___(填字母)。A . Cl- B . NO
 C . CO
C . CO  D . OH-
D . OH-
| 试剂 | 现象 | 结论 | |
| A | 硝酸酸化的AgNO3溶液 | 产生白色沉淀 | 氯水中含有Cl- |
| B | CaCO3固体 | 固体表面有气泡冒出 | 氯水具有酸性 |
| C | KBr溶液 | 溶液变黄 | 氯水具有氧化性 |
| D | 滴加酚酞的NaOH溶液 | 红色褪去 | Cl2具有漂白性 |
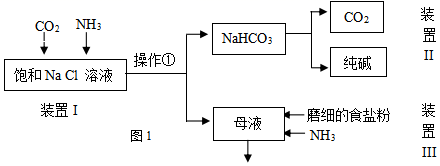
已知:几种盐的溶解度
|
物质 |
NaCl |
NH4HCO3 |
NaHCO3 |
NH4Cl |
|
溶解度 |
36.0 |
21.7 |
9.6 |
37.2 |
-
(1) ①写出装置I中反应的化学方程式。
②操作①的名称是。
-
(2) 写出装置II中发生反应的化学方程式。
-
(3) 该流程中可循环利用的物质是。(填化学式)
-
(4) 用该纯碱配制的溶液中可能含有Cl- , 请设计实验检验含有Cl-:。
-
(1) 向氢氧化铁胶体中不断滴加硝酸,可以看到的现象是,写出最后变化的离子方程式。
-
(2) 已知淀粉溶液(胶体)遇I2变蓝。现有淀粉和氯化钠的混合溶液,问:
①用法可以把它们分开。
②设计实验证明Cl-已分离干净。
 和
和 制备无水
制备无水 , 同时得到副产物
, 同时得到副产物 。实验室用如图装置模拟该制备过程(加热和固定装置已省略):
。实验室用如图装置模拟该制备过程(加热和固定装置已省略):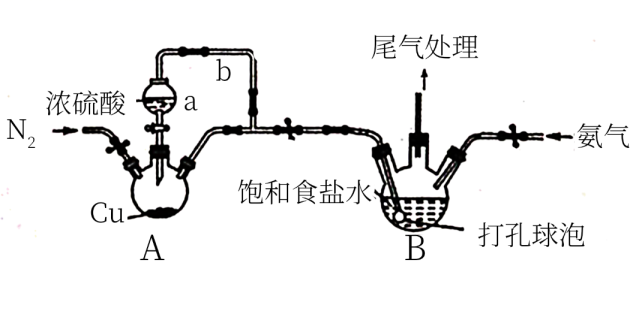
已知:浓硫酸的沸点为338℃.回答下列问题:
-
(1) 仪器a的名称,导气管b的作用.
-
(2) 装置A中发生的化学反应的化学方程式为.
-
(3) 氨气的发生装置可以选择下图中的(填编号),反应的化学方程式为.

-
(4) 利用各物质的溶解度曲线图(见图)分离产品.取出装置B中的溶液,蒸发浓缩,趁热过滤可得,然后将滤液、过滤、洗涤、干燥可得另一产物.
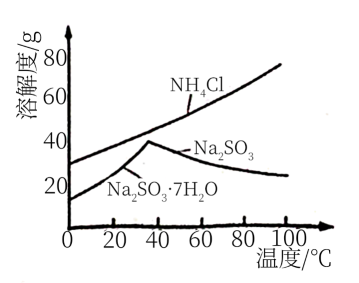
-
(5) 产品中可能混有少量
 和
和 杂质,混有
杂质,混有 杂质的原因可能是检验产品中含有
杂质的原因可能是检验产品中含有 的的实验方法:取少量样品于试管中,加入适量水溶解,。(可选试剂:稀硝酸、
的的实验方法:取少量样品于试管中,加入适量水溶解,。(可选试剂:稀硝酸、 溶液、酸性
溶液、酸性 溶液、
溶液、 溶液、
溶液、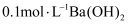 溶液、
溶液、 溶液)
溶液)
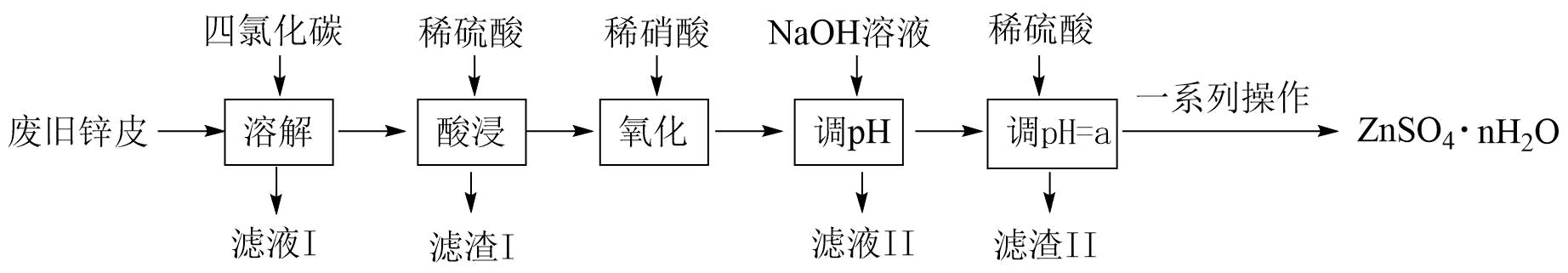
已知:常温下,金属离子开始沉淀及完全沉淀的pH如下表所示:
金属离子 | 开始沉淀的pH | 沉淀完全的pH |
Fe2+ | 7.5 | 9.0 |
Zn2+ | 6.5 | 8.0 |
Fe3+ | 2.2 | 3.5 |
通常认为溶液中离子浓度≤10-5mol·L-1为沉淀完全。请回答下列问题:
-
(1) “溶解”工序中除去废旧锌皮上物质的名称为。
-
(2) 滤渣I的主要成分为(填化学式)。“氧化”工序中发生反应的离子方程式为。
-
(3) 加入NaOH溶液调pH=8后,所得沉淀应用蒸馏水进行洗涤直至滤液中不再含有Cl- , 检验洗涤液中是否还含有Cl-的实验操作为。
-
(4) 加入稀硫酸调pH时,a的取值范围为。常温下,Ksp[(Zn(OH)2]和Ksp[Fe(OH)2]中数值更小的是,其数值为。
-
(5) ZnSO4·nH2O失去5个结晶水时,失重率约为31.35%,则n的值为。
人们常用84消毒液或医用酒精进行消毒。


84消毒液的名称源于北京某医院在1984年研制成功的一种高效含氯消毒液。84消毒液由Cl2与NaOH溶液反应制得,其主要成分为NaClO、NaCl,是无色或淡黄色液体。人们主要利用84消毒液中ClO-的氧化性进行消毒。
医用酒精中,乙醇的体积分数通常为75%。过高浓度的乙醇溶液会使病毒表面的蛋白质迅速凝结,形成一层保护膜,减弱消毒效果;过低浓度的乙醇溶液不能使蛋白质变性,同样不能获得很好的消毒效果。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
-
(1) 84消毒液的消毒原理与ClO-的氧化性有关。
-
(2) 用Cl2与NaOH溶液制备84消毒液的反应属于氧化还原反应。
-
(3) 乙醇溶液的浓度越高消毒效果一定越好。
-
(4) 医用酒精在使用过程中应注意避免明火。
 B . 取某溶液试样进行焰色试验,通过蓝色钴玻璃观察火焰呈紫色,则其为钾盐溶液
C . 往某溶液试样中滴加酚酞试液,溶液变红色,则该溶液一定是碱溶液
D . 取某溶液试样加足量硝酸无现象,再加
B . 取某溶液试样进行焰色试验,通过蓝色钴玻璃观察火焰呈紫色,则其为钾盐溶液
C . 往某溶液试样中滴加酚酞试液,溶液变红色,则该溶液一定是碱溶液
D . 取某溶液试样加足量硝酸无现象,再加 溶液产生白色沉淀,则原溶液中存在
溶液产生白色沉淀,则原溶液中存在
 C . 加入氯化钡溶液有白色沉淀生成,再加盐酸,沉淀不消失,一定有SO
C . 加入氯化钡溶液有白色沉淀生成,再加盐酸,沉淀不消失,一定有SO D . 焰色反应黄色火焰,一定有Na+ , 没有K+
D . 焰色反应黄色火焰,一定有Na+ , 没有K+



