еёёи§ҒиғҪйҮҸзҡ„иҪ¬еҢ–еҸҠиҝҗз”Ё зҹҘиҜҶзӮ№йўҳеә“
A | B | C | D |
|
|
|
|
зЎ…еӨӘйҳіиғҪз”өжұ | й”ӮзҰ»еӯҗз”өжұ | еӨӘйҳіиғҪйӣҶзғӯеҷЁ | зҮғж°”зҒ¶ |
|
|
|
|
AпјҺй”Ңй”°зўұжҖ§з”өжұ | BпјҺзЎ…еӨӘйҳіиғҪз”өжұ | CпјҺж°ўзҮғж–ҷз”өжұ | DпјҺ银й”ҢзәҪжүЈз”өжұ |

 2SO3(g) в–іH =-198kJ/molпјҢеңЁV2O5еӯҳеңЁж—¶пјҢиҜҘеҸҚеә”жңәзҗҶдёә:V2O5+SO2вҶ’2VO3+SO3(еҝ«)пјӣ4VO2+O2вҶ’2V2O5(ж…ў)пјҲ пјү
2SO3(g) в–іH =-198kJ/molпјҢеңЁV2O5еӯҳеңЁж—¶пјҢиҜҘеҸҚеә”жңәзҗҶдёә:V2O5+SO2вҶ’2VO3+SO3(еҝ«)пјӣ4VO2+O2вҶ’2V2O5(ж…ў)пјҲ пјү

 2SO3(g)дёәж”ҫзғӯеҸҚеә”пјҢеҲҷSO2зҡ„иғҪйҮҸдёҖе®ҡй«ҳдәҺSO3зҡ„иғҪйҮҸ
B . иӢҘC(зҹіеўЁпјҢs)=C(йҮ‘еҲҡзҹіпјҢs) О”H>0пјҢеҲҷзҹіеўЁжҜ”йҮ‘еҲҡзҹізЁіе®ҡ
C . е·ІзҹҘNaOH(aq)пјӢHCl(aq)=NaCl(aq)пјӢH2O(l) О”H=пјҚ57.4 kJВ·molпјҚ1 пјҢ еҲҷ20.0 g NaOHеӣәдҪ“дёҺзЁҖзӣҗй…ёе®Ңе…Ёдёӯе’ҢпјҢж”ҫеҮә28.7 kJзҡ„зғӯйҮҸ
D . е·ІзҹҘ2C(s)пјӢ2O2(g)=2CO2(g) О”H1пјӣ2C(s)пјӢO2(g)=2CO(g) О”H2 пјҢ еҲҷО”H1>О”H2
2SO3(g)дёәж”ҫзғӯеҸҚеә”пјҢеҲҷSO2зҡ„иғҪйҮҸдёҖе®ҡй«ҳдәҺSO3зҡ„иғҪйҮҸ
B . иӢҘC(зҹіеўЁпјҢs)=C(йҮ‘еҲҡзҹіпјҢs) О”H>0пјҢеҲҷзҹіеўЁжҜ”йҮ‘еҲҡзҹізЁіе®ҡ
C . е·ІзҹҘNaOH(aq)пјӢHCl(aq)=NaCl(aq)пјӢH2O(l) О”H=пјҚ57.4 kJВ·molпјҚ1 пјҢ еҲҷ20.0 g NaOHеӣәдҪ“дёҺзЁҖзӣҗй…ёе®Ңе…Ёдёӯе’ҢпјҢж”ҫеҮә28.7 kJзҡ„зғӯйҮҸ
D . е·ІзҹҘ2C(s)пјӢ2O2(g)=2CO2(g) О”H1пјӣ2C(s)пјӢO2(g)=2CO(g) О”H2 пјҢ еҲҷО”H1>О”H2
в‘ з”өи§ЈжҳҜжҠҠз”өиғҪиҪ¬еҸҳжҲҗеҢ–еӯҰиғҪ в‘Ўз”өи§ЈжҳҜжҠҠеҢ–еӯҰиғҪиҪ¬еҸҳжҲҗз”өиғҪ в‘ўз”өи§ЈиҙЁжә¶ж¶ІеҜјз”өжҳҜеҢ–еӯҰеҸҳеҢ–пјҢйҮ‘еұһеҜјз”өжҳҜзү©зҗҶеҸҳеҢ–в‘ЈдёҚиғҪиҮӘеҸ‘иҝӣиЎҢзҡ„ж°§еҢ–иҝҳеҺҹеҸҚеә”пјҢйҖҡиҝҮз”өи§Јзҡ„еҺҹзҗҶеҸҜд»Ҙе®һзҺ°в‘Өд»»дҪ•жә¶ж¶Іиў«з”өи§Јж—¶пјҢеҝ…然еҜјиҮҙж°§еҢ–иҝҳеҺҹеҸҚеә”зҡ„еҸ‘з”ҹ

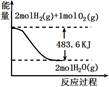
 O2(g)=H2O(g)+241.8kJ
C . иЎЁзӨә1molH2(g)е®Ңе…ЁзҮғзғ§з”ҹжҲҗж°ҙи’ёж°”еҗёж”¶241.8kJзғӯйҮҸ
D . иЎЁзӨә2molH2(g)жүҖе…·жңүзҡ„иғҪйҮҸдёҖе®ҡжҜ”2molж°”жҖҒж°ҙжүҖе…·жңүзҡ„иғҪйҮҸеӨҡ483.6kJ
O2(g)=H2O(g)+241.8kJ
C . иЎЁзӨә1molH2(g)е®Ңе…ЁзҮғзғ§з”ҹжҲҗж°ҙи’ёж°”еҗёж”¶241.8kJзғӯйҮҸ
D . иЎЁзӨә2molH2(g)жүҖе…·жңүзҡ„иғҪйҮҸдёҖе®ҡжҜ”2molж°”жҖҒж°ҙжүҖе…·жңүзҡ„иғҪйҮҸеӨҡ483.6kJ

-
пјҲ1пјү иҜҘз ”з©¶жҲҗжһңдёӯж¶үеҸҠзҡ„иғҪйҮҸиҪ¬жҚўеҪўејҸдёә
-
пјҲ2пјү е·ІзҹҘпјҡеңЁдёҖе®ҡжё©еәҰе’ҢеҺӢејәдёӢпјҢз”ұжңҖзЁіе®ҡеҚ•иҙЁз”ҹжҲҗ1molеҢ–еҗҲзү©зҡ„з„“еҸҳз§°дёәиҜҘзү©иҙЁзҡ„ж‘©е°”з”ҹжҲҗз„“гҖӮжҹҗдәӣеҢ–еҗҲзү©зҡ„ж‘©е°”з”ҹжҲҗз„“еҰӮиЎЁжүҖзӨәгҖӮ
еҢ–еҗҲзү©
CO2(g)
CH3OH(g)
H2O(g)
ж‘©е°”з”ҹжҲҗз„“/(kJВ·mol-1)
-395
-200
-242
еҸҚеә”в… пјҡCO2(g)+3H2(g)
 CH3OH(g)+H2O(g)в–іH1
CH3OH(g)+H2O(g)в–іH1еҸҚеә”в…ЎпјҡCO2(g)+H2(g)
 CO(g)+H2O(g)в–іH2
CO(g)+H2O(g)в–іH2в‘ еҸҚеә”в… зҡ„з„“еҸҳв–іH1=kJВ·mol-1гҖӮ
в‘ЎдҝқжҢҒжё©еәҰTдёҚеҸҳпјҢеңЁдёҖеҲҡжҖ§еҜҶй—ӯе®№еҷЁдёӯпјҢе……е…ҘдёҖе®ҡйҮҸзҡ„CO2еҸҠH2 пјҢ иө·е§ӢеҸҠиҫҫе№іиЎЎж—¶пјҢе®№еҷЁеҶ…еҗ„ж°”дҪ“зү©иҙЁзҡ„йҮҸеҰӮиЎЁжүҖзӨәгҖӮ
CO2
H2
CH3OH
CO
H2O
иө·е§ӢйҮҸ/mol
4.0
8.0
0
0
0
е№іиЎЎйҮҸ/mol
n1
3.0
е·ІзҹҘиө·е§Ӣж—¶жҖ»еҺӢејәдёә1.5pkPaпјҢе№іиЎЎж—¶дҪ“зі»жҖ»еҺӢејәдёәpkPaпјҢеҲҷиЎЁдёӯn1=пјҢеҸҚеә”Iзҡ„е№іиЎЎеёёж•°Kp=гҖӮ(ж— йңҖеёҰеҚ•дҪҚпјҢз”Ёеҗ«pзҡ„ејҸеӯҗиЎЁзӨә)гҖӮ
-
пјҲ3пјү еҸ–зү©иҙЁзҡ„йҮҸжө“еәҰдёәamolВ·L-1зҡ„з”ІйҶҮпјҢйҖүжӢ©дёҚеҗҢзҡ„е·ҘзЁӢй…¶з»„еқ—дҪңдёәеӮ¬еҢ–еүӮеҸҚеә”10hпјҢжөӢеҫ—е®һйӘҢж•°жҚ®еҰӮиЎЁжүҖзӨәгҖӮ
е®һйӘҢеәҸеҸ·
жё©еәҰ(K)
дёҚеҗҢе·ҘзЁӢй…¶зҡ„з»„еқ—
ж·ҖзІү(g/L)
1
T1
ж—
0.21
2
T1
agp-M1
0.38
3
T2
agp-M2
1.82
4
T2
agp-M3
1.24
в‘ жңҖдҪізҡ„еҸҚеә”жқЎд»¶дёә
в‘Ўе·ІзҹҘжё©еәҰеҚҮй«ҳпјҢеҸҚеә”з”ҹжҲҗзҡ„ж·ҖзІүйҮҸе…ҲеўһеҠ еҗҺжҖҘеү§еҮҸе°‘пјҢе…¶еҸҜиғҪзҡ„еҺҹеӣ жҳҜгҖӮ
в‘ўе®һйӘҢ4еҸҜз”Ёж·ҖзІүзҡ„иҙЁйҮҸжө“еәҰиЎЁзӨәеҸҚеә”йҖҹзҺҮдёәgВ·L-1В·h-1 пјҢ ж·ҖзІүзҡ„дә§зҺҮдёә(з”Ёеҗ«aзҡ„д»Јж•°ејҸиЎЁзӨә)гҖӮ
-
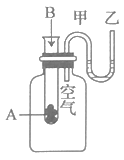
пјҲ1пјү иҜҘеҸҚеә”дёә(еЎ«вҖңж”ҫзғӯвҖқжҲ–вҖңеҗёзғӯвҖқ)еҸҚеә”гҖӮ
-
пјҲ2пјү еҸҚеә”зү©Aе’ҢBзҡ„жҖ»иғҪйҮҸжҜ”з”ҹжҲҗзү©Cе’ҢDзҡ„жҖ»иғҪйҮҸ(еЎ«вҖңй«ҳвҖқжҲ–дҪҺвҖқ)гҖӮ
-
пјҲ3пјү иҜҘеҸҚеә”иҝҮзЁӢдёӯпјҢзү©иҙЁдёӯзҡ„иғҪйҖҡиҝҮеҢ–еӯҰеҸҚеә”иҪ¬еҢ–жҲҗиғҪйҮҠж”ҫеҮәжқҘгҖӮ
-
пјҲ4пјү иҜҘеҸҚеә”иҝҮзЁӢдёӯпјҢеҸҚеә”зү©еҢ–еӯҰй”®ж–ӯиЈӮеҗёж”¶зҡ„иғҪйҮҸ(еЎ«вҖңй«ҳвҖқжҲ–вҖңдҪҺвҖқ)дәҺз”ҹжҲҗзү©еҢ–еӯҰй”®еҪўжҲҗж”ҫеҮәзҡ„иғҪйҮҸгҖӮ
-
пјҲ5пјү дёӢеҲ—еҸҚеә”з¬ҰеҗҲйўҳдёӯе®һйӘҢзҺ°иұЎзҡ„жҳҜ____(еЎ«ж ҮеҸ·)гҖӮA . 2Al+6HCl=2AlCl3+3H2вҶ‘ B . 2Na+2H2O=2NaOH+H2вҶ‘ C . NaOH+HCl=NaCl+H2O D . Na2O2+2CO2=2Na2CO3+O2











