钠的化学性质 知识点题库
下列物质的转化在给定条件下能实现的是( )
A . Na  Na2O2
Na2O2  Na2CO3
B . MgCO3
Na2CO3
B . MgCO3  MgCl2溶液
MgCl2溶液  Mg
C . Fe
Mg
C . Fe  Fe2O3
Fe2O3  Fe2(SO4)3
D . SiO2
Fe2(SO4)3
D . SiO2  SiCl4
SiCl4  Si
Si
 Na2O2
Na2O2  Na2CO3
B . MgCO3
Na2CO3
B . MgCO3  MgCl2溶液
MgCl2溶液  Mg
C . Fe
Mg
C . Fe  Fe2O3
Fe2O3  Fe2(SO4)3
D . SiO2
Fe2(SO4)3
D . SiO2  SiCl4
SiCl4  Si
Si
钠与水反应的离子方程式正确的是( )
A . 2Na+3H+═2Na++H2↑
B . Na+H2O═Na++OH﹣+H2↑
C . 2Na+2H2O═2Na++2OH﹣+H2↑
D . 2Na+2H2O═2Na++O2↑+2H2↑
关于钠及其氧化物性质的叙述中,正确的是( )
A . Na能与CuSO4溶液反应置换出红色的铜
B . Na2O是碱性氧化物,与酸反应生成盐和水
C . Na2O和Na2O2都能与水反应,生成物完全相同
D . Na2O2是白色固体,可用于呼吸面具中氧气的来源
①钠比水要轻;②钠的熔点比较低;③钠与水反应时要放出热量;④钠与水反应后溶液呈碱性;⑤钠是活泼金属.某学生将一小块金属钠投入到滴有酚酞的水中,该实验能证明上述五点性质中的( )
A . 仅①④⑤
B . 仅①②④
C . 仅①③④⑤
D . ①②③④⑤
下列物质暴露在空气中,不容易变质的是( )
A . Na
B . FeSO4
C . SiO2
D . Na2O2
一定质量的钠、钾投入一定量的稀盐酸中,产生气体随时间变化的曲线如图所示,则下列说法正确的是( )

A . 投入的Na、K一定等质量
B . 投入的Na的质量小于K的质量
C . 曲线a为Na,b为K
D . 稀盐酸的量一定是不足量的
金属钠着火,能用来灭火的是( )
A . 水
B . 湿抹布
C . 泡沫灭火剂
D . 干沙
下列解释实验现象的反应方程式正确的是( )
A . 切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O2=Na2O2
B . 金属钠比通金属铜活泼,金属钠放入CuSO4溶液:CuSO4+2Na=Cu+Na2SO4
C . Na2O2在潮湿的空气中放置一段时间,变成白色粘稠物:2Na2O2+2CO2=2Na2CO3+O2
D . 将Na块放入水中,产生气体:2Na+2H2O=2NaOH+H2↑
下列关于钠单质性质的叙述中不正确的是( )
A . 在空气中极易被氧化,常保存在煤油中
B . 是一种银白色金属,具有金属光泽
C . 能与氯化铜溶液反应生成氯化钠和铜
D . 在空气中燃烧火焰为黄色
观察是研究物质性质的基本方法。一同学将一小块金属钠露置于空气中,观察到下列现象:银白色  变灰暗
变灰暗  变白色
变白色  表面潮湿
表面潮湿  白色固体,下列说法错误的是( )
白色固体,下列说法错误的是( )
 变灰暗
变灰暗  变白色
变白色  表面潮湿
表面潮湿  白色固体,下列说法错误的是( )
白色固体,下列说法错误的是( )
A . ①中钠发生了氧化反应
B . ②变白色是因为生成了氢氧化钠
C . ③发生物理变化
D . ④生成了碳酸氢钠
下列有关化学反应的叙述正确的是( )
A . CuSO4稀溶液与Na反应析出Cu
B . Fe与水蒸气在高温下反应生成Fe2O3
C . SO2的水溶液与溴蒸气反应富集溴
D . 饱和食盐水与通入的NH3、CO2反应析出Na2CO3固体
将a mol钠和a mol铝一同投入m g足量水中,所得溶液密度为d g·mL-1 , 该溶液中溶质质量分数为( )
A . 82a/(46a+m)%
B . 8200a/(46a+2m) %
C . 8200a/(46a+m)%
D . 8200a/(69a+m) %
在甲、乙、丙、丁四个烧杯中分别放入 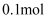 的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体全溶解,有甲、乙、丙、丁内溶液的溶质质量分数大小的顺序为( )
的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体全溶解,有甲、乙、丙、丁内溶液的溶质质量分数大小的顺序为( )
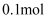 的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体全溶解,有甲、乙、丙、丁内溶液的溶质质量分数大小的顺序为( )
的钠、氧化钠、过氧化钠和氢氧化钠,然后各加入100mL水,搅拌,使固体全溶解,有甲、乙、丙、丁内溶液的溶质质量分数大小的顺序为( )
A . 甲<乙<丙<丁
B . 丁<甲<乙=丙
C . 甲=丁<乙=丙
D . 丁<甲<乙<丙
下列指定反应的离子方程式正确的是( )
A . 钠与水反应:Na+H2O=Na++OH-+H2↑
B . 向AlCl3溶液中加入过量氨水:Al3++4NH3·H2O=  +4
+4  +2H2O
C . FeCl3溶液净水原理:Fe3++3H2O=Fe(OH)3↓+3H+
D . 用饱和Na2CO3溶液处理重晶石:BaSO4+
+2H2O
C . FeCl3溶液净水原理:Fe3++3H2O=Fe(OH)3↓+3H+
D . 用饱和Na2CO3溶液处理重晶石:BaSO4+  -=BaCO3+
-=BaCO3+ 
 +4
+4  +2H2O
C . FeCl3溶液净水原理:Fe3++3H2O=Fe(OH)3↓+3H+
D . 用饱和Na2CO3溶液处理重晶石:BaSO4+
+2H2O
C . FeCl3溶液净水原理:Fe3++3H2O=Fe(OH)3↓+3H+
D . 用饱和Na2CO3溶液处理重晶石:BaSO4+  -=BaCO3+
-=BaCO3+ 
下列方案设计、现象和结论都正确的是( )
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究乙醇消去反应的产物 | 取 | 若溴水褪色,则乙醇消去反应的产物为乙烯 |
| B | 探究乙酰水杨酸样品中是否含有水杨酸 | 取少量样品,加入 | 若有紫色沉淀生成,则该产品中含有水杨酸 |
| C | 探究金属钠在氧气中燃烧所得固体粉末的成分 | 取少量固体粉末,加入 | 若无气体生成,则固体粉末为 |
| D | 探究 | 取少量待测样品溶于蒸馏水,加入足量稀盐酸,再加入足量 | 若有白色沉淀产生,则样品已经变质 |
A . A
B . B
C . C
D . D
下列关于金属钠的叙述中,说法正确的是( )
A . 金属钠可以保存在少量水中
B . 钠长时间暴露在空气中,最终产物是Na2CO3
C . 钠是银白色金属,硬度大,熔点高
D . Na与CuSO4溶液反应可以置换出Cu单质
金属钠与水反应的实验中,与钠的下列性质无关的是( )
A . 密度比水小
B . 熔点低
C . 硬度小
D . 强还原性
回答下列问题:
-
(1) 实验室,少量的钠应保存在中;加热铝箔的实验现象是,原因是(用化学方程式表示)。
-
(2) 在含氮的常见化合物中,常用作制冷剂的是,原理是(用适当文字描述)。
-
(3) 某工厂的燃料煤中硫的质量分数为0.4%,该工厂每天燃烧这种煤80t,试计算:
①若煤中的硫全部转化为SO2 , 该工厂每天产生的SO2的质量为kg。
②如果把产生的SO2全部回收利用,理论上每年(360天)得到的98%的浓硫酸的质量为kg。
下列实验装置不能达到实验目的的是( )
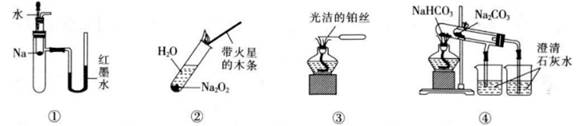
A . 利用装置①验证Na和水反应为放热反应
B . 利用装置②检验Na2O2与H2O反应有O2生成
C . 利用装置③观察纯碱的焰色试验的现象
D . 利用装置④比较Na2CO3和NaHCO3的热稳定性
用铝箔包裹0.1mol金属钠,用针刺出一些小孔,放入水中,完全反应后,产生的气体在标准状况下的体积为( )
A . 小于1.12L
B . 1.12L
C . 在1.12L和4.48L之间
D . 大于4.48L
最近更新
 乙醇,加入
乙醇,加入  浓硫酸、少量沸石,迅速升温至140℃,将产生的气体通入
浓硫酸、少量沸石,迅速升温至140℃,将产生的气体通入 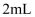 溴水中
溴水中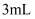 蒸馏水和少量乙醇,振荡,再加入1-2滴
蒸馏水和少量乙醇,振荡,再加入1-2滴  溶液
溶液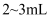 蒸馏水
蒸馏水 ;若有气体生成,则固体粉末为
;若有气体生成,则固体粉末为 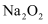
 固体样品是否变质
固体样品是否变质 溶液
溶液


