钠的氧化物 知识点题库
①立即有大量气泡生成.
②无色透明的酚酞溶液迅速变红,振荡后,溶液中的红色褪去,又变为无色.
③反应放出大量的热量,试管壁手触感觉很烫.
请回答:
(1)该兴趣小组同学认为酚酞试液颜色变化的为:
假设①: .
假设②:可能是反应放出的热量,使红色消失.
假设③:可能是Na2O2与水反应生成的NaOH溶液浓度太大,使得酚酞变性,不显颜色.
(2)验证假设②,设计补充实验:取滴加酚酞的稀NaOH溶液加热,若红色消失,则证明假设②成立;若红色不消失,则假设②不成立.
(3)验证假设③,设计补充实验: .
-
(1) 焊接钢铁时常用的焊药为氯化铵,其作用是消除焊接处的铁锈。发生的反应体系中共有六种物质:NH4Cl、N2、Fe2O3、Fe、FeCl3 和 X。
①根据题意,可判断出X是(写化学式)
②写出并配平该反应的化学方程式,并用双线桥标出电子转移的方向和数目:。
-
(2) 铝元素是自然界中含量最多的的金属元素,应用广泛。金属铝既能与酸反应又能与强碱反应,请写出铝与强碱反应的离子方程式 。
-
(3) Na2O2可用作呼吸面具的供氧剂,发生反应的化学方程式为。
-
(4) “水玻璃”长期暴露在空气中会变质,这是因为“水玻璃”与空气中少量二氧化碳接触,生成了乳白色的凝胶状沉淀的缘故。写出反应的离子方程式。
-
(5) 小苏打可作胃药,请写出其中和胃酸时的离子方程式 。
-
(6) 在反应 3BrF3+5H2O = HBrO3+Br2+9HF+O2 中,被氧化的元素是,当有5 mol水反应时,由H2O还原的BrF3为mol。

请回答:
-
(1) W的电子式是。
-
(2) X与Y在溶液中反应的离子方程式是。
-
(3) X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。

①装置Ⅰ中反应的化学方程式是,
装置Ⅱ中物质的化学式是。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,该化合物的化学式是,所需仪器装置是。
(从上图选择必要装置,填写编号)
-
(4) 向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是。

-
(1) Ⅰ.实验探究
装置A中用粗锌和稀盐酸制取氢气,B装置的作用是,里面所盛放的试剂是(①浓硫酸②碱石灰③无水硫酸铜)。
-
(2) 下面是实验过程中的重要操作,正确的顺序是________(填序号)A . 加热至Na2O2逐渐熔化,反应一段时间 B . 用小试管收集气体并检验其纯度 C . 打开K1、K2 , 通入氢气 D . 停止加热,充分冷却,关闭K1、K2
-
(3) 实验过程中观察到淡黄色粉末慢慢变成白色固体,无水硫酸铜未变蓝色。由此可推测出Na2O2与H2反应生成的产物为。
-
(4) Ⅱ.数据处理
实验结束后,该同学欲测定C装置内白色固体中未反应完的Na2O2含量。其操作流程如图:

①测定过程中需要的仪器除固定、夹持仪器外,还有天平、烧杯、酒精灯、蒸发皿和,操作2的名称是。
②白色固体中Na2O2的质量分数为(用含m1和m2的式子表示)。
③在转移溶液时,若溶液转移不完全,则测得的Na2O2质量分数(填“偏大”“偏小”或“不变”)。

-
(1) Na、Na2O、Na2O2、NaOH久置空气中最终都是变为(填化学式);
-
(2) Na放在石棉网上加热反应的化学方程式为。
-
(3) Na2O2与CO2反应的化学方程式为。
-
(4) 写出除去下列气体中的杂质(括号内的气体为杂质)所用的试剂,并写出除杂的化学方程式。
CO2(HCl);化学方程式:。
-
(5) 用1L1.0mol·L-1的NaOH溶液吸收0.8molCO2 , 所得溶液Na2CO3中和NaHCO3物质的量浓度之比为。
-
(1) 写出下列物质的化学式:
A,B ,C,D ,E 。
-
(2) 写出下列反应的化学方程式(③写出离子方程式):
①A生成B: ;
②B与水反应生成E:;
③向C的溶液中通入足量的酸性气体D的离子方程式:。
①Na2O2中阴、阳离子的个数比是1∶1
②Na2O2分别与水及CO2反应产生等量氧气时,需水和CO2的质量相等
③Na2O2分别与水及CO2反应产生等量氧气时,转移电子的物质的量相等
④Na2O2的漂白原理与SO2的漂白原理相同
⑤Na2O2与SO2反应生成Na2SO3与O2
⑥Na2O2能与酸反应生成盐和水,所以Na2O2是碱性氧化物
⑦Na2O2与水反应,Na2O2既是氧化剂,又是还原剂
⑧Na2O2投入到紫色石蕊溶液中,溶液先变蓝,后褪色

回答下列问题:
-
(1) 如图所示组装好实验装置后,首先应该进行的操作是:。
-
(2) 分液漏斗中所装试剂是。
-
(3) 装置D中发生反应的化学方程式是:、。
-
(4) E中碱石灰的作用是。
-
(5) 若开始时测得试样的质量为2.5g,反应结束后测得收集气体的体积为336mL(标准状况),则试样中Na2O2的百分含量为。
| 选项 | 实验操作 | 现象 | 实验结论 |
| A | 将湿润的有色布条放入充满氯气的集气瓶中 | 布条褪色 | 氯气具有漂白性 |
| B | 向KMnO4溶液中滴加某溶液,振荡 | 紫红色褪去 | 该溶液一定是KI溶液 |
| C | 向CaCl2溶液中通入适量CO2 | 产生白色沉淀 | 白色沉淀为CaCO3 |
| D | 向包有Na2O2粉末的脱脂棉滴几滴水 | 脱脂棉剧烈燃烧 | Na2O2与水反应放热且有O2生成 |
 价
C . 过氧化钠分别与H2O、CO2反应产生等质量O2时,转移电子的物质的量不相等
D . 过氧化钠与水反应时,过氧化钠既是氧化剂又是还原剂
价
C . 过氧化钠分别与H2O、CO2反应产生等质量O2时,转移电子的物质的量不相等
D . 过氧化钠与水反应时,过氧化钠既是氧化剂又是还原剂
①Na2O与Na2O2都能和水反应生成碱,它们都是碱性氧化物
②Na2O与CO2发生化合生成Na2CO3 , Na2O2与CO2发生置换生成O2
③Na2O是淡黄色物质,Na2O2是白色物质
④Na2O2可作供氧剂,而Na2O不行
⑤Na2O2和Na2O焰色反应均为黄色
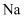 加入到
加入到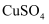 溶液中产生红色金属单质
D .
溶液中产生红色金属单质
D . 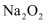 可以作为呼吸面具或潜水艇里的氧气来源
可以作为呼吸面具或潜水艇里的氧气来源
 在水中能形成
在水中能形成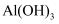 胶体,可用作净水剂
胶体,可用作净水剂



