两性氧化物和两性氢氧化物 知识点题库
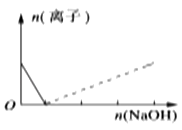 B .
B . 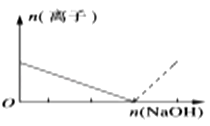 C .
C . 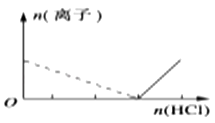 D .
D . 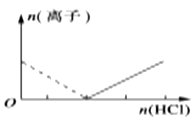
①Al ②Al2O3③NaHCO3④Al(OH)3⑤SiO2 .
①将CO2通入溶有足量氨的BaCl2溶液中,无白色沉淀生成
②向某溶液中滴入盐酸酸化的BaCl2溶液产生白色沉淀,证明溶液中一定含有SO42﹣
③将两小块质量相等的金属钠,一块直接投入水中,另一块用铝箔包住,在铝箔上刺些小孔,放入水中,两者放出的氢气质量相等
④氢氧化铝具有弱碱性,可用于制胃酸中和剂.

-
(1) 混合物中各物质的物质的量:
NaOH是,AlCl3是,MgCl2是。
-
(2) C点所加的盐酸的体积是mL。
①  固体既能溶于
固体既能溶于 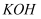 溶液得到
溶液得到 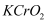 溶液,又能溶于硫酸得到
溶液,又能溶于硫酸得到 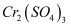 溶液;
溶液;
②向 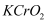 溶液中滴加
溶液中滴加  溶液,再酸化,可得
溶液,再酸化,可得  溶液;
溶液;
③将  溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
溶液滴加到淀粉和KI的混合溶液中,溶液变蓝。
下列判断错误的是( )
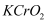 中
中 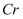 元素为+3价
B . 实验①证明
元素为+3价
B . 实验①证明  是两性氧化物
C . 实验②证明
是两性氧化物
C . 实验②证明  既有氧化性又有还原性
D . 实验③证明氧化性:
既有氧化性又有还原性
D . 实验③证明氧化性: 
选项 | 实验操作 | 实验现象 | 结论 |
A | 在AlCl3溶液中逐滴滴入NaOH溶液至过量,然后通入CO2气体 | 先出现白色沉淀,后沉淀消失,最后又出现白色沉淀 | Al(OH)3是两性氢氧化物,但不能溶解在某些弱酸中 |
B | 向浓度均为0.1mol/L的MgCl2、CuCl2混合溶液中逐滴加入氨水 | 先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
C | 向Na2CO3溶液中加入浓盐酸,将产生的气体通入硅酸钠溶液中 | 产生白色浑浊 | 酸性:盐酸>碳酸>硅酸 |
D | 向盛有KI3溶液的两试管中分别加入淀粉溶液和AgNO3溶液 | 前者溶液变蓝色,后者有黄色沉淀 | KI3溶液中存在I3- |
|
X |
Y |
Z |
|
|
① |
NaOH溶液 |
Al(OH)3 |
稀硫酸 |
|
② |
Na2O2 |
Na2CO3 |
NaHCO3 |
|
③ |
KOH溶液 |
Al |
稀盐酸 |
-
(1) 同组物质中,Y既能与X发生氧化还原反应,又能与Z发生氧化还原反应的是(填数字符号)。若Y与X或Z完全反应,产生的气体在标准状况下的体积为 67.2L,则转移电子的数目为。
-
(2) 写出第①组X与Y反应的离子方程式。
-
(3) 第②组固体X可作供氧剂,写出其中与二氧化碳的化学反应方程式。

-
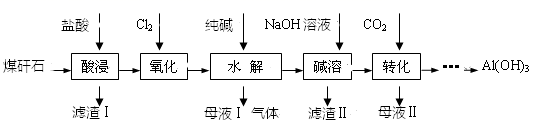
(1) “酸浸”过程中发生的主要反应的离子方程式为。
-
(2) “氧化”的目的是。检验Fe3+的方法是。
-
(3) 滤渣I的主要成分。溶于酸的反应方程式。
-
(4) ②“转化”时主要反应的离子方程式为。
 O2(g)=H2O(l) ΔH=-286 kJ·mol−1 , 则每1 mol [H2(g)+
O2(g)=H2O(l) ΔH=-286 kJ·mol−1 , 则每1 mol [H2(g)+  O2(g)]生成1 mol [H2O(l)]放热286 kJ
B . Cr2O72-+ne−+14H+=2Cr3++7H2O,则每生成1 mol Cr3+转移电子数为3NA
C . Al3++4OH−=[Al(OH)4]− , 说明1 mol Al(OH)3电离出H+数为NA
D . 1 mol CO2与NaOH溶液完全反应,则n(CO32-)+n(HCO3-)+n(H2CO3)=1 mol
O2(g)]生成1 mol [H2O(l)]放热286 kJ
B . Cr2O72-+ne−+14H+=2Cr3++7H2O,则每生成1 mol Cr3+转移电子数为3NA
C . Al3++4OH−=[Al(OH)4]− , 说明1 mol Al(OH)3电离出H+数为NA
D . 1 mol CO2与NaOH溶液完全反应,则n(CO32-)+n(HCO3-)+n(H2CO3)=1 mol
选项 | 生活用途 | 化学原理 |
A | 电热水器内胆连接镁棒防止腐蚀 | 牺牲阳极的阴极保护法 |
B | 过氧化钠用作呼吸面具或潜水艇中的供氧剂 | 过氧化钠具有氧化性 |
C | 明矾可用作净水剂和消毒剂 | 铝离子水解生成氢氧化铝胶体 |
D | 铁粉和生石灰常用作袋装食品的抗氧化剂 | 能够吸收氧气防止食品腐坏 |



