2019年九年级上半年化学中考模拟在线免费考试
| 1. | 详细信息 |
|
下列变化中,属于化学变化的是 A. 冰雪融化 B. 大米霉变 C. 玻璃破碎 D. 酒精挥发 |
|
| 2. | 详细信息 |
|
硅酸钠(Na2SiO3)溶液在建筑行业上可用作防腐剂与粘合剂,硅酸钠属于 A. 酸 B. 碱 C. 盐 D. 氧化物 |
|
| 3. | 详细信息 |
|
下列物质由原子直接构成的是 A. 氯化钠 B. 水银 C. 酒精 D. 氧气 |
|
| 4. | 详细信息 |
|
Cr2O3可以作某些化学反应的催化剂,其中Cr元素的化合价为 A. +1 B. +2 C. +3 D. +6 |
|
| 5. | 详细信息 |
|
下列物质加入水中能形成溶液的是 A. 蔗糖 B. 汽油 C. 泥土 D. 生铁 |
|
| 6. | 详细信息 |
|
下列物质敞口放置于空气中一段时间,质量会增加的是 A. 食盐水 B. 石灰石 C. 浓盐酸 D. 生石灰 |
|
| 7. | 详细信息 |
为保证安全,面粉加工厂内应该张贴下列哪种标志 |
|
| 8. | 详细信息 |
|
下列有关物质用途的叙述不正确的是 A. 活性炭:吸附异味 B. 氯化钠:常见的调味品 C. 烧碱:改良酸性土壤 D. 硫酸铜:可用于配农药波尔多液 |
|
| 9. | 详细信息 |
|
下列有关实验现象的叙述正确的是 A. 镁条在空气中燃烧,产生大量黑色固体 B. NH4NO3溶于水时,放出热量,温度升高 C. 加碘食盐溶液中加入淀粉,溶液变蓝 D. 足量SO2通入稀高锰酸钾溶液中,溶液褪色 |
|
| 10. | 详细信息 |
|
下列实验装置或操作正确的是 A.  保存氧气 B. 保存氧气 B. 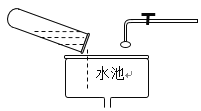 处理废弃药品 处理废弃药品C.  蒸发食盐水 D. 蒸发食盐水 D.  滴加试剂 滴加试剂 |
|
| 11. | 详细信息 |
|
Sb2O5是一种重要的阻燃剂。用X来生产该阻燃剂的化学方程式为: X + 2H2O2 ==Sb2O5+2H2O,根据质量守恒定律,推断X的化学式为 A.SbO2 B.Sb2O3 C.HSbO3 D.H3SbO4 |
|
| 12. | 详细信息 |
|
我国民间有端午节挂艾草驱虫辟邪的习俗,艾草中含有丰富的黄酮素(化学式为C15H10O2)。下列关于黄酮素的叙述正确的是 A. 黄酮素属于有机物 B. 黄酮素中碳、氢元素的质量比为3∶2 C. 黄酮素中含有氧分子 D. 黄酮素的相对分子质量为222 g |
|
| 13. | 详细信息 |
|
下列说法正确的是 A. pH<7的雨水称为酸雨 B. 用汽油洗去衣服上的油污是乳化作用 C. 铁钉在潮湿空气中易生锈 D. 煤、石油、乙醇是三大重要的化石燃料 |
|
| 14. | 详细信息 |
如图是某化学反应前后分子变化的微观示意图,下列说法错误的是 A. 图中共表示了4种物质 B. 该图表示的是一个化合反应 C. 化学反应中,原子发生重新组合 D. 化学反应前后,分子的种类一定发生改变 |
|
| 15. | 详细信息 |
用下列实验装置进行相应实验,能达到实验目的的是 A. 用甲所示装置配制20%的Ca(OH)2溶液 B. 用乙所示装置验证铁、铜、银三种金属的活动性顺序 C. 用丙所示装置验证中和反应的热效应 D. 用丁所示装置验证面粉粉尘能发生爆炸 |
|
| 16. | 详细信息 | |||||||||||||||||||||||||
除去下列物质中的少量杂质,所选用试剂和主要操作均正确的是
|
||||||||||||||||||||||||||
| 17. | 详细信息 |
利用如下装置进行实验,下列有关实验和结论正确的是 A. 缓慢通入N2,再加热Ⅰ处的碳酸氢铵,可观察到Ⅱ处红色石蕊试纸变成蓝色 B. 先缓慢通入CO2,再加热Ⅰ处炭粉,一定观察到Ⅱ处氧化铁粉末由红色变成黑色 C. 先缓慢通入空气,再加热Ⅰ处红磷,根据Ⅰ处燃烧而Ⅱ处红磷不燃烧说明可燃物燃烧一般需要与氧气接触 D. 先缓慢通入空气,再加热Ⅰ处8.00 g黄铁矿样品(主要成分为FeS2,杂质高温下不反应,反应方程式为:4FeS2 +11O2 |
|
| 18. | 详细信息 |
KNO3与NaCl的溶解度曲线如图所示。下列说法正确的是 A. t1℃时,等质量的KNO3和NaCl饱和溶液中溶质质量一定相等 B. t2℃时,100 g KNO3的饱和溶液中含KNO3 60 g C. KNO3溶液中混有少量NaCl,可采用蒸发结晶的方法提纯KNO3 D. 其它条件不变,升高温度可使KNO3的饱和溶液变成不饱和溶液 |
|
| 19. | 详细信息 |
|
关于反应:X + Y→MgSO4 + m H2O(未配平,m为正整数),下列说法正确的是 A. 该反应一定是中和反应 B. 若m等于2时,则X和Y质量比为1:2 C. X、Y中一定均含有氧元素 D. 若X和MgSO4质量比为1:3时,则m一定等于1 |
|
| 20. | 详细信息 |
水是生命之源,人类是自然之子,水则如同孕育生命的母亲。2019年5月3日至6日,首届大运河文化旅游博览会在扬州成功举办。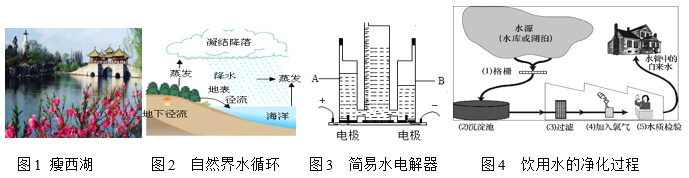 (1)图1:“诗画瘦西湖,人文古扬州”。清澈的瘦西湖水是_____(填“混合物”或“纯净物”)。经检测,湖水为轻度富营养化,是由_____(填元素符号)元素引起的。 (2)图2:在水蒸发的过程中,下列说法正确的是_____(填字母)。 a.水分子大小改变 b.水分子之间间隔不变 c.氢、氧原子不变 地下水中的颗粒和细菌等杂质比湖水、河水等地表水中的少,请写出一个原因_____。 (3)图3:通电一段时间后,若A管中收集2L的气体,则B管内收集的气体体积约为_____L。电解时,加入少量NaOH能增强导电性,是因为其溶于水能产生自由移动的_____和_____(填离子符号)。电解水的化学方程式为_____。 (4)图4:水源中含有较多的杂质。含有较多可溶性钙、镁化合物的水叫做_____(填“软水”或“硬水”),区分硬水和软水常用_____(填物质名称)。图中氯气的作用是_____。 |
|
| 21. | 详细信息 |
|
阅读下面文字,回答相关问题。 油炸薯片受到营养专家的反对,因为其经油炸后含有大量的反式脂肪酸(C18H34O2)。反式脂肪酸进入人体后,导致必需脂肪酸缺乏;抑制婴幼儿的生长发育等。下图为某品牌薯片的包装和营养成分表:  (1)厂商常将N2充入包装袋内做保护气,是因为N2的化学性质_____(填“活泼”或“稳定”);该包装采用铝塑袋包装,它是在双层塑料薄膜中间夹一层铝膜,该包装袋是_____(填字母)。 a.无机材料 b.合成纤维 c.复合材料 (2)表中的脂肪、蛋白质和_____能够为人体提供能量。营养成分表中未标示,但_____和水也是人体必需的基本营养物质。食用下列扬州特产主要与蛋白质摄入有关的是_____(填字母)。 a.仪征紫菜 b.高邮咸鸭蛋 c.宝应藕粉 (3)表中的钠元素_____(填“属于”或“不属于”)人体必需的微量元素;儿童缺少_____(填元素符号),也会导致生长发育迟缓,智力低下。 (4)反式脂肪酸(C18H34O2)_____(填“是”或“不是”)有机高分子,其中碳元素的质量分数为_____(精确到0.1%)。 |
|
| 22. | 详细信息 |
|
氯化钡是一种可溶性重金属盐,广泛应用于化工领域。工业上以重晶石(主要成分BaSO4,杂质为Fe2O3)为原料,通过下列流程生成氯化钡晶体(BaCl2·xH2O)并进行组成测定。 已知:①BaSO4+4C ②CaO、BaO都能与水反应生成碱  (1)焙烧时,焦炭与杂质Fe2O3也会发生反应,反应方程式为_____;实际生产中必须加入过量焦炭,其目的是使重晶石充分反应,提高产率和_____。 (2)焙烧时,温度和时间对硫酸钡转化率的影响如下图,则最佳温度约为_____℃,时间约为_____min。  (3)酸溶时,硫化钡(BaS)与盐酸发生复分解反应产生硫化氢气体(H2S),该反应方程式为_____;气体X成分除H2S和少量挥发出的HCl、水蒸气外,还含有_____。 (4)除铁反应中试剂Y可以是_____(填字母)。 a.NaOH溶液 b.氨水 c.生石灰 d.BaO固体 证明铁已除尽的方法是:取上层清液于试管中,滴入_____溶液,若无明显现象,则已除尽。 (5)滤渣水洗的目的是提高晶体产率和_____。 (6)测定晶体(BaCl2·xH2O)的组成: Ⅰ.称取24.4gBaCl2晶体,置于小烧杯中,加入适量蒸馏水,使其全部溶解。 Ⅱ.再边搅拌边滴加稀硫酸到沉淀完全,静置; Ⅲ.过滤并洗涤沉淀; Ⅳ.将盛有沉淀的滤纸包烘干并中温灼烧后,称得BaSO4沉淀质量为23.3g。 ①通过计算,确定x的值。_____(写出计算过程) ②操作Ⅳ中,如果空气不充足和温度过高,可能会有部分沉淀被滤纸中的碳还原为BaS,这使x的测定结果_____(填“偏低”、“偏高”或“不变”)。 |
|
| 23. | 详细信息 |
|
CO2是一种宝贵的碳氧资源。某兴趣小组对CO2的研究如下: 已知:常温下,CO2难溶于饱和NaHCO3溶液。 Ⅰ.CO2的制备和收集: 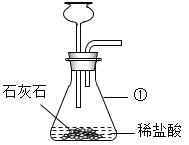 (1)写出图中标号仪器的名称:①_____。 (2)写出用石灰石和稀盐酸制取CO2的化学方程式_____。图中装置有一处明显的错误是_____。 (3)常温下,下列收集CO2的方法中可行的是_____(填字母)。 a.向上排空气法 b.向下排空气法 c.排饱和NaHCO3溶液法 Ⅱ.CO2的利用: 全球能源生产正向“氢能经济”转型,以CO2和可再生生物资源(如纤维素等)为原料生产氢气已成为能源研究的重点。下图是某新型能源转换与利用模式示意图:  (4)该模式中涉及的能源转化依次为:太阳能→生物质能→氢能→_____。 (5)该系统中循环使用的物质是_____。 (6)与电解水相比,该模式制取氢气的主要优点是_____。 Ⅲ.探究CO2与NaOH的反应:  (7)如图装置,气密性良好。在A处放置适量干冰,B处装入适量的浓NaOH溶液,烧杯中加入足量的稀盐酸。实验过程中,观察到乙中导管口有气泡冒出,原因是_____。 (8)一段时间后,观察到的现象是:乙中_____,B中_____,说明CO2与NaOH发生反应,写出CO2与NaOH反应方程式为_____。 |
|
| 24. | 详细信息 | |||||||||||||||||||||||||||||||||||||||||||||||
|
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染。同学们对废旧手机中的金属回收产生兴趣。 (提出问题) 从废旧手机中可以回收到哪些有价值的金属?如何回收?  (查阅资料) Ⅰ.手机电路板中的金属及其价格如下表所示:
|
||||||||||||||||||||||||||||||||||||||||||||||||




