云南2018年高二化学上期期中考试免费试卷
| 1. 选择题 | 详细信息 |
|
构成金属晶体的微粒是 A. 原子 B. 分子 C. 金属阳离子 D. 金属阳离子和自由电子 |
|
| 2. 选择题 | 详细信息 |
|
已知SO3,BF3,CCl4,PCl5、SF6都是非极性分子,而H2S,NH3,NO2、SF4,BrF5都是极性分子,由此可推出ABn型分子属于非极性分子的经验规律是( ) A. ABn型分子中A,B均不含氢原子 B. A元素的相对原子质量必小于B元素的相对原子质量 C. 分子中所有原子都在同一平面上 D. ABn型的价电子对数等于n |
|
| 3. 选择题 | 详细信息 |
|
下列说法正确的是( ) A. π键是由两个p电子以“头碰头”方式重叠而成 B. σ键是镜面对称,而π键是轴对称 C. 乙烷分子中的键全为σ键而乙烯分子中含σ键和π键 D. H2分子中含σ键,Cl2分子中含π键 |
|
| 4. 选择题 | 详细信息 |
|
下列说法中不正确的是( ) A. 一般情况下,σ键比π键重叠程度大,形成的共价键强 B. 两个原子间形成共价键时,最多有一个σ键 C. 在气体单质中,一定有σ键,可能有π键 D. N2分子中有1个σ键,2个π键 |
|
| 5. 选择题 | 详细信息 |
|
下列物质的变化过程中有共价键明显被破坏的是( ) ①I2升华 ②氯化钠溶于水 ③氯化氢溶于水 ④碳酸氢铵中闻到了刺激性气味 A. ①② B. ①③ C. ②③ D. ③④ |
|
| 6. 选择题 | 详细信息 |
钛酸钡的热稳定性好,介电常数高,在小型变压器、话筒和扩音器中都有应用.钛酸钡晶体的晶胞结构示意图如图所示,它的化学式是( )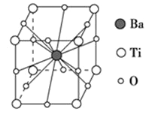 A. BaTi8O12 B. BaTi4O6 C. BaTi2O4 D. BaTiO3 |
|
| 7. 选择题 | 详细信息 |
|
下列各组原子中,彼此化学性质一定相似的是( ) A. 原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 B. 原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 C. 2p轨道上只有2个电子的X原子与3p轨道上只有2个电子的Y原子 D. 最外层都只有一个电子的X、Y原子 |
|
| 8. 选择题 | 详细信息 |
|
当一个碳原子所连四个不同原子或原子团时,该碳原子叫“手性碳原子”。下列化合物中含有2个手性碳原子的是( ) A. 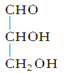 B. B. 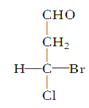 C. C. 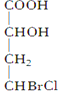 D. D. 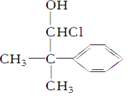 |
|
| 9. 选择题 | 详细信息 |
|
下列有关离子晶体的数据大小比较不正确的是( ) A. 熔点:NaF>MgF2>AlF3 B. 晶格能:NaF>NaCl>NaBr C. 阴离子的配位数:CsCl>NaCl>CaF2 D. 硬度:MgO>CaO>BaO |
|
| 10. 选择题 | 详细信息 |
|
下列说法不正确的是( ) A. 基态氧原子与基态氮原子中未成对电子数之比是2∶3 B. 基态氮原子与基态磷原子中未成对电子数之比是1∶1 C. 基态碳原子与基态氮原子中未成对电子数之比是3∶4 D. 基态铜原子中未成对电子数是1 |
|
| 11. 选择题 | 详细信息 |
|
下列说法正确的是 A. NaOH是含有非极性共价键的离子晶体 B. 氯化钠与氯化铯的晶体结构完全相同 C. 金刚石、硅、锗的熔点和硬度依次降低 D. NaF、MgF2、AlF3三种离子晶体的晶格能逐渐减小 |
|
| 12. 选择题 | 详细信息 |
|
下列不属于金属晶体的共性的是( ) A. 易导电 B. 易导热 C. 有延展性 D. 高熔点 |
|
| 13. 选择题 | 详细信息 |
|
下列表示式错误的是( ) A. Na+的轨道表示式: C. Na的电子排布式:1s22s22p63s1 D. Na的外围电子排布式:3s1 |
|
| 14. 选择题 | 详细信息 |
|
下列现象不能用“相似相溶原理”解释的是( ) A. 氯化氢易溶于水 B. 氯气易溶于氢氧化钠溶液中 C. 碘易溶于四氯化碳 D. 碘难溶于水 |
|
| 15. 选择题 | 详细信息 |
|
下列叙述中错误的是( ) A. 钠原子和氯原子作用生成NaCl后,其结构的稳定性增强 B. 在氯化钠晶体中,除氯离子和钠离子的静电吸引作用外,还存在电子与电子、原子核与原子核之间的排斥作用 C. 任何离子键在形成的过程中必定有电子的得与失 D. 钠与氯气反应生成氯化钠后,体系能量降低 |
|
| 16. 选择题 | 详细信息 |
|
下列说法中正确的是( ) A. 1s22s12p1表示的是激发态原子的核外电子排布 B. 3p2表示3p能级有两个轨道 C. 同一原子中,1s、2s、3s电子的能量逐渐减小 D. 同一原子中,2p、3p、4p能级中的轨道数依次增多 |
|
| 17. 选择题 | 详细信息 |
|
下列变化中,不存在化学键断裂的是 A. 氯化氢气体溶于水 B. 干冰气化 C. 氯化钠固体溶于水 D. 氢气在氯气中燃烧 |
|
| 18. 选择题 | 详细信息 |
|
在金属晶体中,如果金属原子的价电子数越多,原子半径越小,自由电子与金属阳离子间的作用力越大,金属的熔沸点越高。由此判断下列各组金属熔沸点高低顺序,其中正确的是( ) A. Mg>Al>Ca B. Al>Na>Li C. Al>Mg>Ca D. Mg>Ba>Al |
|
| 19. 选择题 | 详细信息 |
|
下列说法不正确的是( ) A. 离子晶体的晶格能越大离子键越强 B. 阳离子的半径越大则可同时吸引的阴离子越多 C. 通常阴、阳离子的半径越小、电荷越大,该阴阳离子组成离子化合物的晶格能越大 D. 拆开1mol离子键所需的能量叫该离子晶体的晶格能 |
|
| 20. 选择题 | 详细信息 |
|
下列说法中正确的是( ) A. 处于最低能量的原子叫做基态原子 B. 原子由基态变为激发态要产生发射光谱 C. 同一原子中,2p能级比3p能级的轨道数少 D. 3d轨道能量小于4s |
|
| 21. 选择题 | 详细信息 |
|
下列事实不能用键能的大小来解释的是( ) A.N元素的电负性较大,但N2的化学性质很稳定 B.稀有气体一般难发生反应 C.HF、HCl、HBr、HI的稳定性逐渐减弱 D.F2比O2更容易与H2反应 |
|
| 22. 选择题 | 详细信息 |
|
某元素基态原子失去3个电子后,3d轨道半充满,其原子序数为( ) A. 24 B. 25 C. 26 D. 27 |
|
| 23. 选择题 | 详细信息 |
|
氯化硼的熔点为﹣107℃,沸点为12.5℃,在其分子中键与键之间的夹角为120°,它能水解,有关叙述正确的是( ) A.氯化硼液态时能导电而固态时不导电 B.氯化硼加到水中使溶液的pH升高 C.氯化硼分子呈正三角形,属非极性分子 D.氯化硼遇水蒸气会产生白雾 |
|
| 24. 选择题 | 详细信息 |
|
下列叙述中正确的是( ) A. 同一周期中,第ⅦA族元素的原子半径最大 B. 第ⅥA族元素的原子,其半径越大,越容易得到电子 C. 室温时,0族元素的单质都是气体 D. 同一周期中,碱金属元素的第一电离能最大 |
|
| 25. 选择题 | 详细信息 |
|
下列电子排布式或电子排布图正确的是( ) A. O的电子排布图: B. Ca的电子排布式:1s22s22p63s23p63d2 C. N的电子排布图: D. Br-的电子排布式:[Ar]3d104s24p6 |
|
| 26. 选择题 | 详细信息 |
|
通常把原子总数和价电子总数相同的分子或离子称为等电子体。人们发现等电子体的空间结构相同,则下列有关说法中正确的是( ) A. CH4和NH4+是等电子体,键角均为60° B. NO3―和CO32―是等电子体,均为平面正三角形结构 C. H3O+和PCl3是等电子体,均为三角锥形结构 D. B3N3H6和苯是等电子体,B3N3H6分子中不存在“肩并肩”式重叠的轨道 |
|
| 27. 选择题 | 详细信息 |
|
下列有关范德华力的叙述正确的是( ) A. 范德华力的实质也是一种电性作用,所以范德华力是一种特殊的化学键 B. 范德华力与化学键的区别是作用力的强弱不同 C. 任何分子间在任意情况下都会产生范德华力 D. 范德华力非常微弱,故破坏范德华力不需要消耗能量 |
|
| 28. 选择题 | 详细信息 |
|
从键长的角度来判断下列共价键中最稳定的是 A. H—F B. H—N C. H—C D. H—S |
|
| 29. 选择题 | 详细信息 |
最近发现了一种由金属原子M和非金属原子N构成的气态团簇分子,如图所示,顶角和面的原子是M原子,棱中心和体心的原子是N原子,它的分子式为( )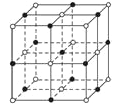 A. M4N4 B. MN C. M14N13 D. 条件不够,无法写出 |
|
| 30. 选择题 | 详细信息 |
|
下列既有离子键又有共价键的化合物是( ) A. Na2O B. NaOH C. CaBr2 D. HF |
|
| 31. 填空题 | 详细信息 |
金晶体的最小重复单元(也称晶胞)是面心立方体,如图所示,即在立方体的8个顶点各有一个金原子,各个面的中心有一个金原子,每个金原子被相邻的晶胞所共有。金原子的直径为d,用NA表示阿伏加德罗常数,M表示金的摩尔质量。请回答下列问题: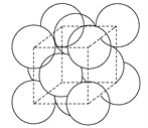 (1)金晶体每个晶胞中含有________个金原子。 (2)欲计算一个晶胞的体积,除假定金原子是刚性小球外,还应假定_______________。 (3)一个晶胞的体积是____________。 (4)金晶体的密度是____________。 |
|
| 32. 综合题 | 详细信息 |
如图所示为高温超导领域里的一种化合物——钙钛矿晶体结构,该结构是具有代表性的最小重复单位。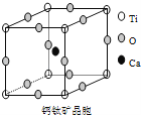 (1)在该物质的晶体结构中,每个钛离子周围与它最接近且距离相等的钛离子、钙离子各有__、__个。 (2)该晶体结构中,元素氧、钛、钙的离子个数比是__.该物质的化学式可表示为__。 (3)若钙、钛、氧三元素的相对原子质量分别为a,b,c,晶体结构图中正方体边长(钛离子之间的距离)为dnm(1nm=10﹣9m),则该晶体的密度为__g/cm3。 |
|
| 33. 填空题 | 详细信息 |
有下列离子晶体立体构型示意图如下图所示。 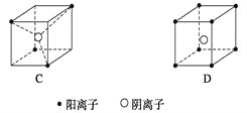 (1)以M代表阳离子,以N代表阴离子,写出各离子晶体的组成表达式。 A.__________,B:________,C:________,D:__________________________。 (2)已知FeS2晶体(黄铁矿的主要成分)具有A的立体结构。 ①FeS2晶体中具有的化学键类型是__________________________________________。 ②若晶体结构A中相邻的阴、阳离子间的距离为acm,且用NA代表阿伏加德罗常数,则FeS2晶体的密度是________g·cm-3。 |
|
| 34. 综合题 | 详细信息 |
|
有A,B,C,D四种元素。已知:①它们均为周期表中前20号元素,C,D在同一周期,A,B在同一主族;②它们可以组成化合物B2C2、A2C、DC2等;③B的阳离子与C的阴离子的核外电子排布相同;④B2C2同A2C或DC2反应都生成气体C2,B与A2C反应产生气体A2,A2与气体C2按体积比2∶1混合后点燃能发生爆炸,其产物是一种无色无味的液体(在常温下)。请回答下列问题: (1)写出A,B,C,D四种元素的符号: A________,B________,C________,D________。 (2)在B2C2、A2C和DC2中,属于离子化合物的是________,其电子式是__________________,属于共价化合物的是____________,其结构式是____________________。并指出含几个σ键,几个π键。 (3)写出有关的化学方程式:_____________________________________。 |
|
| 35. 综合题 | 详细信息 |
|
现有四种短周期元素A,B,C,D,已知:①C,D在同一周期,A,B在同一主族;②它们可以组成化合物A2C、B2C2、DC2、D2A4等;③B的阳离子与C的阴离子的核外电子排布相同;④B2C2同A2C或DC2反应都生成气体C2,B与A2C反应生成气体A2,A2与气体C2按体积比2∶1混合后点燃发生爆炸,其产物是一种常温下常见的无色无味的液体。请回答: (1)写出元素符号:A________、B________、C________、D________。 (2)在A2C、B2C2、DC2和D2A4中,同时含有离子键和非极性共价键的化合物的电子式为__________;按原子轨道重叠方式,其非极性键的类型是________。化合物DC2的结构式__________。 (3)A2C分子的电子式____________,按原子轨道重叠方式,其共价键的类型是____________。D2A4是平面形分子,其分子中含有______个σ键,______个π键。 (4)写出化学方程式或离子方程式: B2C2与A2C反应的化学方程式:___________________________________________; B2C2与DC2反应的化学方程式:___________________________________________; B与A2C反应的离子方程式:______________________________________________。 |
|
最近更新



