2019-2020年高一4月测试化学考题(四川省资中县第三中学)
| 1. 选择题 | 详细信息 |
|
化学与生活密切相关。下列说法错误的是( ) A.工业可用二氧化硫漂白纸浆、毛、丝、草帽辫等,也可用于杀菌消毒 B.医用消毒酒精中乙醇的浓度(体积分数)为 95% C.燃煤中加入 CaO 可以减少酸雨的形成却不能减少温室气体的排放 D.天然气和液化石油气是我国目前推广使用的清洁燃料 |
|
| 2. 选择题 | 详细信息 |
|
除去二氧化碳中混有的少量二氧化硫气体,不可选用的试剂是( ) A.饱和碳酸钠溶液 B.高锰酸钾溶液 C.溴水 D.饱和碳酸氢钠溶液 |
|
| 3. 选择题 | 详细信息 |
|
有一酸性溶液可能含有Br-、SO42-、H2SO3、NH4+ 等微粒,对该酸性溶液分别进行实验: (1)加热,放出的气体可以使品红溶液褪色; (2)取原溶液加碱,调至溶液呈碱性,加热,放出的气体能使湿润的红色石蕊试纸变蓝; (3)取原溶液加氯水,溶液略显黄色,再加入BaCl2溶液,产生的白色沉淀不溶于稀硝酸。 对于下列微粒不能确认其在原溶液中是否存在的是 A.SO42- B.Br- C.H2SO3 D.NH4+ |
|
| 4. 选择题 | 详细信息 |
下列实验装置不能达到实验目的的是 A. A B. B C. C D. D |
|
| 5. 选择题 | 详细信息 |
|
下列关于元素周期表的说法正确的是( ) A. 元素周期表有7个周期,8个主族 B. 元素周期表有18个纵行,共16个族 C. 短周期元素中可能有副族元素 D. 元素周期表中的过渡元素就是副族元素 |
|
| 6. 选择题 | 详细信息 |
下图所示各为元素周期表中的一部分,表中数字是原子序数,其中X为35的是 A. A B. B C. C D. D |
|
| 7. 选择题 | 详细信息 |
|
A. C. |
|
| 8. 选择题 | 详细信息 |
|
某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子。在ag HmX中所含质子的物质的量是( ) A. B. C. D. |
|
| 9. 选择题 | 详细信息 |
如图是一块非常独特的手表,用 H~Mg 12 种元素分别表示 1:00~12:00,关于此表的下列说法中不正确的是( ) A.2:00 时的时针和 12:00 时的分针所指元素极难形成化合物 B.7:00 时,时针和分针所指元素可能形成相对分子质量为 100 的化合物 C.8:00 时,时针和分针所指元素形成的化合物属于碱性氧化物 D.3:00 时,时针所指元素的金属性比 11:00 时时针所指元素的金属性强 |
|
| 10. 选择题 | 详细信息 |
|
下列物质的性质与氢键无关的是( ) A.NH3分子比PH3分子稳定 B.通常情况NH3极易溶于水 C.冰的密度小于水的密度 D.H2O的沸点比H2S的沸点高 |
|
| 11. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.双原子分子中的共价键一定是非极性键 B.任何原子的原子核都是由质子和中子构成的 C.非极性键可能存在于离子化合物中 D.质子数相同的微粒,它们的化学性质基本相同 |
|
| 12. 选择题 | 详细信息 |
|
下列分子中所有原子都满足最外层8电子稳定结构的是( ) A.PCl5 B.CH4 C.BF3 D.CS2 |
|
| 13. 选择题 | 详细信息 |
|
下列有关化学用语表示正确的是( ) A.次氯酸的结构式:H−Cl−O B.18O2−的结构示意图:  C.氨气的电子式: D.电子式表示氯化钠的形成过程: |
|
| 14. 选择题 | 详细信息 |
|
从化学键的角度看化学反应的实质是“旧化学键的断裂,新化学键的形成”,下列既有旧化学键的断裂,又有新化学键的形成的变化是 A.碘升华 B.Cl2 溶于水 C.氯化钠受热熔化 D.酒精溶解于水 |
|
| 15. 选择题 | 详细信息 |
短周期元素W、X、Y、Z 的原子序数依次增加。m、p、r 是由这些元素组成的二元化合物,n 是元素Z 的单质,通常为黄绿色气体,q 的水溶液具有漂白性,r 溶于水是强酸,s 通常是难溶于水的混合物。上述物质的转化关系如图所示。下列说法正确的是 ( ) A.W 在周期表中所在族全是金属 B.X 的最高价氧化物的水化物为强酸 C.Y 的氢化物常温常压下为气态 D.1molZ 单质与氢氧化钠溶液反应转移 1mol 电子 |
|
| 16. 选择题 | 详细信息 |
元素 R、X、T、Z、Q 在元素周期表中的相对位置如图所示,其中 R 的氢化物的水溶液可以用来刻蚀玻璃,则下列判断正确的是( ) A.气态氢化物的酸性:R>T>Q B.气态氢化物的还原性:X>T C.R 与 Q 的电子数相差 16 D.R 的单质通入 T 的钠盐溶液中能置换出T 的单质 |
|
| 17. 选择题 | 详细信息 |
|
短周期元素X、Y、Z、W的原子序数依次递增,X原子的最外层电子数是内层电子数的3倍,X、W同主族。Y、Z是同周期相邻的两种元素,Y的最高价氧化物对应的水化物是一种两性化合物。下列判断正确的是( ) A. 原子半径:r(W)>r(Z)>r(Y)>r(X) B. Y元素的最高价氧化物对应的水化物既能与盐酸反应,也能与氨水反应 C. 最简单气态氢化物的热稳定性:W>Z D. W元素的单质在暗处能与H2剧烈化合并发生爆炸 |
|
| 18. 选择题 | 详细信息 |
|
NA 为阿伏加德罗常数的值,下列说法不正确的是( ) A.0.l mol Cl2与足量的铁粉充分反应转移的电子数为 0.2 NA B.1.0 mol CH4 与Cl2 在光照下反应生成的 CH3Cl 分子数为 1.0 NA C.标准状况下,11.2 L甲烷和乙烯(C2H4)混合物中含氢原子数目为2 NA D.0.1mol Cl2 通入水中,HClO、Cl-、ClO-粒子数之和小于 0.2 NA |
|
| 19. 选择题 | 详细信息 |
|
下列烷烃的沸点由低到高的顺序排列正确的是( ) ①CH3CH2CH2CH3 ②  ④ ④A.①②③④ B.②①④③ C.③④①② D.②①③④ |
|
| 20. 选择题 | 详细信息 |
|
下列烷烃在光照下与氯气反应,能生成三种一氯代烃的是( ) A.CH3CH2CH2CH3 B.  C.  D. D. |
|
| 21. 选择题 | 详细信息 |
|
1.92g 铜投入一定量浓 HNO3 中,铜完全溶解,生成气体颜色越来越浅,共收集到672mL 气体(标况)。将盛有此气体的容器倒扣在水中,通入标况下一定体积的 O2,恰好使气体完全溶于水中,则通入O2 的体积可能是 A.504mL B.168mL C.336mL D.224mL |
|
| 22. 推断题 | 详细信息 | ||||||||||
现有部分元素的性质与原子(或分子)结构的相关信息如表所示:
|
|||||||||||
| 23. 填空题 | 详细信息 |
|
(1)下列几组物质中,互为同位素的是_______,互为同素异形体的是_______,互为同系物的是_______,互为同分异构体的是_______,属于同种物质的是_______。(用序号填空) ①O2 和O3 ②35Cl 和 37Cl ③CH3CH3 和 CH3CH2CH3④  和 和 ⑤CH3(CH2)2CH3 和(CH3)2CHCH3 ⑤CH3(CH2)2CH3 和(CH3)2CHCH3(2)硫酸的性质有:A.高沸点;B.酸性;C.吸水性;D.脱水性;E.强氧化性。在下列硫酸的用途或化学反应中,硫酸可能表现上述的一个或者多个性质,试用字母填空: ①实验室干燥氢气_____; ②浓硫酸与金属铜的反应_____; ③浓硫酸使蔗糖变黑,且有刺激性气味的气体产生_____ (3)已知氯有 2 种常见同位素原子 35Cl、37Cl,氢有 3 种常见的同位素原子 H、D、T,氯气与氢气形成的氯化氢分子的相对分子质量可能有_____种。 (4)质量相同的 H2 16O 和 D2 16O 所含质子数之比为_____ (5)①CO2 ②CH3CH3 ③CaBr2 ④H2O2 ⑤NH4Cl ⑥AlCl3 ⑦NaOH ⑧NH3 ⑨Na2O2试用以上编号填空:既有极性键,又有非极性键的是_____;属于离子化合物的是_____; |
|
| 24. 实验题 | 详细信息 |
某化学兴趣小组利用以下各装置连接成一整套装置,探究氯气与氨气之间的反应。其中D 为纯净干燥的氯气与纯净干燥氨气反应的装置。 请回答下列问题: (1)连接好装置后,必需进行的一步实验操作是_____ (2)装置E 的作用是_____,橡胶管 k 的作用是_____ (3)装置F 中试管内发生反应的化学方程式 _____ (4)装置D 内出现浓厚的白烟并在容器内壁凝结,另一产物是空气的主要成分之一,写出该反应的化学方程式_____ (5)接入D 装置的两根导管左边较长、右边较短,目的是_____ (6)整套装置从左向右的连接顺序是(j)接______、______接(f) (g)接______ 、______接______ 、______接(a) |
|
| 25. | 详细信息 | |||||||||
|
燃煤的烟气中含有 SO2,为了治理雾霾天气,工厂采用多种方法实现烟气脱硫。 Ⅰ.(1)“湿式吸收法”利用吸收剂与 SO2 发生反应从而脱硫。下列试剂中适合用作该法吸收剂的是_____(填字母序号)。 a. 石灰乳 b.CaCl2溶液 (2)某工厂利用含 SO2 的烟气处理含Cr2O72-的酸性废水,吸收塔中反应后的铬元素以Cr3+形式存在,具体流程如下:  ①用 SO2 处理含铬废水时,利用了 SO2 的_____性。 ②吸收塔中发生反应的离子方程式为_____。 Ⅱ.石灰-石膏法和烧碱法是常用的烟气脱硫法。石灰-石膏法的吸收反应为Ca(OH)2+SO2= CaSO3↓+H2O。吸收产物亚硫酸钙由管道输送至氧化塔氧化,反应为2CaSO3+O2+4H2O =2CaSO4·2H2O。其流程如图: 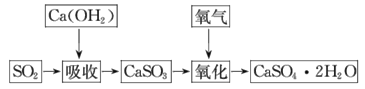 烧碱法的吸收反应为2NaOH+SO2=Na2SO3+H2O。该法的特点是氢氧化钠碱性强、吸收快、效率高。其流程如图:  已知:
|
||||||||||