沪教版化学初三第二学期《常用的金属和盐》测在线测验完整版
| 1. 选择题 | 详细信息 |
|
下列金属的活动性最弱的是 A. Mg B. Zn C. Cu D. Ag |
|
| 2. 选择题 | 详细信息 |
|
明代科学家宋应星所著的《天工开物》中。详细记述了金、铜、铁、镁等金属的开采和冶炼方法。记述的金属中金属活动性最强的是( ) A. 金 B. 铜 C. 铁 D. 镁 |
|
| 3. 选择题 | 详细信息 |
|
有关金属,有下列几种说法: ①黄铜合金比铜的硬度高; ②铁生锈是铁与水和氧气共同作用的结果; ③根据金属与稀硫酸反应的剧烈程度比较 Al、Zn、Fe 的活动性强弱; ④向含有 Cu(NO3)2 和 AgNO3 的混合溶液中加入 Fe 粉,得到的滤渣中一定含有 Ag,滤液一定有硝酸铁; ⑤向硝酸铜溶液中加入铝和铁,过滤,若往滤渣中加入盐酸,有气泡冒出,则滤渣中一定有铝和铜。 以上说法正确的个数是( ) A. 2 个 B. 3 个 C. 4 个 D. 5 个 |
|
| 4. 选择题 | 详细信息 |
|
属于化合反应的是( ) A.Na2O+H2O=2NaOH B.C2H6O+3O2 C.H2+CuO |
|
| 5. 选择题 | 详细信息 |
|
有甲、乙、丙三种金属,如果将甲、乙、丙分别投入到CuSO4溶液中,一段时间后, 甲、丙表面出现红色物质,乙没有明显现象;再将大小相同的甲、丙分别放到相同的盐酸中,甲、丙均产生气泡,但甲产生气泡的速度明显快于丙,则甲、乙、丙三种金属的活动性顺序是 A. 甲>丙>乙 B. 丙>乙>甲 C. 甲>乙>丙 D. 丙>甲>乙 |
|
| 6. 选择题 | 详细信息 |
|
下列关于金属的说法正确的是( ) A. 人类使用金属铝的年代早于铜、铁 B. 武德合金的熔点高,可用于制造保险丝 C. 将生锈的菜刀浸泡在食盐水中,可除去其表面的铁锈 D. “真金不怕火炼”表明金( Au)在高温条件下也很难与氧气反应 |
|
| 7. 选择题 | 详细信息 | |||||||||||||||
除去下列物质中的少量杂质所选的试剂正确的是 ( )
|
||||||||||||||||
| 8. 选择题 | 详细信息 |
下列实验中与下图相符合的是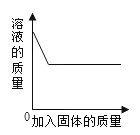 A. 向稀盐酸中加入碳酸钾粉末 B. 向稀硫酸中加入镁条 C. 向硝酸银溶液中加入铜粉 D. 向不饱和硝酸钾溶液加入硝酸钾晶体 |
|
| 9. 选择题 | 详细信息 | |||||||||||||||
将甲、乙、丙、丁四种物质放入一密闭容器中,在一定条件下发生反应,测得反应前后有关数据如下表所示,下列有关此反应的说法中正确的是
|
||||||||||||||||
| 10. 选择题 | 详细信息 |
|
物质的用途与性质密切相关.下列说法不正确是: A. 氮气常用作保护气,是由于氮气的化学性质稳定 B. 二氧化碳通常用于灭火,是由于二氧化碳不可燃、不助燃且密度比空气大 C. 氧化钙可做食品干燥剂,是由于氧化钙能与水反应 D. 因为铝的化学性质比较稳定,所以可用“银粉漆(铝粉)”涂在铁栏杆表面防锈 |
|
| 11. 选择题 | 详细信息 |
|
下列各项,括号中的物质是为了除去物质中的少量杂质所选用的试剂,其中除杂试剂 选用正确的是( ) A. CaCO3 中少量 CaO(稀 HCl) B. 铁粉中少量铜粉(H2SO4) C. CO2 中少量水蒸气(固体 NaOH) D. CO 中少量的CO2[Ca(OH)2] |
|
| 12. 选择题 | 详细信息 | |||||||||||||||
下列实验操作能达到实验目的是
|
||||||||||||||||
| 13. 填空题 | 详细信息 |
|
完成下列填空:①氮气②武德合金③青铜④干冰⑤肥皂水⑥氢气(填序号)。 (1)可作燃料的是_______; (2)制作保险丝的材料的是______; (3)常用于区分硬水与软水的是______; (4)可用来人工降雨的是____; (5)人类使用最早的合金_____; (6)常用作粮食瓜果保护气的是_______。 |
|
| 14. 填空题 | 详细信息 |
化学是以实验为基础的学科,根据以下两个实验回答下列问题: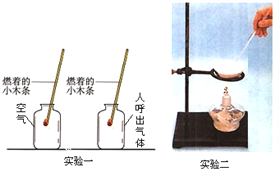 (1)实验一:将燃着的小木条同时伸入两个集气瓶中,观察到的现象是__________,通过该现象你得出的结论是_____________________________。 (2)实验二:该实验是粗盐中难溶性杂质的去除的实验中的步骤,该步骤中玻璃棒的作用是_________________________,实验应待________________时,停止加热。 |
|
| 15. 填空题 | 详细信息 |
|
请回答有关金属的问题。 (1)在Cu和Zn中,活动性较强的是_____________; (2)Cu与AgNO3溶液的反应中,__________离子变成了原子; (3)只用少量的盐酸、一支试管和锌、铜、铝,通过加入金属的顺序不同,也能验证这三种金属的活动性的强弱,则加入的顺序为______________________(假设每次的反应均反应完全)。 |
|
| 16. 推断题 | 详细信息 |
初中化学中的几种常见物质有如图所示的转化关系(部分反应物和生成物已略去),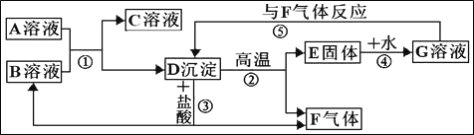 请回答下列问题: (1)A的化学式是_____。 (2)反应⑤的化学方程式为_____; (3)在四种基本反应类型中,如图未涉及到的反应类型是_____。 |
|
| 17. 填空题 | 详细信息 |
(4分)三瓶遗失标签的无色溶液分别是盐酸、氢氧化钠、氢氧化钙,为鉴别这三瓶溶液进行如下实验。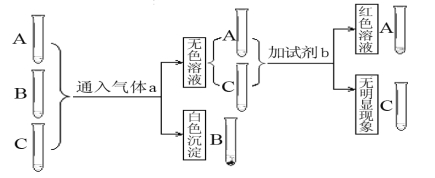 (1)①气体a的名称是 。 ②生成白色沉淀的化学方程式是 。 ③如果只用一种试剂来鉴别三种溶液,可选用的试剂是 。 (2)若遗失标签的是氢氧化钙、碳酸氢钠、盐酸三瓶溶液,鉴别时不需外加任何试剂,只需将其中的溶液①分别滴加到另外两种溶液②、③中,若实验现象是:一个有气泡,一个无明显现象,则①是___________。 |
|
| 18. 填空题 | 详细信息 |
把一定质量的锌粉投入到硫酸亚铁和硫酸铜的混合溶液A中,充分搅拌,过滤。回答下列问题。 (1)若向滤渣C中加入适量稀硫酸,有气体生成。滤渣C中一定有_____,滤液B中除水外,一定有_____。 (2)若向溶液A中加入过量的锌粉,写出向滤渣C中加入足量硫酸,发生的反应的化学方程式为_____、_____。 |
|
| 19. 实验探究题 | 详细信息 |
为了验证金属活动性强弱和验证质量守恒定律,同学们设计了如图所示的实验。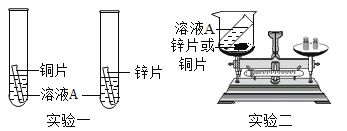 (1)利用实验一和实验二,既能验证铜、锌金属活动性强弱,同时能验证质量守恒定律,则溶液A可以是_____(填序号)。 a、稀硫酸 b、硝酸银溶液 c、氯化亚铁溶液 d、硫酸锌溶液 e、硫酸铜溶液 (2)利用以上试剂设计反应,验证铜和银的金属活动性,化学反应方程式为_____,现象为_____。 |
|
| 20. 计算题 | 详细信息 |
|
取50g一定溶质质量分数的Na2CO3溶液于烧杯中,逐滴加入BaCl2溶液至恰好完全反应,共消耗BaCl2溶液104 g。将沉淀过滤,称得烧杯中溶液的质量为144.15g。求: (1)生成的沉淀质量为_____g; (2)所用Na2CO3溶液的溶质质量分数_____。 |
|
| 21. 计算题 | 详细信息 |
AgNO3可用于电影胶片制作。现取含有NaNO3的AgNO3样品100g,在一定条件下让样品充分反应,只有AgNO3发生反应,得到固体69g,该过程中发生反应的化学方程式为:2AgNO3 2Ag+2NO2↑+O2↑。试计算: 2Ag+2NO2↑+O2↑。试计算:(1)AgNO3中N、O元素的质量比为_____。 (2)分解产生的混合气体中O2的质量。_____ (3)另取100g该样品和一定质量的NaCl固体全部溶解于142.5g水中得到含一种溶质的溶液,该溶液溶质的质量分数是多少?_____ |
|
最近更新



