滨州市2019年九年级化学下半年月考测验试卷带答案和解析
| 1. 选择题 | 详细信息 |
|
下列变化不属于化学变化的是:( ) A. 纸张燃烧 B. 蔗糖溶解 C. 食物腐烂 D. 铁钉生锈 |
|
| 2. 选择题 | 详细信息 |
|
浓盐酸浓硫酸敞口放置在空气中一段时间后,溶液质量变化为( ) A. 增加 减小 B. 减小 减小 C. 减小 增加 D. 增加 增加 |
|
| 3. 选择题 | 详细信息 |
要使如装置中的小气球鼓起来,则使用的固体和液体可以是( )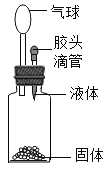 A. 硝酸铵和水 B. 铜和稀硫酸 C. 固体氢氧化钠和水 D. 氯化钠和水 |
|
| 4. 选择题 | 详细信息 |
下图是甲.乙.丙.丁四种常见金属与盐酸反应的比较示意图。以下说法错误的是( )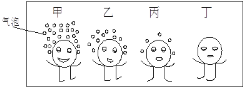 A. 如乙金属为Fe,则乙与盐酸反应的化学方程式为:2Fe+6HCl=2FeCl3+3H2↑ B. 金属甲.乙.丙与盐酸反应属于置换反应 C. 若乙是金属Al,则丙可能是Zn和Fe D. 四种金属的活动性强弱顺序为:甲、乙、丙、丁 |
|
| 5. 选择题 | 详细信息 |
|
下列各组气体中既能用浓硫酸干燥,又能用苛性钠干燥的是 ( ) A. H2、O2 B. CO 2、N2 C. SO 2、CO D. SO 2、CO 2 |
|
| 6. 选择题 | 详细信息 |
|
下列书写正确,且属于置换反应的是( ) A. Cu+2HCl= CuCl2+H2↑ B. 3Cu+ 2AlCl3= 2Al +3CuCl2 C. NaOH+HCl=NaCl+H2O D. 2Al+6HCl=2AlCl3+3H2↑ |
|
| 7. 选择题 | 详细信息 |
|
推理是化学学习中常用的思维方法.下列推理正确的是 A. 酸能使紫色石蕊溶液变红.通入CO2后的紫色石蕊溶液变红,所以CO2是酸 B. 某无色气体混入空气后点燃爆炸,可证明该气体一定是H2 C. 在同一化合物中,金属元素显正价,所以非金属元素一定显负价 D. 饱和溶液恒温蒸发时,有晶体析出,溶质质量减小,所得溶液仍为饱和溶液,所以溶质的质量分数不一定减小 |
|
| 8. 选择题 | 详细信息 | ||||||||||||||||||||
除去下列物质中的少量杂质,所选试剂或方法正确的是( )
|
|||||||||||||||||||||
| 9. 选择题 | 详细信息 |
|
下列四个图象分别对应四种操作过程,其中正确的是( ) A. 双氧水分解 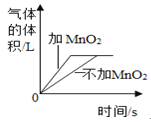 B. 向饱和氯化钠溶液中加水稀释  C. 常温下,相同质量的锌和铁分别与足量的溶质质量分数相同的稀硫酸反应 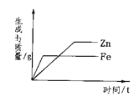 D. 将一定质量的硝酸钾不饱和溶液恒温蒸发水份,直至有少量晶体析出  |
|
| 10. 填空题 | 详细信息 |
|
铁是生活中常见的一种金属。 (1)生铁是常用的合金,生铁属于_______(填“纯净物”或“混合物”)。 (2)铁块可以铸成铁锅,是利用了铁的_________性。 (3)铁制品与__________接触易生锈(填化学式)。 (4)铁生锈可以用盐酸除去,请用化学方程式解释其除锈原理:_______________ (5)工业上用赤铁矿(主要成分是Fe2O3)和一氧化碳炼铁,该反应的化学方程式为:_______ |
|
| 11. 填空题 | 详细信息 |
如图为甲、乙、丙三种物质的溶解度曲线,据下图回答: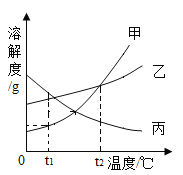 (1)t1℃时,甲、乙、丙三种物质的溶解度由大到小顺序是________(用“>”、“<”或“=”表示) . (2)将t2℃时相等质量的三种物质的饱和溶液分别降到0℃,析出溶质最多的是_________, (3)当甲中含有少量乙时,为了得到纯净的甲,可采用____________的方法. (4)若将t2℃三种物质的饱和溶液分别降到t1℃时,则三种溶液中溶质的质量分数由大到小的顺序是_________(用“>”、“<”或“=”表示) . |
|
| 12. 简答题 | 详细信息 |
|
化学课上,周老师向我们展示了两瓶无标签的溶液,说:“它们分别是稀盐酸和氢氧化钠溶液。请同学们设计不同的方案,然后动手实验: (1)你认为滴加什么试剂加以区分_________ (2) 在探究过程中,要注意安全,因为稀盐酸和氢氧化钠溶液都具有___________(填“酸性” “碱性”或“腐蚀性”)。 (3)小维同学认为不能将CO 2分别通入这两种溶液,通过观察现象加以区分,请帮助他说明理由:____________ |
|
| 13. | 详细信息 |
|
洗衣粉是一种合成洗涤剂,其水溶液能使酚酞变红。洗衣粉的主要成分是表面活性剂,它在洗涤过程中用来疏松并去除污垢,有很强的起泡能力。洗衣粉几乎成为现代家庭必备的洗涤用品。但是,消费者在洗衣粉的使用方面还存在着一些误区。 误区一:泡沫越多去污力越强 洗衣粉中的泡沫主要来自于表面活性剂,洗衣粉加的多产生泡沫就会多,但并不是洗衣粉加得越多越好。当洗衣粉中的表面活性剂在水中达到一定浓度,溶液的表面活性达到最大值以后,去污力就不再随着洗衣粉质量的增加而增强,反而有减小的趋势。洗衣粉加过量,不仅影响去污力,还会因溶液中碱性的增强而对衣物纤维有损伤。另外,大量洗衣粉附着在衣服上,泡沫多,不易漂净,残留在衣物上的成分还会对皮肤造成伤害。 误区二:水温越高去污力越强 水温对洗衣粉的洗涤效果确实有影响,在温水中比冷水中好,温水可以使更多的洗衣粉溶于水中,表面活性剂能发挥更大功效,从而达到洗涤去污的效果。但水温也不是越高越好,温度太高,会破坏其中的一部分辅助清洁成分,反而影响去污效果。另外,高温还会使衣物上的某些污物凝固于织物纤维之上,从而更难以洗净。经研究测定,洗衣粉清洗衣物时,水温以30℃至60℃为宜。 在1000g清水中加入某品牌洗衣粉,其去污能力的测定结果如下图所示。 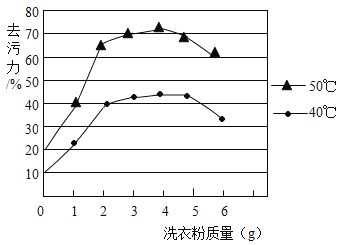 误区三:洗衣粉可以洗涤所有衣物洗衣粉更适合洗涤棉、麻、化纤及混纺织物,不适合洗涤毛、丝绸等衣物。由于毛、丝绸等衣物中含蛋白质,会被碱性物质破坏。另外,婴儿衣物及成人贴身衣服也不要用洗衣粉洗涤。 看完以上关于洗衣粉认识误区的解读,相信你已经学到了一些正确使用洗衣粉的方法。 依据文章内容回答下列问题。 (1)洗衣粉溶于水后,溶液呈________(填“酸性” 或“碱性”)。 (2)从图像可知,若在1000g清水中加入该品牌洗衣粉,当洗衣粉与清水的质量比超过_________(整数比)时,洗涤去污能力开始明显下降。 (3)下列有关洗衣粉说法中正确的是_________(填序号)。 A 洗衣粉主要成分是表面活性剂 B 洗衣粉用量越多去污能力越强 C 用洗衣粉洗衣服时,应尽量用清水将其漂洗干净 D 洗衣粉适合洗涤毛和丝绸等衣物,不适合洗涤棉、麻、化纤及混纺织物 (4)“水温越高洗衣粉去污能力越强”说法不正确的理由是_________(答出一点即可)。 (5)影响洗衣粉去污能力的因素有_________。 |
|
| 14. 科学探究题 | 详细信息 |
|
某化学实验小组同学将铁粉投入硫酸铜溶液中,发现生成红色固体物质的同时有较多的气泡放出.这一现象激发起同学们的探究欲望,生成的是什么气体? (提出猜想)放出的气体可能是SO2、O2、H2.提出猜想的依据是:_________________ (查阅资料)SO2与二氧化碳化学性质相似,也能使澄清石灰水变浑浊,生成CaSO3, 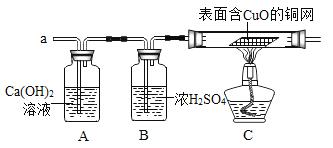 (方案设计)依据上述猜想,实验小组同学分别设计了如下方案: (1)甲同学认为是O2,则检验方法是____________________ . (2)乙同学认为是SO2,则只需将放出的气体通入盛有澄清石灰水中,看澄清石灰水是否变浑浊.写出SO2与澄清石灰水反应的化学方程式 __________________________ . (3)实验小组同学合作设计了如下组合实验方案,排除和验证猜想的气体: ①如果撤去B装置,直接连接A,C装置进行实验。你认为可能导致的后果是___________ ②实验开始时,应先将收集到的气体从a处通入一段时间后,再点燃 C 处酒精灯。这样操作的目的是_________________________。 (实验探究)实验过程中发现 A 装置中溶液不变浑浊, C 装置中表面含CuO的铜网由黑色变为光亮的红色,试管壁上有水滴生成 (4)(实验结论)铁粉与硫酸铜溶液反应时,产生的气体是_______ (5)(思维拓展)①由上述实验可以推出,硫酸铜溶液中可能含_______物质 ②碱的性质决定了保存方式,例如氢氧化钠密封保存一方面是由与它要与二氧化碳作用而变质,另一方面是由于_______________________ |
|
最近更新



