2019届九年级下半期中考二模化学专题训练(江苏省泰州市姜堰区)
| 1. | 详细信息 |
|
2019年3月,姜堰区中小学开展了“打赢蓝天保卫战”活动。下列行动不利于“保卫蓝天”的是 A. 尽量低碳出行 B. 露天焚烧垃圾 C. 使用清洁能源 D. 积极植树造林 |
|
| 2. | 详细信息 |
|
下列属于化学变化的是 A. 工业制氧气 B. 盐酸挥发 C. 石油分馏 D. 粮食酿醋 |
|
| 3. | 详细信息 |
|
下图为“中国节能”标志的是 A.  B. B.  C. C.  D. D.  |
|
| 4. | 详细信息 |
|
下列物质的用途利用其物理性质的是 A. 干冰用于人工降雨 B. 铁粉用作食品吸氧剂 C. 氧气用于医疗供氧 D. 小苏打治疗胃酸过多 |
|
| 5. | 详细信息 |
|
下列实验操作正确的是 A. 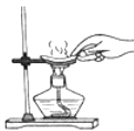 移走蒸发皿 B. 移走蒸发皿 B. 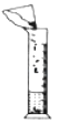 溶解固体 溶解固体C. 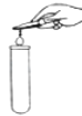 加入大理石 D. 加入大理石 D. 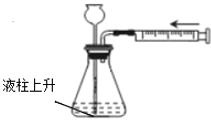 检查装置的气密性 检查装置的气密性 |
|
| 6. | 详细信息 |
|
下列物质属于纯净物的是 A. 酒精 B. 不锈钢 C. 矿泉水 D. 加碘盐 |
|
| 7. | 详细信息 |
|
下列说法正确的是 A. 铜绿加热后颜色变红,并生成有刺激性气味的气体 B. 空气中二氧化碳含量增加,导致了酸雨的形成 C. 洗洁精有乳化作用,可用于洗去碗筷上的油污 D. 活性炭可将硬水软化 |
|
| 8. | 详细信息 |
|
下列有关化学用语表示正确的是 A. 两个亚铁离子:2Fe3+ B. 氧分子:O C. 保持二氧化碳化学性质的最小微粒:CO2 D. 钠原子的结构示意图: |
|
| 9. | 详细信息 |
|
下列选项的物质间转化均能一步实现的是 A. Fe B. Na2CO3 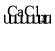 NaCl NaCl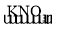 NaNO3 NaNO3C. C 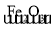 CO2 CO2D. H2O2 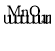 O2 O2 |
|
| 10. | 详细信息 | ||||||||
下列对主题知识的归纳,完全正确的一组是
|
|||||||||
| 11. | 详细信息 |
氨催化氧化是制硝酸的主要反应之一。该反应的微观示意图如图。下列说法正确的是 A. 反应前后原子的种类不变 B. 乙的相对分子质量为32g C. 该反应中共有三种氧化物 D. 生成的丙与丁的分子个数比为1:2 |
|
| 12. | 详细信息 |
甲、乙两种物质(不含结晶水)的溶解度曲线如下图所示,下列叙述正确的是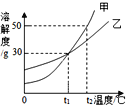 A. 甲和乙的溶解度相等且均为30g B. 甲物质中混有少量的乙,用蒸发结晶的方法进行提纯 C. t1℃时,乙的饱和溶液中溶质与溶剂的质量比为3:7 D. 将t2℃150g甲的饱和溶液降温到t1℃,有20g固体析出 |
|
| 13. | 详细信息 |
|
下列图像能正确反映变化关系的是 A.  向等质量相同形状的镁片和锌片中分别加入相同浓度的稀硫酸至过量 向等质量相同形状的镁片和锌片中分别加入相同浓度的稀硫酸至过量B. 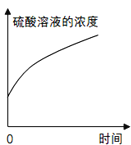 盛有浓硫酸的试剂瓶敞口露置于空气中 盛有浓硫酸的试剂瓶敞口露置于空气中C. 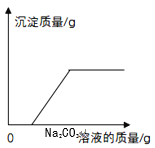 CaCl2和HCl的混合溶液中加入Na2CO3溶液至过量 CaCl2和HCl的混合溶液中加入Na2CO3溶液至过量D. 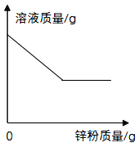 Cu(NO3)2溶液中加入锌粉至过量 Cu(NO3)2溶液中加入锌粉至过量 |
|
| 14. | 详细信息 | |||||||||||||||
下列实验操作不能达到实验目的的是
|
||||||||||||||||
| 15. | 详细信息 |
利用数据传感技术可以比较不同形状的碳酸钙和稀盐酸反应的速率。倾斜锥形瓶,使小试管中的稀盐酸流入瓶中与碳酸钙反应,测得瓶中气压随时间变化如图所示,下列选项正确的是 A. 该实验要求装置的气密性良好,才能保证数据的准确性 B. 对比分析a、b点可知,曲线①表示块状石灰石与稀盐酸反应 C. 完全反应后碳酸钙粉末产生的二氧化碳质量更大 D. 对比分析c、d点可知,碳酸钙粉末与稀盐酸反应速率更快 |
|
| 16. | 详细信息 |
|
化学与人类生活、生产息息相关。 (1)米饭、苹果、面包、瘦肉等食物中,主要为人体提供蛋白质的食物是_____。 (2)在酒厂附近常可以闻到酒味,请从微观角度加以解释_____。为缓解能源危机,可推广使用车用乙醇汽油,乙醇(C2H6O)完全燃烧的化学方程式为_____。天然气的主要成分是_____。(填化学式) (3)科学家利用太阳能产生激光分解海水,反应方程式为:2H2O (4)高铁车头的玻璃是用无机玻璃、树脂、塑料等黏合而成,可耐强大的撞击力,这种玻璃属于_____。(选填“复合材料”、“合成材料”、“金属材料”) |
|
| 17. | 详细信息 |
实验室制取气体需要的一些装置如下图所示: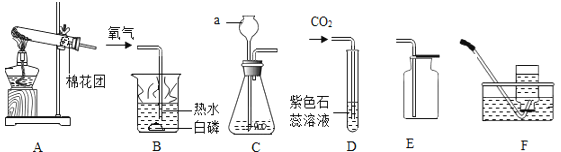 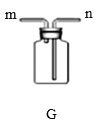  (1)写出标有序号的仪器名称:a_____。 (2)实验室用高锰酸钾制取并收集干燥的氧气,选择的装置组合为_____,反应方程式为_____。 (3)连接A、B装置,观察到B装置热水中的白磷燃烧,该事实说明燃烧需要的条件之一是_____。 (4)实验室利用C、D装置制取CO2并验证性质。C中发生反应的方程式为_____,D中观察到的实验现象为_____。 (5)实验室加热氯化铵和熟石灰的固体混合物制取氨气,该反应的化学方程式为_____,已知氨气极易溶于水且密度小于空气,若用G装置收集,气体应从_____接口进入。 (6)用H装置可以制造“化学喷泉”。将胶头滴管中的KOH溶液挤进圆底烧瓶时,很快看到长导管顶端产生“喷泉”现象。若将烧瓶内的CO2换成下列四种气体中的_____仍可产生“喷泉”现象。(填编号) A SO2 B H2 C CO D HCl |
|
| 18. | 详细信息 |
|
电解饱和食盐水制氢氧化钠,反应方程式为:2NaCl+2H2O (1)NaOH的俗名是_____,气体A的化学式为_____。 (2)气体B的水溶液的一种用途为_____。 (3)向蓝色沉淀D中加入B的溶液,反应的方程式为_____,伴随的现象_____。 (4)气体A和固体E加热时发生反应的方程式为_____,属于_____反应。(填基本反应类型) |
|
| 19. | 详细信息 | |||||||||
|
某化学兴趣小组在一次实验活动中发现镁、钠都能在纯净的二氧化碳气体中燃烧,反应后冷却,瓶底除了有黑色颗粒,瓶壁上还都附着白色物质。经检验,黑色颗粒是碳。他们对镁、钠在二氧化碳气体中燃烧后生成的白色物质分别进行了如下探究: (探究问题一)镁在纯净的二氧化碳中燃烧生成的白色物质是什么? 同学们首先排除了是Mg(OH)2的可能性,理由是_____。 (做出猜想)白色固体可能是①MgO、②MgCO3、③_____。 (进行实验)取少量白色固体,加入足量的稀盐酸,观察到_____现象,猜想①正确。 (实验结论)镁在二氧化碳中燃烧的化学方程式是_____。 (探究问题二)钠在纯净的二氧化碳中燃烧生成的白色物质是什么? (查阅资料)信息1:钠能与冷水发生剧烈反应。 信息2:Na2O+H2O=2NaOH (实验设计)甲组方案:
|
||||||||||
| 20. | 详细信息 |
|
(1)若用98%的浓硫酸(密度为1.84g/mL)配制500g19.6%的稀硫酸,需要浓硫酸_____mL(结果精确到0.1)。 (2)向100g碳酸钠溶液中慢慢滴加(1)中配制的稀硫酸,并用玻璃棒不断搅拌,测得pH的变化情况如图。玻璃棒的作用是_____,B处溶液中的溶质有_____。 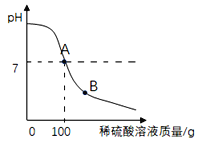 当稀硫酸和碳酸钠溶液恰好完全反应时,求所得溶液中溶质的质量分数。_____(写出详细计算过程,结果精确到0.1%) |
|




