六安市2019年九年级化学上半年期中考试同步练习
| 1. 选择题 | 详细信息 |
|
六安是一座富有悠久历史文化的城市,勤劳智慧的六安人民在生产生活中创造了无数的瑰宝,下列工艺中发生化学变化的是( ) A. 采摘茶叶 B. 煎蒿子粑粑 C. 板栗切口 D. 葛根磨粉 |
|
| 2. 选择题 | 详细信息 |
|
大别山脉山青水秀,孕育着无数江淮儿女。我们在享受自然美景、呼吸新鲜空气时,更要保护自然环境的可持续发展。下列做法,符合这一观念的是( ) A. 工业废水只要是无色透明的就直接排放 B. 大量使用农药和化肥,提高产量 C. 高污染企业由城市搬到山 D. 生活污水集中处理后排放 |
|
| 3. 选择题 | 详细信息 |
|
规范的实验操作是实验成功的保证。下列实验操作正确的是( ) A. 检验CO2气体  B. 量取8.6mL液体 B. 量取8.6mL液体 C. 检查装置气密性 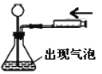 D. 滴加液体 D. 滴加液体 |
|
| 4. 选择题 | 详细信息 |
|
霍山石斛是我国特有,国家一级保护植物,主要产于我市霍山县,大多生长在云雾缭绕的悬崖峭壁崖石缝隙间和参天古树上。霍斛富含多糖、氨基酸和石斛碱(C16H25NO2)、等十多种生物碱。下列有关石斛碱说法正确的是( ) A. 石斛碱有四个元素组成 B. 每个石斛碱含有44个原子构成 C. 石斛碱中碳氧元素质量比为6:1 D. 石斛碱中氢元素质量分数最高 |
|
| 5. 选择题 | 详细信息 |
|
用“王水”(浓盐酸与浓硝酸的混合物)溶解某金属M后得到一种物质:HMCl4,则下列物质所含M元素的化合价与HMCl4不同的是( ) A. M2O3 B. M2Cl3 C. M(NO3)3 D. M2(SO4)3 |
|
| 6. 选择题 | 详细信息 |
经过几代地质人的苦苦探索和不懈追求,我省首个“世界级”金属矿床,终在金寨县沙坪沟揭开神秘面纱。沙坪沟巨型“斑岩型”钼矿探明钼金属量220万吨以上,储量亚洲第一、世界第二。根据如图钼在元素周期表中信息,下列说法正确的是( )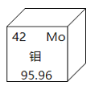 A. 钼的原子质量是95.96 B. 钼原子中有42个中子 C. 钼原子核外有42个电子 D. 钼原子容易失去电子形成阴离子 |
|
| 7. 选择题 | 详细信息 |
|
逻辑推理是一种重要的化学思维方法,以下逻辑合理的是( ) A. 离子是带电荷的微粒,所以带电荷的微粒一定是离子 B. CO和CO2的组成元素相同,但它们的化学性质不同 C. 分子可以构成物质,所以物质都是由分子构成的 D. 粒子间有间隔,通常两种液体混合总体积变小,所以任何液体混合总体积不会变大 |
|
| 8. 选择题 | 详细信息 |
如图是一定条件下某反应的微观过程,下列说法中不正确的是( ) A. 反应物分子个数比为1:1 B. 该反应属于分解反应 C. 化学反应前后原子种类和数目不变 D. 生成物是两种物质 |
|
| 9. 选择题 | 详细信息 |
|
建立模型是学习化学的重要方法,下列有关模型正确的是( ) A. 原子结构模型  B. 化合反应和分解反应关系模型 B. 化合反应和分解反应关系模型 C. 物质分类模型  D. 自然界氧循环模型 D. 自然界氧循环模型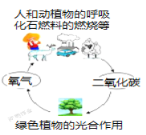 |
|
| 10. 选择题 | 详细信息 |
一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如表所示,下列说法正确的是( ) A. W由碳、氢、氧三种元素组成 B. 参加反应的W和氧气的质量之比2:5 C. X的值为10 D. W可能是氧化物 |
|
| 11. 填空题 | 详细信息 |
|
空气是一种非常宝贵的资源。 (1)氮气是生产化肥的重要原料。空气中氮气的体积分数为_______。 (2)目前未计入空气污染指数监测项目的有______(填字母)。 A.一氧化碳 B.二氧化硫 C.可吸人颗粒物 D.二氧化碳 (3)化工企业的安全生产至关重要,如果合成氨工厂出现氨气泄漏,方圆几里市民都会在空气中闻到刺激性气味,请从分子原子的角度解释__________________________________。 (4)硝酸工厂排放的尾气中常含有NO、NO2等有害气体,可用氢氧化钠溶液来吸收:NO+NO2+2NaOH=2X+H2O ,X的化学式为_________。 |
|
| 12. 填空题 | 详细信息 |
李老师去佛子岭水库游玩时,用瓶装了一些水库中的水。我校化学兴趣小组同学在老师的指导下,按下图流程进行水的净化实验。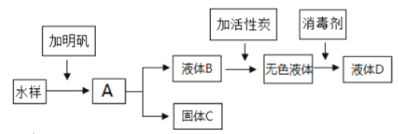 请回答下列问题: (1)水样中加入明矾后的A操作是_____________;A操作需要的玻璃仪器有玻璃棒、烧杯和________,A操作后的液体依然浑浊,可能的原因是(试写一点错误的实验操作)_______________________________________; (2)向滤液中加入活性炭,利用其________________的结构,可吸附水样中的色素和异味; (3)硬水给生活和生产带来很多麻烦,生活中可鉴别水样是否为硬水的物质是_________; (4) 水是生命之源,请写出一个你生活中爱护水资源的做法__________________________。 |
|
| 13. 实验探究题 | 详细信息 |
下图所示为实验室常用的实验装置: 据此回答下列问题: (1)写出带标号仪器的名称:②_______________; (2)常温下,实验室制取并收集较纯净氧气选择的装置组合是______(填序号,下同),化学方程式为___________________________________,其基本反应类型是_____________。 (3)F装置可用来测量生成的CO2气体的体积,其中在水面上放一层植物油的目的是___________. (4)某同学在实验室用大理石与一定浓度盐酸制取二氧化碳,发现产生气体的速率太快,请你分析并写出可能的原因_______________________________,实验室检验二氧化碳的反应方程式是____________________________。 |
|
| 14. 科学探究题 | 详细信息 |
|
小华同学进行了木炭在氧气中的燃烧实验,对燃烧后的产物产生了浓厚的兴趣。 (提出问题)木炭在一定量的氧气中燃烧产物是什么? (作出假设)假设1:产物是CO2 ; 假设2:产物是CO ; 假设3:产物是___________________; (设计实验)小华同学在老师的帮助下设计如下图所示流程(浓硫酸是干燥剂,不与其它物质反应),进行实验,请解释相关问题: 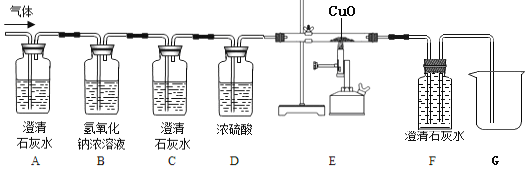 (1)按上面连接好装置,在装入药品之前,必须进行的操作是______________________; (2)A装置的作用是_________________________; (3)B装置的作用是吸收除去二氧化碳,若C装置中澄清石灰水无明显变化,则说明B装置已完全除去二氧化碳; (得出结论)根据设计意图,观察到______________________________(填写实验现象)时,得出假设3成立;写出装置E中反应的化学方程式:___________________________。 (交流与反思)有同学认为该装罝需要添加尾气处理装置,你认为是否需要并说明理由______________________________________________________。 |
|
| 15. 科学探究题 | 详细信息 | ||||||
|
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验。 (1)请写出镁条与氧气反应的化学方程式________________________________。 (2)小明发现燃烧产物的质量大于反应物镁条的质量,认为这个反应不遵循质量守恒定律。我________(“同意”或“不同意”)小明的观点,因为___________________________。 (3)小红按下图装置改进实验,验证了质量守恒定律,却发现产物中还有少量黄色固体。  (提出问题)黄色固体是什么呢? (查阅资料)①氧化镁为白色固体;②镁能与氮气剧烈反应生成黄色的氮化镁(Mg3N2)固体;③氮化镁可与水剧烈反应产生氨气,该气体能使湿润的红色石蕊试纸变蓝。 (做出猜想)黄色固体是Mg3N2 (实验探究)请设计实验,验证猜想
|
|||||||
| 16. 计算题 | 详细信息 |
|
将氯酸钾与二氧化锰的固体混合物15.5克装入大试管加热,完全反应后固体剩余物的质量为10.7克。求: (1)生成氧气的质量?___________________________ (2)混合物中氯酸钾的质量?___________________________ |
|
最近更新



