2019届九年级下册中考一模化学题免费试卷(安徽省合肥市蜀山区)
| 1. | 详细信息 |
|
宣纸是中国传统的古典书画用纸,原产于安徽省宜城泾县,故称“宣纸”。下列制作宣纸的过程中主要发生化学变化的是: A. 选材  B. 蒸煮  C. 捞纸  D. 干燥  |
|
| 2. | 详细信息 |
2019年3月6日合肥出现了严重雾霾天气。雾霾中的微粒容易进入气管,可引发呼吸系统疾病,雾霾中的有害物质还易引发心脑血管疾病。下列措施不能减轻或防治空气污染的是: A. 多使用共享自行车和地铁出行 B. 开发、使用太阳能路灯照明 C. 建筑工地和路面及时酒水降尘 D. 发展特色烧烤促进地方旅游发展 |
|
| 3. | 详细信息 |
下图A、B分别是元素在元素周期表中提供的部分信息和原子结构示意图,据图分析得出的下列结论中错误的是: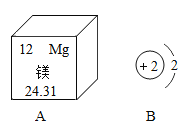 A. 依据电子排布两种元素有相似化学性质 B. 原子A在化学反应中易失电子成阳离子 C. 原子A的核电荷数和核内质子数均为12 D. 元素B组成的单质具有稳定的化学性质 |
|
| 4. | 详细信息 |
|
下列图示实验基本操作正确的是: A. 检查装置气密性 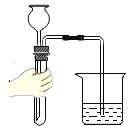 B. 称氢氧化钠固体 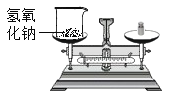 C. 过滤浑浊液 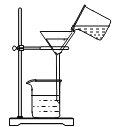 D. 铁丝在氧气中燃烧  |
|
| 5. | 详细信息 |
下图是在密闭容器中发生的物质变化过程,有关该过程的下列说法错误的是: A. 变化Ⅰ前后元素的化合价都没有发生变化 B. 用A中是混合物图B、C中是纯净物是化合反应 C. 引起Ⅱ和Ⅲ相互转化可能的原因是温度变化 D. 变化Ⅰ的化学反应属于基本反应类型 |
|
| 6. | 详细信息 |
|
归纳法是学习化学的一种重要方法。下列图示有错误的是: A. 此矿物燃料  B. 常见的干燥剂  C. 能与碱反应的物质  D. 溶液间的关系  |
|
| 7. | 详细信息 |
|
合肥生产的江淮新能源汽车用铁离子电池作动力即电池正极活性物质采用磷酸铁锂,这种电池具有容量足、功率大、内阻小、寿命长的优点。磷酸铁锂的化学式为LiFePO4,磷酸根离子的符号为PO43-,下列有关说法正确的是: A. 磷酸铁锂中铁元素的化合价为+2  B. 磷酸铁锂中含有4个氧原子 C. 磷酸铁锂中四种元素的个数比为1:1:1:4 D. 磷酸铁锂是属于氧化物 |
|
| 8. | 详细信息 |
如图所示进行有关碳及其氧化物的性质实验,错误的说法是: A. 玻璃管内的炭粉减少、氧化铜由黑变红 B. 甲处发生的反应是一个典型的吸热反应 C. 该装置的不足之处是没有进行尾气处理 D. 丙处的试管可以防止液体倒吸入玻璃管 |
|
| 9. | 详细信息 |
利用右图装置探究氧气的质量分数对燃烧的影响。点燃蜡烛后立即塞紧橡皮塞,待蜡烛熄灭后,将滴管中的水全部滴入集气瓶中,铝盒中的白磷立即燃烧。左图是版中①二氧化碳和②氧气的含量随时间变化的图象。下列有关说法错误的是: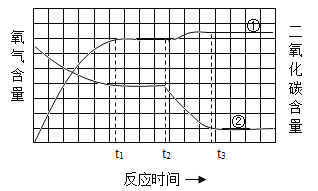 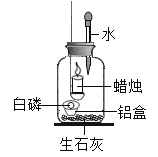 A. 在t1至t2时间段内蜡烛已熄灭而白磷还没有开始燃烧 B. 在t1至t3时间段气体含量的变化是因为磷燃烧消耗氧气生成固体 C. 该实验证明了不同物质的燃烧对氧气的质量分数需求不同 D. 该实验证明了蜡烛燃烧生成的二氧化碳气体仍能支持白磷的燃烧 |
|
| 10. | 详细信息 |
如图是甲、乙两种固体物质的溶解度曲线,下列说法错误的是( )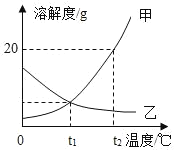 A. 甲中含有少量的乙可以采用降温结晶的方法提纯甲 B. 将t1℃甲、乙的饱和溶液升温至t2℃时,乙溶质质量分数变小 C. t2℃时,甲饱和溶液中溶质的质量分数比乙饱和溶液大 D. t2℃时,等质量的甲、乙两种物质配饱和溶液,甲溶液质量大 |
|
| 11. | 详细信息 |
打火机因其经济、环保而被人们广泛使用,右图是打火机的结构图,使用的燃料丁婉(C4H10)是一种易燃,无色,容易液化的气体。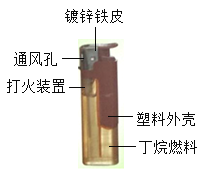 (1)在铁表面镀锌除了美观外,还能起到隔绝氧气和__________的作用而防止铁生锈,铁锈主要成分的化学式是______________。 (2)使用打火机时,用力按下打火装置上的按钮,打火装置产生电火花将气体点燃,从分子的角度解释丁烷液体喷出后变成气体的原因是____________________________________. (3)打火机上有通风孔,说明燃烧的条件之是_________________________,丁烷在氧气中充分燃烧的生成物是_______________和_________________________. |
|
| 12. | 详细信息 |
活泼金属可以和酸反应生成氢气,现在利用如图所示装置制取氢气,塑料片上放有足量锌粒,从漏斗中加入稀盐酸。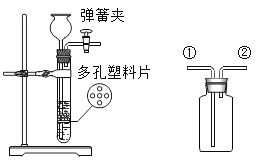 (1)该气体发生装置的优点是__________________,收集氢气可以从导管__________通入(填序号),点燃瓶中氢气前应进行的操作是____________________________________. (2)锌粒和稀盐酸刚接触时没有气泡产生,过会才产生大量气泡其原因可能是_________________________. (3)该气体发生装置一般不用于过氧化氢溶液和二氧化锰制氧气,其原因是__________________________,过氧化氢溶液和二氧化锰制氧气的化学方程式是____________________________________. |
|
| 13. | 详细信息 |
亚硫酸钠是种常见食品添加剂,亚硫酸钠在加热条件下可以和酸反应生成氧化硫气体。为检验某食品中亚硫酸钠的含量(以1kg样品生成的SO2质量计),某研究小组设计了如下实验流程: (1)为防止煮沸时发生暴沸,可以先向烧瓶中加入___________________________.在实验装置中先通入 (2)写出氢氧化钠溶液吸收SO2的化学方程式:_______________________________________________. (3)要得到SO2的质量,实验中需要称量反应前碱液的质量和_____________的质量。 (4)若用盐酸代替稀硫酸处理样品,则对实验结果的影响是_____________(填“偏高”、“偏低”或“无影响”),这是因为盐酸具有_____________性。 |
|
| 14. | 详细信息 |
铝是重要的轻金属,广泛应用于航空、电讯和建筑等领域。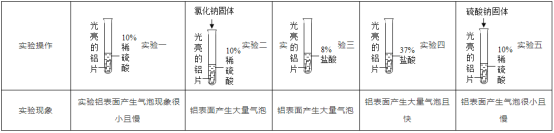 (1)依据金属的活动性顺序,铝的金属活动性比锌__________.但是将铝片和锌粒分别投入稀硫酸中,铝片表面产生的气泡却比锌粒少而慢。为了探究影响铝与酸反应速率的因素,振兴同学用相同质量、相同形状、除去氧化膜的铝片设计如图所示实验。 (2)写出实验中发生反应的化学方程式_______________________________________. (3)比较实验三、四说明铝与酸反应产生氢气的速率,与_____________________有关. (4)比较实验一、二说明铝与酸反应产生氢气的速率,可能与_________、_________(填粒子符号)、与和温度、金属与酸的接触面积等各种因素有关。 (5)比较实验一、二、五可以得出的结论是____________________________________. |
|
| 15. | 详细信息 |
|
中和反应在工农业生产和生活中有有泛的应用。某学生课外兴趣小组对中和反应进行研究。 (实验一)对于没有明显实验现象的中和反应,如稀盐酸与稀氢氧化钠溶液的反应,要证明它们之间确实发生了化学反应,可通过如下实验来进行。 将稀盐酸逐滴匀速加入一定量的稀氢氧化钠溶液中,用数字化仪器对反府过程中溶液的pH、温度进行实验测定,得到的曲线如图、如图所示中。 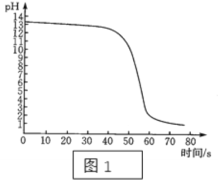 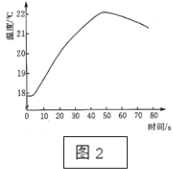 如图、如图均能证明中和反应发生了,如图能证明中和反应的判断依据是________________________________。由如图还能得出的其他结论是____________________________________。 (实验二)取少量难溶的氢氧化镁置于试管中加水振荡,得到浑浊液,再加入稀盐酸,若观察到现象_____,就可说明反应已经发生。该反应的化学方程式是____________________________________。 (实验反思)在敞口久置的氢氧化钠溶液中加入盐酸后,意外发现有气泡产生,同学们认为产生意外现象是因为______________________________而变质,变质后的物质和盐酸反应生成了___________气体。 (实验三)用白色无水硫酸铜粉末证明酸与碱之间能发生中和反应。 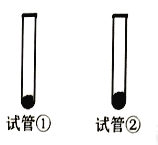 (1)在试管①和②中加入等质量的无水硫酸铜粉末,并在试管②里加入一些固体氢氧化钠和无水醋酸与无水硫酸铜粉末混合,段时间后试管②中无水硫酸铜粉末先变蓝,说明有水生成,从而证明中和反应发生了。 (2)小艺认为上述对照试验不能证明酸与碱发生了中和反应,小艺的理由是________________________________________________.你认为应怎样改进试验?______ (实验四)利用如图所示的原理来证明酸与碱可以发生中和反应。 (1)在盛有10mL浓硫酸的烧杯中倒入5mL氢氧化钠溶液,溶液温度迅速上升,由此证明硫酸与氢氧化钠发生了中和反应。小涵认为该实验不能证明硫酸与氢氧化钠发生了反应,小涵的理由是___________________. (2)该实验可能造成的危害是_____________________________________________. |
|
| 16. | 详细信息 |
|
电石主要成分是碳化钙(CaC2),是化学工业的基本原料。碳化钙可以和水反应生成乙炔 (CaC2)气体:CaC2+2H2O=Ca(OH)2+C2H2 |
|
最近更新



