甘肃省武威第六中学2020届高三下期第三次诊断考试理科综合化学免费试卷
| 1. 选择题 | 详细信息 |
|
化学与生产、生活及社会发展密切相关,下列有关说法不正确的是( ) A. “血液透析”和“静电除尘”利用了胶体的不同性质 B. 把石灰浆喷涂在树干上可消灭树皮上的过冬虫卵 C. 酸性重铬酸钾用于检查酒驾是利用其强还原性 D. 在食品袋中放入盛有硅胶和铁粉的透气小袋,可防止食物受潮、氧化 |
|
| 2. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的数值,下列有关说法正确的是 A.60克的乙酸和葡萄糖混合物充分燃烧消耗O2分子数为2NA B.5.8g熟石膏(2CaSO4·H2O)含有的结晶水分子数为0.04NA C.把4.6g乙醇完全氧化变成乙醛,转移电子数为0.1NA D.实验室制取氧气方法有多种,制取1molO2转移电子数均是4NA |
|
| 3. 选择题 | 详细信息 | ||||||||||||||||||||
下列根据实验操作和实验现象所得出的结论中,正确的是
|
|||||||||||||||||||||
| 4. 选择题 | 详细信息 |
|
短周期主族元素X、Y、Z、M 的原子序数依次递增,四种原子的最外层电子数之和为20。X与Y、Z、M 位于相邻周期,Z原子最外层电子数是X原子内层电子数的2 倍,Y、Z 相邻,M比X族序数大1。下列说法正确的是( ) A. 简单离子的半径:Y>X B. 简单氢化物的热稳定性:Z>M C. X和Z可形成ZX2分子 D. 最高价氧化物的水化物酸性:M>Y |
|
| 5. 选择题 | 详细信息 |
化合物 (y)、 (y)、A. y 的二氯代物有3 种 B. x、y和z均能与溴水发生反应 C. z 中的所有原子在同一平面上 D. x的同分异构体只有y和z两种 |
|
| 6. 选择题 | 详细信息 |
根据反应KMnO4+FeSO4+H2SO4→MnSO4+Fe2(SO4)3+K2SO4+H2O(未配平)设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。下列说法不正确的是( ) A. 石墨b是原电池的负极,发生氧化反应 B. 甲烧杯中的电极反应式:MnO4-+5e-+8H+===Mn2++4H2O C. 电池工作时,盐桥中的阴阳离子分别向乙甲烧杯中移动,保持溶液中的电荷平衡 D. 忽略溶液体积变化,Fe2(SO4)3浓度变为1.5 mol/L,则反应中转移的电子为0.1 mol |
|
| 7. 选择题 | 详细信息 |
某温度下,向10 mL 0.1 mol/L CuCl2溶液中滴加0.1mol/L的Na2S溶液,滴加过程中-lg c(Cu2+)与Na2S溶液体积的关系如图所示.下列有关说法正确的是( ) A.0.1mol/LNa2S溶液中:c(OH-)=c(H+)+c(HS-)+c(H2S) B.a、b、c三点对应的溶液中,水的电离程度最大的为b点 C.该温度下,Ksp(CuS)的数量级为10-36 D.向10 mL Ag+、Cu2+物质的量浓度均为0.1mol/L的混合溶液中逐滴加入0.01mol/L的Na2S溶液,Cu2+先沉淀[已知:Ksp(Ag2S)=6.4×10-50] |
|
| 8. | 详细信息 | ||||||||||||||||||||||||||||||
利用熔融碱焙烧工艺可从铝热法生产金属铬的铬渣(Al、Al2O3、Cr2O3等)中浸出铬和铝,为实现铬和铝的再生利用。其工作流程如下: (1)铝热法冶炼金属铬,是利用了金属铝的__________(填“氧化性”或“还原性”)。 (2)溶液1中的阴离子有CrO42-、______、_______。 (3)过程I,在Cr2O3参与的反应中,若生成0.4molCrO42-,消耗氧化剂的物质的量是_______。 (4)通入CO2调节溶液pH实现物质的分离。 ①滤渣A煅烧得到Al2O3,再用电解法冶炼Al。冶炼Al的化学方程式是____________________。 ②滤渣B受热分解所得物质可以循环利用,B是__________。 ③已知:2CrO42-+2H+ (5)过程II的目的是得到K2Cr2O7粗品。下表是不同温度下化合物的溶解度(g/100gH2O)
|
|||||||||||||||||||||||||||||||
| 9. 综合题 | 详细信息 |
|
研究发现,NOx和SO2是雾霾的主要成分。 Ⅰ. NOx主要来源于汽车尾气,可以利用化学方法将二者转化为无毒无害的物质。 已知:N2(g)+O2(g) 2CO(g)+O2(g) (1)2NO(g)+2CO(g) (2)T℃时,将等物质的量的NO和CO充入容积为2 L的密闭容器中,保持温度和体积不变,反应过程(0~15 min)中NO的物质的量随时间变化如图所示。  ①已知:平衡时气体的分压=气体的体积分数×体系的总压强,T℃时达到平衡,此时体系的总压强为p=20MPa,则T℃时该反应的压力平衡常数Kp =_______;平衡后,若保持温度不变,再向容器中充入NO和CO2各0.3mol,平衡将_____ (填“向左”、“向右”或“不”)移动。 ②15 min时,若改变外界反应条件,导致n(NO)发生如上图所示的变化,则改变的条件可能是_____(填序号) A.增大CO浓度 B.升温 C.减小容器体积 D.加入催化剂 Ⅱ. SO2主要来源于煤的燃烧。燃烧烟气的脱硫减排是减少大气中含硫化合物污染的关键。 已知:亚硫酸:Ka1=2.0×10-2 Ka2=6.0×10-7 (3)请通过计算证明,NaHSO3溶液显酸性的原因:_________________________ (4)如图示的电解装置,可将雾霾中的NO、SO2转化为硫酸铵,从而实现废气的回收再利用。通入NO的电极反应式为____________________;若通入的NO体积为4.48L(标况下),则另外一个电极通入的SO2质量至少为________g。  |
|
| 10. 实验题 | 详细信息 | ||||||||||||
无水四氯化锡(SnCl4)是一种用途广泛的锡化工中间体,实验室可用熔融的锡(熔点231℃)与Cl2反应制备SnCl4,装置如图所示,请回答下列问题: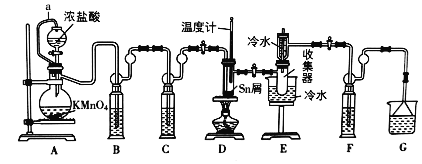 已知,SnCl4在潮湿的空气中极易水解生成SnO2•xH2O。
|
|||||||||||||
| 11. 推断题 | 详细信息 |
根皮素J ( )是一种新型天然美白剂,主要分布于苹果、梨等多汁水果的果皮及根皮.其中一种合成J的路线如下: )是一种新型天然美白剂,主要分布于苹果、梨等多汁水果的果皮及根皮.其中一种合成J的路线如下: 已知:  +R"CHO +R"CHO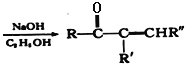 +H2O +H2O回答下列问题: (1)C的化学名称是___________.E中官能团的名称为_______________. (2)B为溴代烃,请写出A→B的反应试剂___________. (3)写出由C生成D的反应类型___________ (4)F→H的化学方程式为______________________. (5)M是E的同分异构体,同时符合下列条件的M的结构有___________种(不考虑立体异构) ①能与FeCl3溶液发生显色反应 ②能发生银镜反应 (6)设计以丙烯和1,3-丙二醛为起始原料制备 |
|
| 12. 综合题 | 详细信息 |
|
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题: (1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。 A.404.4 B.553.5 C.589.2 D.670.8 E.766.5 (2)基态K原子中,核外电子占据的最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。 (3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________,中心原子的杂化形式为________________。 (4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。 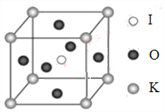 |
|



