盈江县第一高级中学高一化学上册期末考试在线测验完整版
| 1. 选择题 | 详细信息 |
|
现有以下几种措施:①对燃烧煤产生的尾气进行除硫处理;②少用原煤做燃料;③燃煤时鼓入足量空气;④开发清洁能源。其中能减少酸雨产生的措施是 A. ①②③ B. ①②④ C. ①③④ D. ②③④ |
|
| 2. 选择题 | 详细信息 |
|
对于硫酸和硝酸的比较中,下列叙述不正确的是 A.冷的浓硫酸和浓硝酸都可以用铝、铁的容器盛装 B.浓硫酸和浓硝酸都具有很强的腐蚀性、脱水性 C.稀硫酸和稀硝酸都具有氧化性 D.硫酸和硝酸都是重要的化工原料 |
|
| 3. 选择题 | 详细信息 |
|
下列物质中含有的电子数最多的是 A. 27 g H2O B. 51 g H2O2 C. 34 g OH- D. 19 g H3O+ |
|
| 4. 选择题 | 详细信息 |
|
已知:2Fe2++Cl2===2Cl﹣+2Fe3+,2Br﹣+Cl2===Br2+2Cl﹣,2Fe2++Br2===2Br﹣+2Fe3+。含有amol FeBr2的溶液中,通入xmol Cl2,下列各项为通Cl2过程中,溶液内发生反应的离子方程式,其中不正确的是( ) A. x=0.4a,2Fe2++Cl2===2Fe3++2Cl﹣ B. x=0.6a,2Br﹣+Cl2===Br2+2Cl﹣ C. x=a,2Fe2++2Br﹣+2Cl2===Br2+2Fe3++4Cl﹣ D. x=1.5a,2Fe2++4Br﹣+3Cl2===2Br2+2Fe3++6Cl﹣ |
|
| 5. 选择题 | 详细信息 |
|
在水泥厂、冶金厂常用高压电作用于气溶胶,以除去大量烟尘,减少烟尘对空气的污染。这种除尘法的原理是( ) A.渗析 B.电泳 C.聚沉 D.丁达尔效应 |
|
| 6. 选择题 | 详细信息 |
|
常温下,不能使金属铝溶解的物质是( ) A. 硫酸铜溶液 B. 稀硫酸 C. 浓硫酸 D. 氢氧化钠溶液 |
|
| 7. 选择题 | 详细信息 |
|
将20 mL0.5 mol•L﹣1K2SO3溶液逐滴加入到20 mL 0.2 mol•L﹣1硫酸酸化的紫色KMnO4溶液中,溶液恰好变为无色,则Mn元素在产物中的存在形态是( ) A. Mn B. Mn2+ C. Mn2O3 D. K2MnO4 |
|
| 8. 选择题 | 详细信息 |
|
下列各组都为两种化合物溶于水时电离出的离子:①Na+、OH-、 A. ②③④ B. ②①④ C. ②③① D. ②①③ |
|
| 9. 选择题 | 详细信息 |
|
下列物质的属类归纳不正确的是( ) A. 由两种或两种以上元素组成的纯净物称为化合物 B. 由一种元素组成的纯净物是单质 C. 由一种物质组成的称为纯净物 D. 含氧元素的化合物称为氧化物 |
|
| 10. 选择题 | 详细信息 |
|
能用H++OH﹣===H2O来表示的化学反应是( ) A. 固体Cu(OH)2和稀盐酸反应 B. 澄清石灰水和HNO3溶液反应 C. KOH溶液和醋酸溶液反应 D. Ba(OH)2溶液和H2SO4溶液反应 |
|
| 11. 选择题 | 详细信息 |
|
溶液具有导电性是因为其中存在自由移动的离子。向氢氧化钡溶液中加入下列物质至恰好完全反应,溶液导电能力不会发生明显变化的是( ) A.硫酸 B.硫酸铜 C.二氧化碳 D.硫酸钠 |
|
| 12. 选择题 | 详细信息 |
|
目前未列入我国“城市空气质量日报”报告的是 A.二氧化碳 B.二氧化硫 C.二氧化氮 D.可吸入颗粒 |
|
| 13. 选择题 | 详细信息 |
|
不锈钢通常不与酸、碱、盐反应,是因为加入了( ) A. Ni和Cr B. Ni和Au C. Cr和 Au D. Cr和Pt |
|
| 14. 选择题 | 详细信息 |
|
不能鉴别二氧化硫和二氧化碳的化学试剂是( ) A.澄清石灰水 B.品红溶液 C.高锰酸钾溶液 D.溴水 |
|
| 15. 选择题 | 详细信息 |
|
有NO、CO2、N2O4三种气体,它们分别都含有0.5 mol氧原子,则三种气体的物质的量之比为( ) A. 1:2:4 B. 1:1:1 C. 4:2:1 D. 1:2:4 |
|
| 16. 选择题 | 详细信息 |
|
将1.12 g铁粉加入到25 mL 2 mol·L-1的氯化铁溶液中,充分反应后,其结果是( ) A.铁粉剩余,溶液呈浅绿色,Cl-基本不变 B.向溶液中滴入无色硫氰化钾溶液,仍无色 C.溶液中Fe2+与Fe3+物质的量之比为6∶1 D.氧化产物与还原产物的物质的量之比为2∶5 |
|
| 17. 选择题 | 详细信息 |
|
当光束通过下列分散系: ①有尘埃的空气 ②稀硫酸 ③蒸馏水 ④墨水,能观察到有丁达尔效应的是( ) A. ①② B. ②③ C. ①④ D. ②④ |
|
| 18. 选择题 | 详细信息 |
|
下列关于氮气的性质和用途的叙述中错误的是( ) A. 是一种很难溶于水的无色无味气体 B. 通常情况下,很难与其它物质发生化学反应 C. 从空气中分离出的氮气,可用于填充白炽灯的灯泡 D. 从空气中分离出的氮气,不能用于生产氮肥 |
|
| 19. 选择题 | 详细信息 |
|
下列各组物质,前者属于电解质,后者属于非电解质的是( ) A. NaCl晶体、BaSO4 B. 铜、二氧化硫 C. 液态的醋酸、酒精 D. 熔融的KNO3、硫酸溶液 |
|
| 20. | 详细信息 |
|
下列叙述正确的是( ) A. Na在空气中久置最终变为NaHCO3粉末 B. 向Fe2(SO4)3溶液中加入铜粉,溶液变蓝且有黑色固体析出 C. C12能与石灰乳反应,可用于制取漂白粉 D. 向KC1O3溶液中滴加AgNO3溶液得到白色AgCl沉淀 |
|
| 21. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数,下列说法中正确的是( ) A. 1 000 mL 0.1 mol·L-1的NaCl溶液中,Na+与Cl﹣总数为0.2NA B. 2NA个二氧化碳分子的质量为44 g C. NA个氢气分子所占的体积为22.4 L D. 17 g氨气中所含原子数为NA |
|
| 22. 选择题 | 详细信息 |
|
下列离子方程式的书写正确的是( ) A. 实验室用大理石和稀盐酸制取CO2:2H++CO32-===CO2↑+H2O B. 铁和稀硝酸反应:Fe+2H+===H2↑+Fe2+ C. 向AlCl3溶液中加入过量的NaOH溶液:Al3++3OH﹣===Al(OH)3↓ D. NaHCO3溶液与NaOH溶液反应:OH﹣+ HCO3-=== CO32-+H2O |
|
| 23. 填空题 | 详细信息 |
|
氮、磷、砷(As)、锑(Sb)、铋(Bi)、镆(Mc)为元素周期表中原子序数依次增大的同族元素。回答下列问题: (1)砷在元素周期表中的位置______。 已知:P(s,白磷)=P(s,黑磷) ΔH=-39.3 kJ·mol-1;P(s,白磷)=P(s,红磷) ΔH=-17.6 kJ·mol-1;由此推知,其中最稳定的磷单质是________。 (2)氮和磷氢化物性质的比较:热稳定性:NH3________PH3(填“>”或“<”)。沸点:N2H4________P2H4(填“>”或“<”),判断依据是____________。 |
|
| 24. 实验题 | 详细信息 |
某学习小组的同学对氯气与铁的反应及产物进行了如下探究: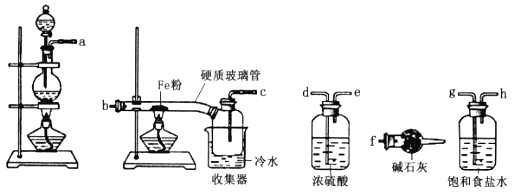 (1)装置的连接顺序为a→_____→______→_____→_____→b→c→f。________ (2)硬质玻璃管与收集器之间没有用导管连接,这样做的优点是________________。 (3)反应一段时间,熄灭酒精灯,冷却后,将收集器及硬质玻璃管中的物质快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:  试剂X中溶质的化学式为____________;固体产物的成分可能为_____(填字母)。 A.Fe和FeCl3 B.FeCl2 和FeCl3 C.Fe、FeCl2和FeCl3 D.Fe和FeCl2 (4)加入少许植物油的作用是____________,加入新制氯水后溶液红色加深的原因:___________(用离子方程式表示)。 (5)现有一含FeCl2和FeCl3混合物的样品,用离子交换法测得n(Fe):n(Cl)=1:2.1,则该样品中FeCl3的物质的量分数为______。(计算结果保留两位有效数字) |
|
| 25. 推断题 | 详细信息 |
某化学兴趣小组用含A、B两种金属单质的粉末状混合物进行如下实验,其转化关系如下图所示(部分反应物和生成物未列出),其中E为白色胶状沉淀,I为红褐色沉淀。(此转化关系中所用的试剂都是足量的)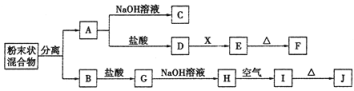 (1)写出下列物质的化学式:F____________,G________________。 (2)将混合物中两种金属分离开的最简单的方法是___________。 (3)D→E的转化中,加入过量的X可能是_____________________。 A.饱和NaCl溶液 B.NaOH溶液 C.氨水 D.Ba(OH)2溶液 (4)写出下列转化的化学方程式: A→C:______________________________________________; H→I:_______________________________________________。 |
|
| 26. 实验题 | 详细信息 |
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下: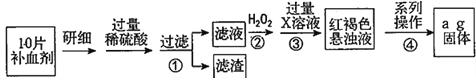 请回答下列问题: (1)向操作①的滤液中滴加KSCN 溶液后变为红色,则该滤液中含有______(填离子符号)。 (2)操作②中反应的离子方程式:__________________________________。 (3)操作③中反应的离子方程式:__________________________________。 (4)操作④中一系列处理的操作步骤:过滤、______、灼烧、_______、称量。 (5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为______g。(用含a的代数式表示) |
|
| 27. 推断题 | 详细信息 |
|
有A、B、C、D四种元素,A的最高正价与其最低负价的绝对值之差为6;A、D次外层都是8个电子,A与D的化合物DA在水溶液中能电离出具有相同电子层结构的阴、阳离子;B有两个电子层,其最高正价与最低负价的代数和为0;C2-与氩原子具有相同的电子层结构。 (1)试写出上述各元素的符号:A______,B______,C______,D______。 (2)画出下列粒子的结构示意图:A:________________,C2-:__________。 (3)元素A、C、D形成简单离子的半径由大到小的顺序是________________。 (4)写出A、D的最高价氧化物对应水化物反应的化学方程式:_____________。 |
|
| 28. 推断题 | 详细信息 |
(1)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题。 ①与离子相对应的元素符号是______________,与原子相对应的离子的结构示意图是______________。 ②电子层结构相同的是__________(填写代号,下同),性质最稳定的是__________,最容易失去电子的是__________,最容易得到电子的是__________。 ③可直接相互结合形成的化合物的化学式是____________。可经过得失电子后再相互结合形成的化合物的化学式是______________。 ④在核电荷数1~10的元素内,列举两个与B电子层结构相同的离子,写出离子的符号______________。 (2)已知元素X和Y的核电荷数均小于18,最外层电子数分别为n和(m-5),次外层有(n+2)个和m个电子,据此推断元素X和Y,其名称为X__________,Y__________。 |
|
高中化学 试卷推荐
- 高一后半期期末学业质量监测化学网上检测无纸试卷带答案和解析(2019-2020年广东省珠海市)
- 2018至2019年高二5月月考化学专题训练(河北省鸡泽县第一中学)
- 高一上学期期中考试化学免费试卷完整版(2019~2020年四川省成都石室中学)
- 四川省泸县第一中学2020届高三上半年期末考试理综化学考试完整版
- 高二下册4月考试化学题带参考答案(2019-2020年湖北省黄石市黄石二中)
- 山东省德州市2020届高三第一次模拟考试化学考试
- 2019-2020年高一10月月考化学考试完整版(广西南宁市第三中学)
- 2019-2020年高一上学期第一阶段考试化学题带答案和解析(辽宁省盘锦市第二高级中学)
最近更新



