й«ҳдёҖдёҠеҶҢжңҹжң«иҖғиҜ•еҢ–еӯҰйўҳеёҰзӯ”жЎҲе’Ңи§ЈжһҗпјҲ2019-2020е№ҙж№–еҚ—еёҲиҢғеӨ§еӯҰйҷ„еұһдёӯеӯҰпјү
| 1. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁдёӯпјҢдёҚеұһдәҺеҗҲйҮ‘зҡ„жҳҜпјҲ пјү A.зЎ¬й“қ B.й»„й“ң C.й’ўй“Ғ D.йҮ‘ |
|
| 2. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—еҸҷиҝ°дёӯпјҢй”ҷиҜҜзҡ„жҳҜпјҲ пјү A.ж‘©е°”жҳҜзү©иҙЁзҡ„йҮҸзҡ„еҚ•дҪҚ B.36gж°ҙдёӯеҗ«ж°ўеҺҹеӯҗж•°зӣ®дёә4NAпјҲNAиЎЁзӨәйҳҝдјҸеҠ еҫ·зҪ—еёёж•°зҡ„еҖјпјү C.еңЁ0.5molNa2SO4дёӯпјҢеҗ«жңүзҡ„Na+ж•°зәҰжҳҜ6.02Г—1023 D.зӯүиҙЁйҮҸзҡ„O2дёҺO3пјҢжүҖеҗ«ж°§еҺҹеӯҗж•°д№ӢжҜ”дёә3пјҡ2 |
|
| 3. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁеұһдәҺз”өи§ЈиҙЁзҡ„жҳҜпјҲ пјү A.Ba(OH)2 B.Cu C.Cl2 D.й…’зІҫ |
|
| 4. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
иҠӮж—ҘзҮғж”ҫзҡ„зғҹиҠұеҲ©з”ЁдәҶвҖңз„°иүІеҸҚеә”вҖқзҡ„еҺҹзҗҶгҖӮдёӢеҲ—иҜҙжі•дёӯжӯЈзЎ®зҡ„жҳҜ A.з„°иүІеҸҚеә”еұһдәҺеҢ–еӯҰеҸҳеҢ– B.NaClдёҺNa2CO3зҒјзғ§ж—¶зҒ«з„°йўңиүІзӣёеҗҢ C.жҹҗж ·е“Ғзҡ„з„°иүІйўңиүІдёәй»„иүІпјҢеҲҷиҜҘж ·е“Ғд»…еҗ«жңүй’ е…ғзҙ D.з„°иүІеҸҚеә”ж—¶йҮ‘еұһдёқеә”з”ЁзЎ«й…ёжё…жҙ—并еңЁеӨ–з„°дёҠзҒјзғ§иҮіжІЎжңүйўңиүІпјҢеҶҚиҳёеҸ–ж ·е“ҒзҒјзғ§ |
|
| 5. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—жңүе…ізҰ»еӯҗж–№зЁӢејҸй”ҷиҜҜзҡ„жҳҜпјҲ пјү A.зӣҗй…ёдёҺж°ўж°§еҢ–й’Ўжә¶ж¶ІеҸҚеә”пјҡH++OH-=H2O B.зўій…ёй’ҷдёҺзЁҖзӣҗй…ёеҸҚеә”пјҡCaCO3+2H+=Ca2++CO2вҶ‘+H2O C.й“ңзІүдёҺи¶ійҮҸзҡ„зЁҖзЎқй…ёеҸҚеә”пјҡ3Cu+8H++2NO3-=3Cu2++2NOвҶ‘+4H2O D.зЎ«й…ёй“қжә¶ж¶ІдёҺиҝҮйҮҸж°ўж°§еҢ–й’ жә¶ж¶ІеҸҚеә”пјҡAl3++3OH-=Al(OH)3вҶ“ |
|
| 6. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
жҹҗжә¶ж¶Ідёӯеҗ«жңүNa+гҖҒK+гҖҒHCO A.Na+ B.SO |
|
| 7. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёӢеҲ—зү©иҙЁйғҪе…·жңүжјӮзҷҪжҖ§пјҢжјӮзҷҪеҺҹзҗҶдёҺе…¶е®ғеҮ з§ҚдёҚеҗҢзҡ„жҳҜпјҲ пјү A.ж°Ҝж°ҙ B.SO2 C.H2O2 D.HClO |
|
| 8. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
й«ҳзәҜеәҰжҷ¶дҪ“зЎ…жҳҜиүҜеҘҪзҡ„еҚҠеҜјдҪ“жқҗж–ҷпјҢе®ғзҡ„еҸ‘зҺ°е’ҢдҪҝз”Ёеј•иө·дәҶи®Ўз®—жңәзҡ„дёҖеңәвҖңйқ©е‘ҪвҖқгҖӮе®ғеҸҜд»ҘжҢүдёӢеҲ—ж–№жі•еҲ¶еӨҮпјҡ SiO2 дёӢеҲ—иҜҙжі•дёҚжӯЈзЎ®зҡ„жҳҜпјҲ пјү A.жӯҘйӘӨв‘ўдёӯж°ўж°”дҪңиҝҳеҺҹеүӮ B.зЎ…е’ҢдәҢж°§еҢ–зЎ…йғҪиғҪз”ЁдҪңи®Ўз®—жңәвҖңиҠҜзүҮвҖқ C.жӯҘйӘӨв‘ зҡ„еҢ–еӯҰж–№зЁӢејҸдёәпјҡSiO2+2C D.жӯҘйӘӨв‘ в‘Ўв‘ўдёӯеҸ‘з”ҹзҡ„еҸҚеә”йғҪеұһдәҺж°§еҢ–иҝҳеҺҹеҸҚеә” |
|
| 9. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
е·ІзҹҘдёүдёӘж°§еҢ–иҝҳеҺҹеҸҚеә”пјҡ в‘ в‘Ў в‘ў иӢҘжҹҗжә¶ж¶Ідёӯ A. |
|
| 10. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
еҸӘз”ЁдёҖз§ҚиҜ•еүӮеҢәеҲ«Na2SO4гҖҒMgCl2гҖҒAl2(SO4)3дёүз§Қжә¶ж¶ІпјҢиҝҷз§ҚиҜ•еүӮжҳҜпјҲ пјү A.H2SO4 B.Ba(OH)2 C.NaOH D.AgNO3 |
|
| 11. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||
дёӢеҲ—е®һйӘҢиғҪиҫҫеҲ°зӣ®зҡ„зҡ„жҳҜпјҲ пјү
|
|||||||||||||
| 12. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
ClO2жҳҜдёҖз§Қж–°еһӢж°ҙж¶ҲжҜ’еүӮпјҢе·ҘдёҡдёҠз”ЁNaClO2дёҺзӣҗй…ёеҸҚеә”еҲ¶еӨҮClO2зҡ„еҸҚеә”дёә5NaClO2+4HCl(зЁҖ)=5NaCl+4ClO2вҶ‘+2H2OпјҢдёӢеҲ—иҜҙжі•жӯЈзЎ®зҡ„жҳҜпјҲ пјү A.еҸҚеә”дёӯHClдҪңиҝҳеҺҹеүӮ B.ClO2д№ӢжүҖд»ҘиғҪеҒҡж°ҙж¶ҲжҜ’еүӮпјҢжҳҜеҲ©з”ЁдәҶе®ғзҡ„ејәж°§еҢ–жҖ§ C.еҸҚеә”дёӯж°§еҢ–дә§зү©дёҺиҝҳеҺҹдә§зү©зү©иҙЁзҡ„йҮҸд№ӢжҜ”дёә4пјҡ5 D.еҸҚеә”дёӯжҜҸз”ҹжҲҗ1molClO2иҪ¬з§»4molз”өеӯҗ |
|
| 13. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
дёҖеқ—иЎЁйқўе·ұиў«зј“ж…ўж°§еҢ–зҡ„йҮ‘еұһй’ пјҢе…¶иҙЁйҮҸдёә10.8gпјҢжҠ•е…Ҙ100gж°ҙдёӯпјҢ收йӣҶеҲ°ж°ўж°”0.2gгҖӮеҲҷеҺҹжқҘй’ еқ—иЎЁйқўиў«ж°§еҢ–зҡ„й’ зҡ„иҙЁйҮҸжҳҜ A.6.2g B.4.6g C.7.8g D.10.6g |
|
| 14. йҖүжӢ©йўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
е°Ҷ0.4g NaOHе’Ң1.06g Na2CO3ж··еҗҲ并й…ҚжҲҗжә¶ж¶ІпјҢеҗ‘жә¶ж¶Ідёӯж»ҙеҠ 0.1molВ·L-1зЁҖзӣҗй…ёгҖӮдёӢеҲ—еӣҫеғҸиғҪжӯЈзЎ®иЎЁзӨәеҠ е…Ҙзӣҗй…ёзҡ„дҪ“з§Ҝе’Ңз”ҹжҲҗCO2зҡ„зү©иҙЁзҡ„йҮҸзҡ„е…ізі»зҡ„жҳҜпјҲ пјү A. 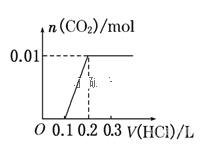 B. B. C.  D. D. |
|
| 15. еЎ«з©әйўҳ | иҜҰз»ҶдҝЎжҒҜ |
|
еҢ–еӯҰдёҺдәәзұ»з”ҹжҙ»еҜҶеҲҮзӣёе…ігҖӮиҜ·жҢүиҰҒжұӮпјҢеӣһзӯ”дёӢеҲ—й—®йўҳпјҡ пјҲ1пјүе®ҮиҲӘе‘ҳеёёз”ЁиҝҮж°§еҢ–й’ дҪңдҫӣж°§еүӮпјҢеҶҷеҮәеҜ№еә”еҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢ__гҖҒ__гҖӮ пјҲ2пјүж–°еҲ¶ж°Ҝж°ҙеңЁйҳіе…үз…§е°„дёӢе®№жҳ“еҲҶи§Јдә§з”ҹж— иүІж°”дҪ“пјҢиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸжҳҜ__гҖӮ е·ҘдёҡдёҠе°Ҷж°Ҝж°”йҖҡе…ҘеҶ·зҡ„ж¶ҲзҹізҒ°еҲ¶жҲҗжјӮзҷҪзІүпјҢеҶҷеҮәиҜҘеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸ并用еҸҢзәҝжЎҘжі•иЎЁзӨәз”өеӯҗиҪ¬з§»зҡ„ж–№еҗ‘е’Ңж•°зӣ®зҡ„__гҖӮ пјҲ3пјүKAl(SO4)2В·12H2Oеӣ е…¶жә¶дәҺж°ҙз”ҹжҲҗ__пјҲеҢ–еӯҰејҸпјүиғ¶дҪ“еҸҜд»Ҙеҗёйҷ„жқӮиҙЁпјҢд»ҺиҖҢиҫҫеҲ°еҮҖж°ҙзҡ„зӣ®зҡ„гҖӮ пјҲ4пјүK2FeO4жҳҜдёҖз§ҚйҮҚиҰҒзҡ„еҮҖж°ҙеүӮпјҢеҸҜз”ЁдёӢеҲ—ж–№жі•еҲ¶еҫ—пјҡ2Fe(OH)3+3Cl2+10KOH |
|
| 16. | иҜҰз»ҶдҝЎжҒҜ |
дёүж°ҜеҢ–й“Ғжә¶ж¶ІеҸҜи…җиҡҖеҚ°еҲ·з”өи·ҜжқҝдёҠзҡ„й“ңиҶңпјҢжҹҗе°Ҹз»„дёәдәҶд»Һи…җиҡҖеәҹж¶ІпјҲеҗ«жңүеӨ§йҮҸCuCl2гҖҒFeCl2е’ҢFeCl3пјүдёӯеӣһ收й“ңпјҢ并е°Ҷй“Ғзҡ„еҢ–еҗҲзү©е…ЁйғЁиҪ¬еҢ–дёәжә¶ж¶ІдҪңдёәи…җиҡҖж¶ІеҺҹж–ҷеҫӘзҺҜдҪҝз”ЁпјҢи®ҫи®ЎдәҶеҰӮдёӢе®һйӘҢжӯҘйӘӨпјҡ пјҲ1пјүеҶҷеҮәдёӢеҲ—зү©иҙЁзҡ„еҢ–еӯҰејҸв‘ __гҖҒв‘ў___гҖҒв‘Ҙ__гҖӮ пјҲ2пјүжӯҘйӘӨв… зҡ„ж“ҚдҪңеҗҚз§°пјҡ___гҖӮ пјҲ3пјүеҶҷеҮәFeCl3жә¶ж¶ІдёҺй“ңеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸпјҡ__гҖӮ пјҲ4пјүеҗ‘в‘ЎдёӯеҠ е…ҘNaOHжә¶ж¶Іе№¶й•ҝж—¶й—ҙжҡҙйңІеңЁз©әж°”дёӯпјҢе…Ҳдә§з”ҹзҷҪиүІжІүж·ҖпјҢеҗҺиҝ…йҖҹеҸҳдёәзҒ°з»ҝиүІпјҢжҺҘзқҖеҸҲиҪ¬еҢ–дёә___иүІжІүж·ҖпјҢжӯӨиҝҮзЁӢжүҖж¶үеҸҠеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸдёәпјҡ___гҖҒ___гҖӮ пјҲ5пјүйҖҡе…Ҙв‘ҘеҸ‘з”ҹеҸҚеә”зҡ„зҰ»еӯҗж–№зЁӢејҸпјҡ___гҖӮ пјҲ6пјүиӢҘеҗ‘зӣӣжңүж°ҜеҢ–й“Ғжә¶ж¶Ізҡ„зғ§жқҜдёӯеҗҢж—¶еҠ е…Ҙй“ҒзІүе’Ңй“ңзІүпјҢеҸҚеә”з»“жқҹеҗҺпјҢдёӢеҲ—з»“жһңдёҚеҸҜиғҪеҮәзҺ°зҡ„жҳҜ__пјҲеЎ«еӯ—жҜҚд»ЈеҸ·пјүгҖӮ A.жңүй“ңж— й“Ғ B.жңүй“Ғж— й“ң C.й“ҒгҖҒй“ңйғҪжңү D.й“ҒгҖҒй“ңйғҪж— |
|
| 17. е®һйӘҢйўҳ | иҜҰз»ҶдҝЎжҒҜ |
жҹҗиҜҫеӨ–жҙ»еҠЁе°Ҹз»„еңЁе®һйӘҢе®Өз”ЁеҰӮеӣҫжүҖзӨәиЈ…зҪ®еҲ¶еҸ–氨并йӘҢиҜҒж°Ёзҡ„жҹҗдәӣжҖ§иҙЁпјҢиҜ·еӣһзӯ”гҖӮ пјҲ1пјүеҶҷеҮәжӯӨе®һйӘҢдёӯеҲ¶ж°Ёзҡ„еҢ–еӯҰж–№зЁӢејҸпјҡ___гҖӮ пјҲ2пјүе®һйӘҢиҝӣиЎҢдёҖж®өж—¶й—ҙпјҢи§ӮеҜҹеҲ°зЎ¬иҙЁзҺ»з’ғз®ЎеҶ…й»‘иүІж°§еҢ–й“ңзІүжң«еҸҳдёәзәўиүІпјҢзӣӣж— ж°ҙзЎ«й…ёй“ңзҡ„е№ІзҮҘз®ЎеҶ…еҮәзҺ°и“қиүІпјҢеҗҢж—¶жңүж°®ж°”з”ҹжҲҗгҖӮж №жҚ®иҝҷдәӣзҺ°иұЎпјҢеҶҷеҮәеңЁзЎ¬иҙЁзҺ»з’ғз®ЎеҶ…еҸ‘з”ҹеҸҚеә”зҡ„еҢ–еӯҰж–№зЁӢејҸпјҡ__пјҢиҝҷдёӘеҸҚеә”иҜҙжҳҺж°Ёе…·жңү___пјҲеЎ«еӯ—жҜҚд»ЈеҸ·пјүгҖӮ A.зўұжҖ§ B.иҝҳеҺҹжҖ§ C.ж°§еҢ–жҖ§ D.дёҚзЁіе®ҡжҖ§ пјҲ3пјүиЈ…зҪ®Eзҡ„дҪңз”ЁжҳҜ__пјҢиЈ…зҪ®Fзҡ„дҪңз”ЁжҳҜ___гҖӮEдёӯзҡ„зўұзҹізҒ°__пјҲеЎ«вҖңиғҪвҖқжҲ–вҖңдёҚиғҪвҖқпјүжҚўжҲҗCaCl2гҖӮ пјҲ4пјүDдёӯжө“зЎ«й…ёзҡ„дё»иҰҒдҪңз”ЁжҳҜ___гҖӮ |
|
| 18. з»јеҗҲйўҳ | иҜҰз»ҶдҝЎжҒҜ | ||||||||||||||
|
жҹҗеҹҺеёӮеҜ№еӨ§ж°”иҝӣиЎҢзӣ‘жөӢпјҢеҸ‘зҺ°иҜҘеёӮйҰ–иҰҒжұЎжҹ“зү©дёәеҸҜеҗёе…Ҙйў—зІ’зү©PM2.5пјҲзӣҙеҫ„е°ҸдәҺзӯүдәҺ2.5Ојmзҡ„жӮ¬жө®йў—зІ’зү©пјүпјҢе…¶дё»иҰҒжқҘжәҗдёәзҮғз…ӨгҖҒжңәеҠЁиҪҰе°ҫж°”зӯүгҖӮеӣ жӯӨпјҢеҜ№PM2.5гҖҒSO2гҖҒNOxзӯүиҝӣиЎҢз ”з©¶е…·жңүйҮҚиҰҒж„Ҹд№үгҖӮиҜ·еӣһзӯ”дёӢеҲ—й—®йўҳ пјҲ1пјүе°ҶPM2.5ж ·жң¬з”Ёи’ёйҰҸж°ҙеӨ„зҗҶеҲ¶жҲҗеҫ…жөӢиҜ•ж ·гҖӮиӢҘжөӢеҫ—иҜҘиҜ•ж ·жүҖеҗ«ж°ҙжә¶жҖ§ж— жңәзҰ»еӯҗзҡ„еҢ–еӯҰз»„еҲҶеҸҠе…¶е№іеқҮжө“еәҰеҰӮдёӢиЎЁпјҡ
|
|||||||||||||||
- 2016-2017е№ҙй«ҳдёүдёӢеҚҠе№ҙзҗҶз»јеҢ–еӯҰејҖеӯҰиҖғиҜ•пјҲзҰҸе»әзңҒеҺҰ门第дёҖдёӯеӯҰпјү
- 2016-2017е№ҙй«ҳдёҖдёҠжңҹеҢ–еӯҰжңҹдёӯиҖғиҜ•иҜ•еҚ·пјҲдә‘еҚ—зңҒзҺүжәӘдёҖдёӯпјү
- 2018еұҠй«ҳдёүдёҠеӯҰжңҹ第дёҖж¬Ўз»ҹдёҖиҖғиҜ•еҢ–еӯҰпјҲжІіеҚ—зңҒжҙӣйҳіеёӮпјү
- й«ҳдёӯеҢ–еӯҰдәәж•ҷзүҲ еҝ…дҝ®2 第дёүз« жңүжңәеҢ–еҗҲзү© 第дёүиҠӮ з”ҹжҙ»дёӯдёӨз§Қеёёи§Ғзҡ„жңүжңәзү© д№ҷй…ё
- й«ҳдёӯеҢ–еӯҰдәәж•ҷзүҲ йҖүдҝ®дә” 第еӣӣз« з¬¬дёүиҠӮ иӣӢзҷҪиҙЁе’Ңж ёй…ё
- 2018еұҠй«ҳдёү第дёҖж¬ЎзҗҶз»јжөӢиҜ•еҢ–еӯҰеңЁзәҝжөӢйӘҢпјҲеұұдёңзңҒж–°жі°еёӮж–°жұ¶дёӯеӯҰпјү
- 2016-2017е№ҙй«ҳдёҖдёӢеӯҰжңҹжңҹдёӯиҖғиҜ•еҢ–еӯҰиҖғиҜ•пјҲжұҹиӢҸзңҒеҚ—дә¬еёӮйҮ‘йҷөдёӯеӯҰпјү
- 2018еұҠй«ҳдёү12жңҲж‘ёеә•иҖғиҜ•еҢ–еӯҰеңЁзәҝжөӢйӘҢпјҲеұұдёңзңҒж·„еҚҡеёӮйғЁеҲҶеӯҰж Ўпјү







