2018-2019年高一上期期中考试化学考试(河南省信阳市罗山高级中学)
| 1. 选择题 | 详细信息 |
在盛放浓硫酸的试剂瓶的标签上应印有下列警示标记中的是( )。 |
|
| 2. 选择题 | 详细信息 |
|
如图所示的实验操作中,正确的是( ) A. 检查容量瓶是否漏水  B. 给溶液加热 B. 给溶液加热 C. 滴加液体 C. 滴加液体 D. 过滤 D. 过滤 |
|
| 3. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数,下列说法中,正确的是( )。 A. 2.4 g金属镁所含电子数目为0.2 NA B. 16 g CH4所含原子数目为NA C. 标准状况下,22.4 L H2O含有的分子数为1NA D. 溶液的体积为1L,物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl—个数为1NA |
|
| 4. 选择题 | 详细信息 |
|
下列关于溶液和胶体的叙述,一定正确的是( )。 A. 溶液是电中性的,胶体是带电的 B. 卤水点豆腐与胶体的性质无关 C. 布朗运动是胶体微粒特有的运动方式,可以据此把胶体和溶液、悬浊液区别开来 D. 一束光线分别通过溶液和胶体时,后者会出现明显的光路,前者则没有 |
|
| 5. 选择题 | 详细信息 |
下列化学反应属于阴影部分的是( ) A.CuSO4+Fe=Cu+FeSO4 B.2NaHCO3 C.2Na2O2+2CO2=2Na2CO3+O2↑ D.4Fe(OH)2+O2+2H2O=4Fe(OH)3 |
|
| 6. 选择题 | 详细信息 |
|
下列说法错误的一组是( ) ①不溶于水的BaSO4 是强电解质 ②可溶于水的酸都是强电解质 ③0.5mol/L的所有一元酸中氢离子浓度都是0.5mol/L ④熔融态的电解质都能导电。 A. ①③④ B. ②③④ C. ①④ D. ①②③ |
|
| 7. 选择题 | 详细信息 |
|
以下三组溶液:①煤油和硫酸钾溶液 ②42%的乙醇水溶液 ③单质溴和水溶液,分离以上各混合液的正确方法依次是( )。 A. 分液、蒸馏、萃取 B. 萃取、蒸馏、分液 C. 分液、萃取、蒸馏 D. 蒸馏、萃取、分液 |
|
| 8. 选择题 | 详细信息 |
|
硫酸镁和硫酸铝溶液等体积混合后,铝离子浓度为0.2mol/L,硫酸根离子的浓度为0.5 mol/L,则混和溶液中镁离子浓度为( )。 A. 0.15 mol/L B. 0.3 mol/L C. 0.45 mol/L D. 0.2 mol/L |
|
| 9. 选择题 | 详细信息 |
|
某反应的化学方程式为:aFeCl2+bKNO3+cHCl=dFeCl3+eKCl+fX+gH2O,若b=1,d=3,则X的化学式为( ) A.N2 B.NO C.NO2 D.NH4Cl |
|
| 10. 选择题 | 详细信息 |
|
下列各组离子中,在溶液中能大量共存,加入氢氧化钠溶液有沉淀析出,加入稀盐酸有气体放出的是( ) A. Na+、Ca2+、HCO3-、NO3- B. Na+、Ca2+、SO42-、CO32- C. K+、Al3+、SO42-、NO3- D. K+、Na+、CO32-、SO42- |
|
| 11. 选择题 | 详细信息 |
|
常温常压下,用等质量的CH4、CO2、O2、SO2四种气体分别吹出四个气球,其中气体为CH4的是( )。 A.  D. D.  |
|
| 12. 选择题 | 详细信息 |
|
能正确表示下列化学反应的离子方程式的是 A. 氢氧化钡溶液与硫酸的反应:OH-+H+===H2O B. 澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+===Ca2++2H2O C. 铜片插入硝酸银溶液中:Cu+Ag+===Cu2++Ag D. 碳酸钙溶于稀盐酸中:CaCO3+2H+="==" Ca2++H2O+CO2↑ |
|
| 13. 选择题 | 详细信息 |
|
下列溶液中Cl-浓度与50mL 1mol•L-1 AlCl3溶液中Cl-浓度相等的是( ) A. 150mL 3mol•L-1的KCl溶液 B. 75mL 2.5mol•L-1的CaCl2溶液 C. 150mL 3mol•L-1KClO3溶液 D. 25mL 2mol•L-1的FeCl3溶液 |
|
| 14. 选择题 | 详细信息 |
|
下列化学方程式中,不能用H++OH-=H2O表示的是 A. 2NaOH+H2SO4 =Na2SO4+2H2O B. Ba(OH)2+2HCl=BaCl2+2H2O C. Cu(OH)2+2HNO3=Cu(NO3)2+2H2O D. KOH+HCl=KCl+H2O |
|
| 15. 填空题 | 详细信息 |
|
根据问题填空: (1)有以下四种物质①22g二氧化碳;②5g氢气;③1.204×1024个氮气分子;④4℃时18g水,质量最大的是_______;常温时体积最大的是________(填序号)。 (2)标准状况下,336L的NH3溶于1L水中,若该溶液的密度为ag/cm3,则其物质的量浓度为____________。 (3)若20g密度为ρg·cm-3的硝酸钙溶液里含1gCa2+,则NO3-的物质的量浓度是_______________。 (4)现有下列九种物质:①AgCl ② 铜 ③液态醋酸 ④CO2 ⑤纯硫酸 ⑥Ba(OH)2固体 ⑦C2H5OH ⑧稀硝酸 ⑨熔融NaOH。 ①上述属于电解质的是_______________________。 ②上述九种物质中有两种物质之间可发生离子反应H++OH-=H2O,该离子反应对应的化学方程式为______________________________。 |
|
| 16. 实验题 | 详细信息 |
掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为三套实验装置。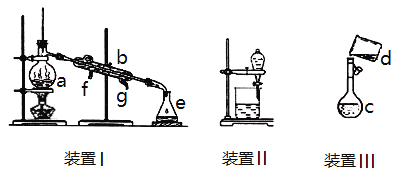 (1)写出下列仪器的名称:a.___________________b.____________________。 (2)若利用装置I分离四氯化碳和酒精的混合物,冷凝水由_____(填f或g)口通入。 (3)用装置II分离混合物时,为使液体顺利流下,应进行的操作是_____________。 (4)实验室用Na2CO3·10H2O晶体配制0.05mol/L的Na2CO3溶液970mL。 ①应用托盘天平称取Na2CO3·10H2O的质量是_____________g。 ②装置III是某同学转移溶液的示意图。图中的错误是___________________。 (5)定容时,俯视刻度线,对所配溶液浓度的影响:_____________(填:偏大、偏小、或无影响)。 |
|
| 17. 推断题 | 详细信息 | ||||||||||||||||||||||||
现有失去标签的四瓶无色溶液分别为Na2CO3溶液、稀盐酸、Ba(OH)2溶液、NaHSO4溶液,为确定四瓶溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示。
|
|||||||||||||||||||||||||
| 18. 填空题 | 详细信息 |
|
二氧化硒(SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HNO3或浓H2SO4反应生成SeO2以回收Se。 已知:①Se+2H2SO4(浓)===2SO2↑+SeO2+2H2O; ②2SO2+SeO2+2H2O===Se+2SO42—+4H+。 (1) Se与浓H2SO4的反应中,氧化剂是________________,还原剂是_______________。当有标准状况下22.4 L SO2气体生成时,转移电子的物质的量是________ mol。 (2)依据反应①、②判断SeO2、浓H2SO4、SO2的氧化性由强到弱的顺序是______________________。 (3)用单线桥法标出反应②电子转移的方向和数目:_____________________________。 (4)SeO2、KI和HNO3发生如下反应:SeO2+KI+HNO3―→Se+I2+KNO3+H2O配平上述反应的化学方程式______________________________________________。 |
|
最近更新



