高一7月学情测试化学试卷带参考答案和解析(2019-2020年山东省济南市)
| 1. 选择题 | 详细信息 |
|
近年来,我国在探索太空、开发5G,以及在抗击新冠肺炎等方面都取得了举世瞩目的成就这些成就都与化学有着密切的联系。下列有关说法正确的是 A.用75%的医用酒精杀死新型冠状病毒,是利用了酒精的强氧化性 B.大飞机C919采用了大量复合材料与铝锂合金,铝锂合金属于金属材料 C.5G技术的应用离不开光缆,我国光缆线路总长度超过了三千万千米,光缆的主要成分是晶体硅 D.“神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷属于有机高分子材料 |
|
| 2. 选择题 | 详细信息 |
|
下列关于电解质的说法正确的是 A.易溶于水的物质一定是电解质 B.熔融状态能导电的物质不一定是电解质 C.电解质中一定含有自由移动的阴阳离子 D.熔化电解质时一定会破坏化学键 |
|
| 3. 选择题 | 详细信息 |
|
下列实验所用装置正确的是 A.实验室制取氨气  B.分离乙醇和水的混合物 B.分离乙醇和水的混合物 C.干燥氨气  D.收集二氧化氮气体 D.收集二氧化氮气体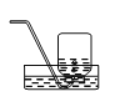 |
|
| 4. 选择题 | 详细信息 |
有机化合物TBPMA( )是一种常用的阻燃改性剂。下列关于TBP-MA的说法错误的是 )是一种常用的阻燃改性剂。下列关于TBP-MA的说法错误的是A.分子式为 B. C.完全燃烧的产物只有 D.在一定条件下可以发生加聚反应 |
|
| 5. 选择题 | 详细信息 |
|
《科学快报》报道了科学家观测到化学键产生过程的消息。下列关于化学键的说法正确的是 A.不含化学键的物质不能稳定存在 B.熔融状态能够导电的物质一定不含共价键 C.离子键是指阴阳离子间的静电引力 D.只含共价键的物质不一定是共价化合物 |
|
| 6. 选择题 | 详细信息 |
|
中国科学院上海硅酸盐研究所设计出以金属锂作负极,以“催化剂一碳一催化剂”结构的材料作正极的高稳定锂硫电池,具有较高的能量密度(单位质量的电池所放出的能量)。下列关于这种电池的说法错误的是 A.能量密度高的原因之一是锂的相对原子质量小 B.放电时电能转化为化学能 C.放电时硫在正极上发生还原反应 D.放电时锂离子向正极移动 |
|
| 7. 选择题 | 详细信息 |
|
短周期主族元素甲、乙、丙、丁、戊的原子序数依次增大。已知甲和丙的原子最外层电子数均为乙原子电子层数的一半,且甲的原子半径小于乙的原子半径。乙和丁同主族,且乙原子的最外层电子数是丁原子电子层数的2倍。下列说法正确的是 A.甲和丙形成的化合物中,甲的化合价为+1 B.乙和丙形成的化合物中,不可能存在共价键 C.气态氢化物的稳定性:戊>丁 D.戊的含氧酸均为强酸,且具有强氧化性 |
|
| 8. 选择题 | 详细信息 |
|
A.常温常压下,22.4g鲸蜡烯 B. C. D.10.4g苯乙烯( |
|
| 9. 选择题 | 详细信息 | ||||||||||
炼铁高炉中发生的主要反应为
|
|||||||||||
| 10. 选择题 | 详细信息 |
硝酸铵钙 A.若要加快“过滤”的速率,可以采用抽滤的方法 B.“蒸发”时所用的坩埚应该放置在泥三角上 C.“结晶”时为防止晶体脱水通常采用降温结晶的方式 D.加入碳酸钙的目的之一是调节铵钙比 |
|
| 11. 选择题 | 详细信息 |
|
下列化学用语正确的是 A.中子数为8的氧原子: B. C.HClO的结构式: D.丙烷分子的填充模型:  |
|
| 12. 选择题 | 详细信息 |
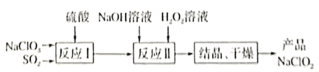 A.反应Ⅰ中会生成含+4价氯元素的化合物 B.反应Ⅱ最好在高温条件下进行,以加快反应的速率 C. D.相同质量的 |
|
| 13. 选择题 | 详细信息 |
|
在绝热的恒容容器中发生反应 A.消耗 B.混合气体的颜色(透光率)不再改变 C.混合气体的压强不再改变 D.混合气体的密度不再改变 |
|
| 14. 选择题 | 详细信息 |
|
某种复合膨松剂的组成如下:碳酸氢钠21%,酒石酸氢钾 A.淀粉与纤维素互为同分异构体 B.该膨松剂中钠和钾的质量分数相等 C.该膨松剂的作用原理之一是酒石酸氢钾中的羧基与碳酸氢根反应 D.100g该膨松剂与足量盐酸反应,可产生气体1.4L |
|
| 15. 选择题 | 详细信息 |
|
向含有 A.若 B.若 C.若 D.若 |
|
| 16. | 详细信息 |
|
短周期主族元素甲、乙、丙、丁、戊的原子序数依次增大。其中甲是所有元素中原子半径最小的元素,乙、戊两种元素原子的最外层电子数都是电子层数的两倍,由丙、丁两元素组成的化合物A为淡黄色固体。回答下列问题: (1)写出丙在元素周期表中的位置:_________;戊的原子结构示意图:_________; (2)丙、丁、戊三种元素形成的简单离子中半径最小的是_________(用离子符号表示);由甲、丙、丁、戊四种元素组成的化合物含有的化学键类型为_________; (3)下列说法正确的有_________(填标号); A.甲和乙组成的化合物在常温下一定呈气态 B.丙和戊都存在同素异形体 C.丙和丁组成的两种常见化合物中阴阳离子的个数比均为1:2 D.甲和乙组成的化合物中各原子均达到了8电子稳定结构 (4)A与乙的最高价氧化物反应的化学方程式为______________。 |
|
| 17. 实验题 | 详细信息 |
|
氢气和氯气都是重要的化工原料。回答下列问题: (1)利用下图装置制备并收集干燥纯净的氯气。 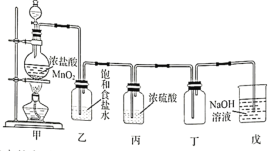 ①装置甲中发生反应的离子方程式为_____________;装置乙的作用是____________; ②某同学提出,戊装置中可能会发生倒吸,建议使用下列装置中的____________(填标号);    (2)利用启普发生器(如图所示)可以便捷地制取氢气。 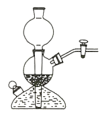 ①使用启普发生器前首先应进行的操作是____________; ②下列装置与启普发生器原理相近的是____________(填标号);  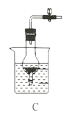 (3)某同学设计了如图装置,在获得盐酸的同时对外提供电能。  ①该装置中的“离子导体”宜选用____________(填标号); A.稀盐酸 B.稀氢氧化钠溶液 C.浓硫酸 D.乙醇 ②写出负极的电极反应式:____________。 |
|
| 18. | 详细信息 |
乳酸( )是葡萄糖无氧呼吸的产物。以乙烯为原料合成乳酸的路线如下: )是葡萄糖无氧呼吸的产物。以乙烯为原料合成乳酸的路线如下:回答下列问题: (1)乳酸含有的官能团为羧基和_________(填名称); (2)反应①的反应类型为_________;反应②的反应类型为_________; (3)反应③的化学方程式为_________; (4)某有机物D含有两个甲基且与乳酸具有相同的官能团,相对分子质量比乳酸大14,则D的结构简式为_________; (5)聚乳酸(PLA)是一种新型可降解的高分子材料,写出聚乳酸的结构简式:_________。 |
|
| 19. | 详细信息 |
铜是生产、生活中常用的金属。工业上利用黄铜矿(有效成分为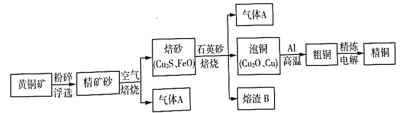 回答下列问题: (1)“粉碎”的目的是____________; (2)A是形成酸雨的主要气体,精矿砂在空气中焙烧发生反应的化学方程式为____________,在反应中每生成 (3)焙烧焙砂时加入适量石英砂的目的是____________; (4)泡铜与Al反应的化学方程式为____________ (5)工业上常用石灰石浆吸收气体A,吸收产物可以作为建筑材料。若使用含碳酸钙2kg的石灰石浆能完全吸收标准状况下 |
|
最近更新



