普洱市高一化学上册期末考试题带答案和解析
| 1. 选择题 | 详细信息 |
|
关于分散系的下列说法中,正确的是( ) A.分散系一定是混合物 B.分散剂一定是液体 C.一种分散系里只有分散质和分散剂两种物质 D.胆矾、空气、有色玻璃都是分散系 |
|
| 2. 选择题 | 详细信息 |
|
在下列反应中氧化剂和还原剂为同一物质的是( ) A.Cl2+H2O==HCl+HClO B.Fe2O3+3CO C.2F2+2H2O==4HF+O2 D.2Na+2H2O==2NaOH+H2↑ |
|
| 3. 选择题 | 详细信息 |
|
下列实验过程中,不会产生气体的是( ) A.  B. B. C. C. D. D. |
|
| 4. 选择题 | 详细信息 |
|
某元素的原子最外层只有一个电子,它跟卤素结合时,生成的化学键 A. 一定是离子键 B. 一定是共价键 C. 两者都有可能 D. 以上说法都不对 |
|
| 5. 选择题 | 详细信息 |
|
下列物质的溶液,能与1 mol·L-1小苏打溶液发生化学反应,既无气体生成也无沉淀生成的是 A.苏打 B.氯化氢 C.熟石灰 D.烧碱 |
|
| 6. 选择题 | 详细信息 |
|
下列电离方程式书写正确的是( ) A.NaOH=Na++O2-+H+ B.FeCl3=Fe3++ C.Ca(NO3)2=Ca2++2(NO3)2- D.H2SO4=2H++ |
|
| 7. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值,下列说法中正确的是( ) A.0.2 mol氧原子中含1.6NA个电子 B.1 mol 氯化镁中含有离子数为NA C.12.4 g白磷中含有磷原子数为0.1NA D.28 g一氧化碳气体所含的电子数为20NA |
|
| 8. 选择题 | 详细信息 |
|
实验室需用480 mL 0.1 mol·L-1的硫酸铜溶液,以下操作正确的是 ( ) A.称取7.68 g硫酸铜,加入480 mL水 B.称取12.5 g胆矾,配成480 mL溶液 C.称取8.0 g硫酸铜,加入500 mL水 D.称取12.5 g胆矾,配成500 mL溶液 |
|
| 9. 选择题 | 详细信息 |
|
下列关于金属铝的叙述中,说法不正确的是 A. 铝的化学性质很活泼,但在空气中不易锈蚀 B. 铝是比较活泼的金属,在化学反应中容易失去电子,表现出还原性 C. 铝箔在空气中受热可以熔化,且发生剧烈燃烧 D. 铝箔在空气中受热可以熔化,但由于氧化膜的存在,熔化的铝并不滴落 |
|
| 10. 选择题 | 详细信息 |
|
现有一氧化碳、二氧化碳、臭氧(O3)三种气体,它们分别都含有1 mol氧原子,则三种气体的分子个数之比为 ( ) A.1∶1∶1 B.1∶2∶3 C.3∶2∶1 D.6∶3∶2 |
|
| 11. 选择题 | 详细信息 |
|
与50 mL 0.1 mol·L-1的Na2CO3溶液中Na+的物质的量相同的溶液是( ) A.50 mL 0.2 mol·L-1的NaCl溶液 B.100 mL 0.2 mol·L-1的NaCl溶液 C.25 mL 0.1 mol·L-1的Na2SO4溶液 D.50 mL 0.1 mol·L-1的NaHCO3溶液 |
|
| 12. 选择题 | 详细信息 |
|
在K2SO4和Fe2(SO4)3的混合溶液中,Fe3+的物质的量浓度为0.1 mol•L﹣1,SO42-的物质的量浓度为0.3 mol•L﹣1,则混合液中K+的物质的量浓度为( ) A. 0.15 mol•L﹣1 B. 0.45 mol•L﹣1 C. 0.3 mol•L﹣1 D. 0.6 mol•L﹣1 |
|
| 13. 选择题 | 详细信息 |
下列各性质中符合图示关系的是 ①化合价 ②ROH的碱性 ③密度 ④最外层电子数 ⑤核外电子层数 ⑥单质失e-能力 A.②④⑤⑥ B.②⑤⑥ C.②③⑤⑥ D.①②③⑤ |
|
| 14. 选择题 | 详细信息 |
|
下列物质中能够导电的电解质是( ) A.铁丝 B.熔融氯化镁 C.氯化钠溶液 D.三氧化硫 |
|
| 15. 选择题 | 详细信息 |
|
把金属钠投入下列溶液中,既有气体放出,又有白色沉淀生成的是 ( ) A.盐酸 B.氯化钠溶液 C.氯化铜溶液 D.氯化镁溶液 |
|
| 16. 选择题 | 详细信息 |
|
下列叙述正确的是 A.两种微粒,若核外电子排布完全相同,则其化学性质一定相同 B.凡单原子形成的离子,一定具有稀有气体元素原子的核外电子排布 C.两原子如果核外电子排布相同,则一定属于同种元素 D.阴离子的核外电子排布一定与上一周期稀有气体原子的核外电子排布相同 |
|
| 17. 选择题 | 详细信息 |
|
据中央电视台报道,近年来我国的一些沿江城市多次出现大雾天气,致使高速公路关闭,航班停飞,雾属于下列哪种分散系( ) A.乳浊液 B.溶液 C.胶体 D.悬浊液 |
|
| 18. 选择题 | 详细信息 |
|
14C常用于测定生物遗骸的年份。下列说法正确的是 A. 14C含有14个中子 B. 14C与14N含有相同的质子数 C. 14C与C60互为同位素 D. 14C与12C是两种不同的核素 |
|
| 19. 选择题 | 详细信息 |
|
下列关于化学键的叙述正确的是( ) A.任何物质里都含有化学键 B.离子化合物中可能含有共价键 C.共价化合物分子中可能含有离子键 D.水分子中氢、氧原子间的化学键是非极性键 |
|
| 20. 选择题 | 详细信息 |
|
能与Fe3+反应且能证明Fe3+具有氧化性的物质是( ) A. 氢氧化钠 B. 硫氰化钾 C. 氯化亚铁 D. 铁 |
|
| 21. 选择题 | 详细信息 |
|
下列关于碱金属铷的叙述中,不正确的是( ) A.碳酸铷易溶于水、易电离 B.在钠、钾、铷三种单质中,铷的熔点最低 C.铷比钠活泼,铷可以从氯化钠溶液中置换出钠 D.氢氧化铷与盐酸反应的离子方程式是H++OH-=== H2O |
|
| 22. 选择题 | 详细信息 |
|
某核素的质量数为37,该核素质子数、中子数和电子数正确的顺序是( ) A. 18、19、19 B. 18、20、18 C. 19、18、20 D. 18、19、18 |
|
| 23. 选择题 | 详细信息 |
|
关于1 mol·L-1K2SO4溶液的下列说法正确的是( ) A.溶液的体积越大,浓度越大 B.含0.1 mol K2SO4的溶液的体积是1 L C.溶液中c(K+)=2 mol·L-1 D.1 L溶液中含2 mol K+,2 mol |
|
| 24. 选择题 | 详细信息 |
|
下列物质沸点递变顺序正确的是( ) A.SnH4>GeH4>SiH4>CH4 B.SbH3>AsH3>PH3>NH3 C.HI>HBr>HCl>HF D.H2Te>H2Se>H2S>H2O |
|
| 25. 实验题 | 详细信息 |
|
已知Fe3O4是一种复杂的化合物,其化学式可改写为FeO·Fe2O3。对于Fe与水蒸气反应后的黑色物质,有三个学习小组提出了三种不同的猜想,以下是小组同学进行的实验猜想与探究,请你根据小组的思路与提示完成相关空白。 实验之前查阅资料得知Fe3+的盐溶液遇到KSCN溶液时,溶液变成红色,而Fe2+遇KSCN溶液无明显变化。 [猜想]甲组:黑色物质是FeO 乙组:黑色物质是Fe3O4 丙组:____________; [实验探究] (1)丙组认为一种简单定性的方法即可判断甲组的正误:取生成的黑色物质少许于烧杯中,加稀盐酸使其完全溶解,再加________溶液以检验Fe3+,观察到溶液有无出现________现象即可判断。 (2)乙组认为可通过定量测定来确定生成的黑色物质的组成,以验证该组猜想正确。取生成的黑色物质2.32 g溶解于适量稀盐酸后,加入新制氯水,加入氯水后反应的离子方程式为__________,再加入足量NaOH溶液后,过滤、洗涤、烘干、灼烧、称量,若称得固体质量为________,即可判断乙组同学猜想正确。 |
|
| 26. 实验题 | 详细信息 |
如图所示是制取无水氯化铜的实验装置图,将浓盐酸滴加到盛有二氧化锰粉末的圆底烧瓶中。请回答下列问题: (1)盛放浓盐酸的仪器名称为__。 (2)烧瓶中发生反应的离子方程式为__。 (3)C瓶中的试剂是__,其作用是__。 (4)玻璃管D中发生反应的化学方程式是__,反应现象是__。 (5)干燥管E中盛有碱石灰(CaO+NaOH),其作用是__。 |
|
| 27. 推断题 | 详细信息 |
|
五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,C和E形成的化合物是日常生活中的常用调味品。回答下列问题: (1)五种元素中,原子半径最大的是________,非金属性最强的是________(填元素符号)。 (2)由A分别和B、D、E所形成的共价型化合物中,热稳定性最差的是__________(用化学式表示)。 (3)A、B、E形成的离子化合物电子式为____________,其中存在的化学键类型为____________。 (4)D最高价氧化物的水化物的化学式为________________。 (5)单质D在充足的单质E中燃烧,反应的化学方程式为__________________;D在不充足的E中燃烧,生成的主要产物的化学式为__________。 (6)单质E与水反应的离子方程式为____________________。 |
|
| 28. 推断题 | 详细信息 |
A、B、C、D、E分别是铁或铁的化合物。其中D是一种红褐色沉淀。其相互反应关系如图所示: 根据如图所示变化,按要求回答下列问题: (1)写出A、E的化学式:A__,E__; (2)写出其中几步反应的化学方程式: C→B:___; B→D:___; E→A:___。 (3)C中加入NaOH溶液,看到的现象是__。 |
|
| 29. 实验题 | 详细信息 |
利用如图装置可以验证非金属性的变化规律。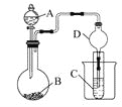 (1)仪器A的名称为________,干燥管D的作用是________________。 (2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为_________________,离子方程式为______。 (3)若要证明非金属性:S>C>Si,则A中加________、B中加Na2CO3、C中加________。 |
|
最近更新



