2019-2020年初三下期期中化学无纸试卷完整版(黑龙江省大庆市萨尔图区大庆市二十三中)
| 1. 选择题 | 详细信息 |
|
2020年春节前后武汉新冠肺炎疫情牵动着全国人民的心,在春节这个原本欢庆的时间里,大家都在努力对抗病毒。为阻断疫情传播,下列防疫措施中,发生化学变化的是( ) A.  测量体温 B. 测量体温 B. 穿防护服 穿防护服C.  酒精消毒 D. 酒精消毒 D. 流水洗手 流水洗手 |
|
| 2. 选择题 | 详细信息 | ||||||||
下表中对部分知识的归纳完全正确的一组是
|
|||||||||
| 3. 选择题 | 详细信息 |
|
下列应用和相应原理(用化学方程式表示)及基本反应类型都正确的是 ( ) A.用烧碱溶液吸收二氧化硫 2NaOH + SO2 =Na2SO4 +2 H2O 复分解反应 B.测定空气中氧气含量 P +5O2 C.实验室用过氧化氢溶液制氧气 2H2O2 D.用氢氧化铝治疗胃酸过多 3H2SO4+2Al(OH)3=A12(SO4)3+3H2O 置换反应 |
|
| 4. 选择题 | 详细信息 |
|
推理是学习化学时常用的思维方式,以下推理结果正确的是( ) A. 用洗洁精洗油污是乳化作用,用汽油洗油污也是乳化作用 B. NaOH溶液能使无色酚酞试液变红色,Cu(OH)2也能使无色酚酞试液变红色 C. 化合物是由不同种元素组成的纯净物,则只含一种元素的物质一定不是化合物 D. 复分解反应有沉淀、气体或水生成,有沉淀、气体或水生成的反应是复分解反应 |
|
| 5. 选择题 | 详细信息 |
碳酸钠(俗名纯碱)是生活中的重要物质。我国化学家侯德榜发明了联合制碱法(又称氨碱法),生产纯碱的主要反应原理如下:NaCl+NH3+CO2+H2O═NaHCO3↓+NH4Cl;2NaHCO3 A.加热时的稳定性:碳酸钠>碳酸氢钠 B.用食盐制纯碱还需要含碳、氧元素的物质 C.配制饱和食盐水时,可通过搅拌来提高食盐的溶解度 D.向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收 |
|
| 6. 选择题 | 详细信息 |
KNO3和NH4Cl的溶解度曲线如图1所示。某化学兴趣小组的同学进行了如图2所示实验,R是KNO3或NH4Cl中的一种。关于下图中烧杯内的物质,下列说法正确的是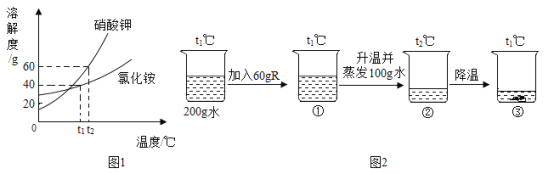 A. R是NH4Cl B. 烧杯①溶液的溶质质量分数小于烧杯③ C. 若使烧杯③中的固体溶解,只能采用加水的方法 D. 烧杯①、②、③中,只有烧杯③中上层清液是饱和溶液 |
|
| 7. 选择题 | 详细信息 |
下列四个图像中,能正确反映对应变化关系的是 ( )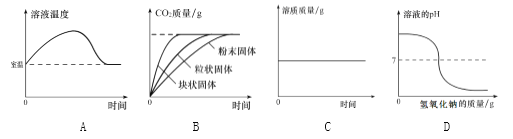 A. 硝酸铵溶于水时溶液的温度变化 B. 等质量碳酸钙与足量同浓度稀盐酸反应 C. 将浓硫酸加水稀释成稀硫酸 D. 向稀盐酸中不断滴加氢氧化钠溶液 |
|
| 8. 选择题 | 详细信息 |
|
某金属粉末可能由镁、锌、铁、铝、银中的一种或几种组成。取该样品2.4g,向其中加入100g一定溶质质量分数的稀硫酸,恰好完全反应,生成0.2g氢气,得到无色溶液,固体无剩余。下列说法正确的是 A.样品中一定不含有银,可能含有铁 B.样品中一定含有镁 C.所得溶液中溶质总质量为12g D.加入的稀硫酸的溶质质量分数为19.6% |
|
| 9. 选择题 | 详细信息 |
实验室有一包白色固体,其中除了碳酸钠以外,还可能含有硝酸钡、硫酸钠、氢氧化钠中的一种或几种。为确定其组成进行如下实验:①取少量白色固体于烧杯中,向烧杯中加入足量水并不断搅拌,固体部分溶解;②继续向烧杯中逐滴加入足量稀硝酸并不断搅拌,此时固体质量变化如图。下列说法正确的是( ) A.A→B段对应的实验现象是固体部分溶解,无气泡冒出 B.B→C段对应溶液pH逐渐变大 C.原白色固体中一定含有碳酸钠、硫酸钠、硝酸钡 D.C点对应溶液中一定含有的溶质是硝酸、硝酸钠、碳酸钠、硝酸钡 |
|
| 10. 填空题 | 详细信息 |
|
社会在进步,我们的生活进入了新时代,请从化学的视角回答下列生活中的相关问题: (1)网购已成为人们生活的一部分,小刚通过“美团”网站订购了外卖套餐:红烧排骨、西红柿鸡蛋、米饭,其中富含糖类的食物是_____。 (2)常食用黑木耳、绿叶蔬菜可补充人体所需的铁元素,铁元素摄入不足可能会引起的疾病是_____症。 (3)饮用水的质量越来越被人们所关注,目前市场上出售的净水器中的活性炭主要起_____作用。 (4)“中国高铁”已成为我国的一张新名片,其车身主要采用的镍铬奥氏体不锈钢属于_____(填序号) A无机非金属材料 B金属材料 C有机合成材料 D复合材料 |
|
| 11. 填空题 | 详细信息 |
|
钙元素是构成人体的重要组成部分,钠、锌等元素对人体健康也有着重要作用。 (1)少儿患佝偻病和发育不良,老年人得骨质疏松症是因为体内缺_____(填元素符号)。 (2)上述三种元素中,属于微量元素的是_____(填元素符号);对维持人体内的水分和维持体液pH的恒定起重要作用的是_____(填离子符号)。 |
|
| 12. 填空题 | 详细信息 |
|
铬(Cr)是一种重要的金属元素,铬的单质及其化合物应用广泛。 (1)重铬酸钾(K2Cr2O7)可用于测试酒驾,则重铬酸钾中铬元素的化合价为_____。 (2)铬桶可以盛装AlCl3溶液,不能盛装稀硫酸,则金属活动性,Cr_____Al(填“>”“<”)。 根据上述信息,不能证明Zn和Cr的活动性强弱的试剂组是_____。 A Zn、Cr和稀硫酸 B Cr、ZnSO4溶液 C Cu、ZnSO4溶液、CrSO4溶液 (3)Cr2(SO4)3为有毒的重金属盐,可用KOH溶液将其转化为沉淀而除去,该转化的化学方程式为_____。 |
|
| 13. 推断题 | 详细信息 |
|
推理和判断是学习化学的重要方法。 A、B、C为初中化学常见的三种物质,它们之间的转化关系如图所示(“→”表示某一种物质经一步反应可转化为另一种物质,部分反应物、生成物的反应条件已略去)请回答下列问题: 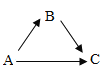 (1)若A、B、C均含有同一种元素,B、C组成元素相同,C的固体俗称“干冰”,则B的化学式是______________。 (2)若A、B、C是含相同金属元素的化合物,B、C的水溶液为蓝色,三种物质相互间发生的反应均为复分解反应,则A的化学式可能是____________(合理即可得分)。 (3)若A、B、C均为碱,其中B易溶于水,C难溶于水,写出一个由B转化为C的化学方程式_____________(合理即可得分)。 |
|
| 14. 填空题 | 详细信息 |
只含一种杂质的硫酸溶液M,加足量的氢氧化钡溶液后,再加足量的稀盐酸,过程如图所示。下列判断合理的有_____(填序号)。 ①M中一定不含有碳酸钠 ②图中ab间(不含a、b两点)滴入酚酞溶液变红色 ③bc段表示沉淀部分消失,无气泡产生 ④c点后溶液中的溶质不少于两种 |
|
| 15. 科学探究题 | 详细信息 |
某化学活动小组,在实验室中进行了如图所示的实验: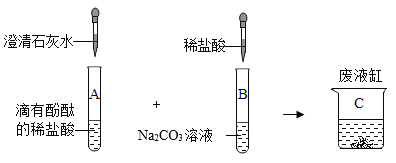 (实验探究)实验时B中观察到了明显的实验现象,则该现象是____________;实验后,小组同学将试管A的红色废液和试管B中的无色废液都倒入废液缸C中,充分振荡后,观察到废液缸C中产生了白色沉淀。废液缸中产生的沉淀的化学式为___________; 由此可推知试管B中废液的溶质是_____________;然后又对C滤液中所含有的离子产生了浓厚的兴趣(不考虑酚酞)。 (提出问题)滤液C中含有哪些离子? (猜想与假设)小明同学:Na+ 、Cl-、Ca2+、 (评价与交流)同学们认为小明的猜想不正确,因为_____________(离子符号)在溶液中能发生反应,不能共存; (探究与分析)小亮同学为了证明自己的猜想,取滤液少许于试管中,然后滴加稀盐酸至过量,分析实验数据绘制如图所示图像,证明了自己的猜想正确。请结合图像说出小亮同学的理由是____________;  (讨论与总结)通过上述探究过程,同学们总结出:在溶液中__________的离子不能共存。 |
|
| 16. 实验探究题 | 详细信息 |
实验室常用块状大理石和稀盐酸反应制取CO2气体。某大理石中因含少量硫化物,使制得的CO2中混有H2S气体。某化学兴趣小组的同学欲用下图装置制取一瓶纯净、干燥的CO2,请回答下列问题: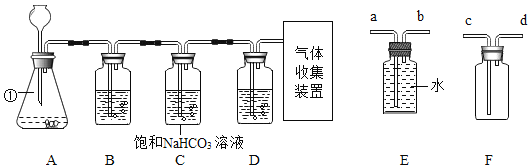 (1)仪器①的名称是____________; (2)写出实验室制取二氧化碳的化学方程式_____________;找出装置A~D中的一处错误并加以改正:______________,利用改正后的装置完成后面的实验; (3)实验室制取的CO2中往往混有少量的HCl气体,其可能原因是______________;混有的HCl气体可用饱和NaHCO3溶液吸收化学方程式为_____________。 (4)小组同学查阅资料得知:H2S能与氢氧化钠溶液、硫酸铜溶液反应。欲除去CO2中混有H2S气体,B装置中所盛试剂应选用________(填“氢氧化钠”或“硫酸铜”)溶液,D装置的作用是____________; (5)用多功能瓶收集CO2的装置应选用________(填“E”或“F”),气体应从________(填“a”、“b”、“c”或“d”)端导管口通入。 |
|
| 17. 科学探究题 | 详细信息 | ||||||||||||||||||||||||
|
“五一”假期,聪聪同学和家人到安徽省博物馆去参观,发现博物馆内许多铜制品表面有一层绿色物质。绿色物质是什么?它是怎样形成的?化学活动课上,同学们设计实验对这种绿色物质进行了如下探究活动。 (査阅资料) ①铜在空气中易生成铜锈,它为绿色,其主要成分是Cu2(OH)2CO3; ②白色的硫酸铜粉末遇水能变为蓝色。 探究活动一:验证铜锈的组成。 (进行实验1) 同学们设计了如图所示装置并进行实验。 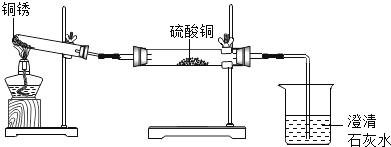
|
|||||||||||||||||||||||||
| 18. 科学探究题 | 详细信息 | ||||||||||||
|
过氧化钙(CaO2)是一种环境友好型供氧剂,可用于鱼类养殖、农作物栽培等,实验室有一瓶放置一段时间的过氧化钙样品,某兴趣小组对其成分展开了如下探究。 (查阅资料)CaO2能与水反应最终生成Ca(OH)2和O2;也能与CO2反应得到CaCO3和O2.过氧化氢溶液具有漂白性。 (提出问题)该固体样品的成分是什么? (猜想假设)可能是CaO2、Ca(OH)2、CaCO3中的一种或几种。 (实验探究)
|
|||||||||||||
| 19. 计算题 | 详细信息 |
江西省积极落实化肥减量增效示范项目,并对在售的化肥提出明确的质量要求。某兴趣小组对市售的某钾肥进行了检测,称取5.0g样品放入烧杯中,加入适量的水溶解后,逐滴加入13%的BaCl2溶液产生沉淀的质量与所加入BaCl2溶液质量的关系如图所示(假定杂质不参加反应)。已知K2SO4+BaCl2=BaSO4↓+2KCl。 (1)恰好反应时,所用BaCl2溶液中所含溶质的质量为_____g。 (2)通过计算判断该钾肥中K2SO4的质量分数是否符合如图的包装说明_____?(写出计算过程) (3)加入6gBaCl2溶液时溶液中K+和Cl﹣的个数比为_____。 |
|