九年级上半年期末化学题带答案和解析(2017-2018年湖南省株洲市茶陵县)
| 1. 选择题 | 详细信息 |
|
下列变化中,属于物理变化的是( ) A. 动物呼吸 B. 光合作用 C. 铜丝拉直 D. 钢铁生锈 |
|
| 2. 选择题 | 详细信息 |
|
下图所示的化学实验基本操作中,正确的是 A.  倾倒液体 B. 倾倒液体 B.  称量固体 称量固体C.  检查气密性 D. 检查气密性 D.  加热液体 加热液体 |
|
| 3. 选择题 | 详细信息 |
|
下列物质中,属于混合物的是( ) A.冰水 B.干冰 C.液氧 D.溶液 |
|
| 4. 选择题 | 详细信息 |
|
日常生活中用铁锅炒菜可适当地给人体补“铁”,这里的“铁”指的是 A、离子 B、原子 C、元素 D、分子 |
|
| 5. 选择题 | 详细信息 |
工业酒精中含有少量的甲醇,甲醇有剧毒,不能食用,其分子结构用如图所示的模型表示。下列有关甲醇的叙述中错误的是( )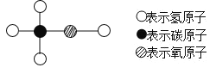 A. 甲醇的化学式为CH4O B. 甲醇中C、H、O三种元素的质量比为1:4:1 C. 甲醇的相对分子质量为32 D. 甲醇中氧元素的质量分数为50% |
|
| 6. 选择题 | 详细信息 | |||||||||||||||
下列对一些事实的解释错误的是( )
|
||||||||||||||||
| 7. 选择题 | 详细信息 |
|
要使已被接近饱和的硝酸铵溶液变为饱和溶液,下列方法中不正确的是( ) A.倒出少量溶剂 B.投入硝酸铵 C.蒸发部分水 D.适当降温 |
|
| 8. 选择题 | 详细信息 |
|
饮料中的果味大多来自酯类。丁酸乙酯(C6H12O2)是无色具有菠萝香味的液体,常用作食品、饮料的调香剂。下列叙述中,正确的是( ) A.丁酸乙酯是由20个原子构成的 B.丁酸乙酯的相对分子质量为116g C.丁酸乙酯中碳、氢、氧元素的质量比为18:3:8 D.一个丁酸乙酯分子中,碳、氢、氧原予的个数比为3:6:2 |
|
| 9. 选择题 | 详细信息 |
|
X、Y、Z三种金属及其化合物间可发生如下化学反应:Y+ZCl2=Z+YCl2 X+ZCl2=Z+XCl2 Y+2HCl=YCl2+H2↑ X+HCl不反应则X、Y、Z三种金属的活动性由强到弱的顺序是( ) A.Z>Y>X B.X>Y>Z C.Y>X>Z D.Y>Z>X |
|
| 10. 选择题 | 详细信息 |
|
已知铁原子的相对原子质量为56,铁原子核内有26个质子,该种铁原子的原子核内的中子数目为( ) A.82个 B.30个 C.26个 D.52个 |
|
| 11. 选择题 | 详细信息 |
|
下列化学反应中,属于置换反应的是( ) A.4P+5O2 C.CaCO3 |
|
| 12. 选择题 | 详细信息 |
|
下列坐标图分别表示实验过程中某些量的变化,其中正确的是( ) A.一定温度下,向硝酸钾溶液中加入硝酸钾固体  B.将水通电一段时间  C.将等质量的镁片和铁片投入到足量的稀H2SO4中  D.用等质量、等浓度的过氧化氢溶液分别制取氧气 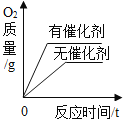 |
|
| 13. 选择题 | 详细信息 | |||||||||||||||
下列依据实验目的所设计的实验操作中,正确的是( )
|
||||||||||||||||
| 14. 选择题 | 详细信息 |
|
下列探究实验设计不能达到目的是( ) A.探究燃烧的条件  B.探究水的组成 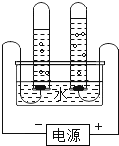 C.探究铁、铜的金属活动强弱  D.探究化学发应是否遵循质量守恒定律 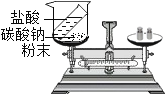 |
|
| 15. 选择题 | 详细信息 |
|
用氯化钠配制100g溶质质量分数为0.9%的生理盐水,现有下列操作:①溶解;②称取氯化钠固体;③过滤;④量取蒸馏水;⑤计算。正确的操作顺序是( ) A.①②③④ B.⑤②④① C.⑤①②④ D.③②④① |
|
| 16. 选择题 | 详细信息 |
|
推理是学习化学的一种重要方法,下列推理关系成立的是( ) A. MnO2是加快H2O2分解的催化剂,所以催化剂是加快化学反应速率的物质 B. 水电解产生氢气和氧气,所以水是由氢气和氧气组成的 C. 空气中可燃物燃烧必须与氧气接触,所以把可燃物与氧气隔绝是灭火的有效方法之一 D. 镁条在空气中燃烧得到的氧化镁的质量与参加反应的镁条质量不同,故该反应不符合质量守恒定律 |
|
| 17. 选择题 | 详细信息 | |||||||||||||||
在一只密闭容器内有四种物质,在一定条件下充分反应,测得反应前后各物质的质量如下表:
|
||||||||||||||||
| 18. 填空题 | 详细信息 |
|
请用化学用语填空: (1)2个铝离子_____; (2)镁在空气中燃烧生成的主要氧化物_____; (3)3个水分子_____; (4)由70个碳原子构成的单质分子_____。 |
|
| 19. 填空题 | 详细信息 |
|
(1)秋冬之交,我们北方地区频现雾霾天气,雾霾中含有大量的PM2.5颗粒物导致呼吸病人增多,为了减少空气污染,下列措施不正确的是_____。 A 鼓励市民出行乘坐公交少开私家车 B 开发新能源,如:太阳能 C 将垃圾收集起来焚烧 D 火力发电厂排放的废气必须处理达标后排放 (2)下列图标中,属于消防安全标志的是_____。  (3)将煤块制成蜂窝煤后燃烧,其目的是_____。 (4)使用乙醇汽油是一种“节能减排”的有效措施。下列关于乙醇作燃料的说法不正确的是_____(填选序号)。 A 乙醇属于可再生能源 B 乙醇汽油不能用作汽车燃料 C 使用乙醇汽油可减少大气污染 D 使用乙醇汽油可节省石油资源 |
|
| 20. 填空题 | 详细信息 |
锶元素的粒子结构示意图和在元素周期表中显示的信息如图所示: (1)锶属于_____元素(填“金属”或“非金属”)。 (2)锶元素的原子序数为_____。 (3)图2所表示的粒子的化学符号是_____,锶元素和氯元素形成化合物的化学式是_____ |
|
| 21. 填空题 | 详细信息 |
|
(1)已知在有机物中,氢元素通常为+1价,氧元素通常为-2价。草酸(H2C2O4)是一种有机物,其中碳元素的化合价为_____价; (2)有些含氧化合物可写成氧化物的形式,如Na2SiO3(硅酸钠)可写成Na2O·SiO2,H2SO4可写成SO3·H2O,根据这种方法,CaCO3可写成_____。 |
|
| 22. 填空题 | 详细信息 |
下图是A、B、C三种物质的溶解度曲线,据图回答: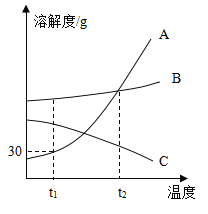 (1)t1℃时A、B、C三种物质的溶解度由大到小的顺序是_____(填写序号,下同)。 (2)t1℃时30gA物质加入到50g水中不断搅拌,形成的溶液质量是_____g,该溶液是_____(填“饱和”或“不饱和”) (3)将t1℃时A、B、C三种物质饱和溶液的温度升高到t2℃时,三种溶液的溶质质量分数由大小关系是_____。 |
|
| 23. 填空题 | 详细信息 |
|
我国古代将炉甘石(ZnCO3)、赤铜(Cu2O)和木炭粉混合后加热到约800℃,得到一种外观似金子的锌和铜的合金,有关反应可用3个化学方程式表示: (1)ZnCO3 (2)_____; (3)_____。 |
|
| 24. 简答题 | 详细信息 |
|
请用所学的知识回答下列问题: (1)洗涤剂能去油污,汽油也能去油污,二者去油污的原理相同吗?为什么? (2)铝是比较活泼的金属,为什么铝制品的抗腐蚀性能却很强? |
|
| 25. 推断题 | 详细信息 |
已知:A是红色粉末,B、C是氧化物,D、I是常见金属,H是浅绿色溶液,G为单质,具有可燃性。它们之间的转化关系如下: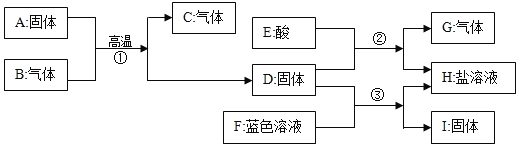 请回答: (1)写出下列物质的化学式:A_____ C_____ 、G_____ 。 (2)上述转化①②③中,属于置换反应的有_____(填序号)。 (3)向D和I的混合物中,加入稀硫酸,写出有关反应的化学方程式_____。 |
|
| 26. 实验探究题 | 详细信息 |
现有下列实验装置图,结合该图回答下列问题: (1)写出图中标号仪器的名称:①_____;②_____。 (2)实验室选用A装置来制取氧气,发生反应的化学方程式为_____,能用D装置收集氧气的原因是_____。 (3)实验室制取二氧化碳,若用F装置来收集,验满时应将燃着的木条放在_____(填“a”或“b”)端管口;检验二氧化碳的化学方程式为_____。 (4)实验室在常温下用块状电石与水反应制取不易溶于水的乙炔(C2H2)气体,该反应必须严格控制加水速度,以免剧烈反应放热引起发生装置炸裂。要制取较纯净的乙炔气体,你认为图中最适合的发生和收集装置为_____(填序号)乙炔是一种可燃性气体,点燃前要_____。 |
|
| 27. 科学探究题 | 详细信息 |
|
为了延缓蛋糕等食品的氧化,生产厂家在包装袋中加入了一种除氧剂。该除氧剂是一种或两种常见单质的粉末状固体,未变质时呈黑色,失效后带有红棕色。某化学课外兴趣小组为了确定该除氧剂的主要成分,进行了如下探究。 提出问题: 假设①:该除氧剂的主要成分是活性炭; 假设②:该除氧剂的主要成分是铁粉; 假设③:该除氧剂的主要成分是活性炭和铁粉的混合物。 设计并进行实验: 将一包未变质的除氧剂分成两份,一份加入到氯化铜溶液中,一段时间后溶液颜色变成浅绿色且出现紫红色固体,说明假设_____一定是不正确的;另一份加入到足量的稀盐酸中,发现产生大量气泡且一段时间后没有固体剩余,说明假设_____是正确的。 反思与评价: (1)为了验证该除氧剂是否含有铁粉,可以采用的一种物理方法是_____; (2)下列有关说法正确的有_____(填字母)。 A 凡是能与氧气反应的固体物质均可作为食品的除氧剂 B 该除氧剂可用于牛奶、果汁等饮料的保鲜 C 米饭、蛋糕等食品的腐败变质属于缓慢氧化 D 一些食品中放小包装袋的氧化钙,主要是利用其能吸收空气中的氧气 拓展: (1)若某除氧剂主要成分为铁粉,由于铁与氧气、水蒸气反应生成铁锈(用Fe2O3·3H2O表示),从而达到吸收包装袋中的氧气、延长食品保质期的目的。 ①生成铁锈的化学方程式为_____。 ②已知该除氧剂含铁粉的质量为2.8 g,则该除氧剂最多能够吸收氧气_____g。 (2)日常使用的铁制品容易发生锈蚀。请说出一种防止铁制品锈蚀的方法:_____。 |
|
| 28. 计算题 | 详细信息 |
|
据有关专家介绍,用醋酸(CH3COOH)蒸气对空气进行消毒可以有效地预防流感。请计算: (1)醋酸的相对分子质量为_____。 (2)30g的醋酸中含氧元素的质量为_____g。 |
|
| 29. 计算题 | 详细信息 | ||||||||||||
为测定石灰石中碳酸钙的纯度,取石灰石样品与足量的稀盐酸在烧杯中反应(杂质不反应也不溶于水),有关数据如表。
|
|||||||||||||
最近更新



