新疆2019年高一化学上册高考模拟免费检测试卷
| 1. 选择题 | 详细信息 |
|
下列实验操作中正确的是( ) A. 蒸发操作时,应使混合物中的水分完全蒸干后才能停止加热 B. 蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶支管口处 C. 分液操作时,分液漏斗中下层液体从下口放出后,再将上层液体从下口放出到另一个烧杯 D. 萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
|
| 2. 选择题 | 详细信息 |
|
为了除去粗盐中的 Ca2+、Mg2+、SO42-及泥沙,可将粗盐溶于水,然后进行下列五项操作,其中正确的操作顺序是 ①过滤 ②加过量NaOH溶液 ③加适量盐酸 ④加过量 Na2CO3溶液 ⑤加过量 BaCl2溶液 A. ①④②⑤③ B. ④①②⑤③ C. ②④⑤①③ D. ⑤②④①③ |
|
| 3. 选择题 | 详细信息 |
|
下列离子检验的方法正确的是 A. 某溶液 B. 某溶液 C. 某溶液 D. 某溶液 |
|
| 4. 选择题 | 详细信息 |
|
下列各组数据中,前者刚好是后者两倍的是 A. 2 mol水的摩尔质量和1 mol水的摩尔质量 B. 200 mL 1 mol·L-1氯化钙溶液中c(Cl-)和100 mL 2 mol·L-1氯化钾溶液中c(Cl-) C. 标准状况下,22.4 L一氧化碳中氧原子数和16 g二氧化硫中氧原子数 D. 2 mol·L-1H2SO4溶液中的H+个数与1 mol·L-1HCl溶液中的H+个数 |
|
| 5. 选择题 | 详细信息 |
|
下列溶液这氯离子(Cl-)的物质的量浓度最大的是 A. 200mL 0.5mol/L NaCl溶液 B. 100mL 0.5mol/L MgCl2溶液 C. 50mL 0.5mol/L AlCl3溶液 D. 150mL 1mol/L NaCl溶液 |
|
| 6. 选择题 | 详细信息 |
|
同温同压下相同体积的任何气体中含有的分子数相同。在一定温度和压强下,50 mL A2气体与75 mL B2气体恰好化合生成50 mL某气体化合物,则该化合物的化学式为( ) A. AB2 B. AB C. A3B D. A2B3 |
|
| 7. 选择题 | 详细信息 |
|
某风景区被称为天然氧吧,其原因是空气中的自由电子附着在分子或原子上形成空气负离子,被称为“空气维生素”。下列关于1mol O2—的说法正确的是 ( ) A. 摩尔质量为64g B. 含16 mol质子 C. 含有1 mol电子 D. 最外层有8mol电子 |
|
| 8. 选择题 | 详细信息 |
|
50g密度为ρg·cm-3的CaCl2溶液里含2gCa2+,从中再取出一半的溶液中Cl-的浓度是 A. |
|
| 9. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数,下列说法正确的是 ①标准状况下,11.2 L以任意比例混合的氮气和氧气所含的原子数为NA ②同温同压下,体积相同的氢气和氩气所含的分子数相等 ③1 L 2 mol·L-1的AlCl3溶液中含氯离子为6NA ④22.4 L H2分子数为NA ⑤32 g O2和O3混合气体中含有原子数为2NA A. ①②③⑤ B. ①②③④ C. ①③④ D. ③④ |
|
| 10. 选择题 | 详细信息 |
|
下列各物质所含原子数由多到少的顺序是 ①24 g石墨 ②0.7 mol NH3 ③4.6 g钠 ④0.2 mol H2SO4 ⑤4 g 氦气 A. ②①④⑤③ B. ①③②④⑤ C. ②④①⑤③ D. ④⑤②①③ |
|
| 11. 选择题 | 详细信息 |
|
用10mL的0.1mol·L-1BaCl2 溶液恰好都可使相同体积的硫酸铁、硫酸锌和硫酸钾三种溶液中的硫酸根离子完全转化为硫酸钡沉淀,则三种硫酸盐溶液的物质的量浓度之比是( ) A. 3:2:2 B. 1:2:3 C. 1:3:3 D. 3:1:1 |
|
| 12. 选择题 | 详细信息 |
|
下列有关阿伏加德罗常数(NA)的说法正确的是( ) A. 常温常压下11.2LCO所含的原子数目为NA个 B. 16g O2和O3中含有的原子数目为NA C. 任何条件下0.5mol氮气分子的分子数不一定是0.5 NA D. 标准状况下1molCCl4含有的氯离子数目为4NA个 |
|
| 13. 计算题 | 详细信息 |
|
(1)已知8 g A能与32 g B恰好完全反应,生成22 g C和一定量的D;现将16 g A与70 g B混合,充分反应后,生成2 mol D和一定量的C,则D的摩尔质量为__________。 (2) 标准状况下,0.5molH2和 O2的混合气体所占的体积为________。 (3)8.5 g氢氧根离子含有的电子数目为________。 (4)14 g C2H4与C4H8的混合物所含质子的物质的量为________。 (5)将4gNaOH溶于__________g水中,可使溶液中H2O与Na+的物质的量之比等于20:1,若测得该溶液的密度为1.1g/cm3,则该溶液中c(Na+)为__________。 |
|
| 14. 实验题 | 详细信息 |
海洋植物如海带、海藻中含有大量的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如图: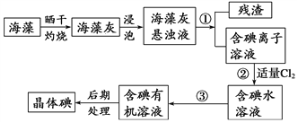 (1)提取碘的过程中有关的实验操作名称:①_______________,③_______________。 (2)提取碘的过程中,不能选择乙醇作有机萃取剂的原因是_____________________。 (3)第③步时使用的主要玻璃仪器有_______________________。 (4)小组用CCl4萃取碘水中的碘,在图中,下层液体呈______色;他们打开仪器下端的活塞,却未见液体流下,原因可能是_________________。  |
|
| 15. 实验题 | 详细信息 |
掌握仪器名称、组装及使用方法是中学化学实验的基础,下图为两套实验装置。   (1)写出下列仪器的名称:a.____________,b.___________,c.__________。 (2)仪器a~e中,使用前必须检查是否漏水的有___________。(填序号) (3)若利用装置分离四氯化碳和酒精的混合物,还缺少的仪器是__________,将仪器补充完整后进行实验,温度计水银球的位置在_______处。冷凝水由____口流出(填f或g)。 (4)现需配制0.1mol/LNaOH溶液450mL,装置是某同学转移溶液的示意图。 ①图中的错误是_____________________________。 ②根据计算得知,所需NaOH的质量为_______。 ③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次)_____________。 A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶 B.准确称取计算量的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解 C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中 D.将容量瓶盖紧,振荡,摇匀 E.改用胶头滴管加水,使溶液凹面恰好与刻度相切 F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处 (5)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)。若没有进行A操作___________;容量瓶用蒸馏洗涤后残留有少量的水_____________;若定容时俯视刻度线__________。 |
|
最近更新



