2019届高三下半期复习诊断化学(河南省许昌高级中学)
| 1. 选择题 | 详细信息 |
|
2018年“地球一小时“活动号召公众开启绿色行为方式。下列做法不符合绿色行为方式的是 A. 优先选择私家车出行 B. 理性购物,适度点餐不浪费 C. 购物自带环保袋,少用塑料包装 D. 垃圾尽量分类,电子设备以旧换新 |
|
| 2. 选择题 | 详细信息 |
|
宋应星所著《天工开物》被外国学者警为“17世纪中国工艺百科全书”。下列说法不正确的是 A. “凡白土曰垩土,为陶家精美启用”中“陶”是一种传统硅酸盐材料 B. “每红铜六斤,入倭铅四斤,先后入罐熔化,冷定取出,即成黄铜“中的黄铜是合金 C. “烧铁器淬于胆矾水中,即成铜色也”该过程中反应的类型为置换反应 D. “凡火药,硫为纯阳,硝为纯阴”中“硫”指的是硫黄,“硝”指的是硝酸 |
|
| 3. 选择题 | 详细信息 |
|
下列有关实验装置进行的相应实验,能达到目的的是( ) A. 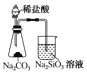 证明非金属性Cl>C>Si B. 证明非金属性Cl>C>Si B. 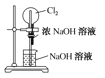 “喷泉”实验 “喷泉”实验C.  制取并收集干燥纯净的NH3 D. 制取并收集干燥纯净的NH3 D.  探究SO2的还原性和漂白性 探究SO2的还原性和漂白性 |
|
| 4. 选择题 | 详细信息 |
a、b、c的结构如图所示,下列说法正确的是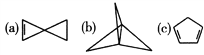 A. a中所有碳原子处于同一平面 B. b的二氯代物有三种 C. a、b、c三种物质均可与溴的四氯化碳溶液反应 D. a、b、c互为同分异构体 |
|
| 5. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数值下列有关叙述正确的是 A. 常温常压下, 30 g乙烷中所含的极性共价键数为6NA B. 0.1mol Fe与足量盐酸反应,转移的电子数为0.3NA C. 0.1 mol D. 0.1mol·L-1的NH4NO3溶液中含有的氮原子数为0.2NA |
|
| 6. 选择题 | 详细信息 |
|
已知短周期主族元素X、Y、Z、W、R,其中X的原子半径在短周期主族元素中最大,Y元素的原子最外层电子数为m,次外层电子数为n,Z元素的原子L层电子数为m+n,M层电子数为m-n,W与Z同主族,R元素原子与Y元素原子的核外电子数之比为2:1。下列叙述错误的是 A. X与Y形成的两种化合物中阴、阳离子的个数比均为1:2 B. Y的氢化物比R的氢化物稳定,且熔沸点高 C. RY2和WY2通入Ba(NO3)2溶液中均不产生白色沉淀 D. RY2和X2Y2均具有漂白性,均能使品红试液褪色 |
|
| 7. 选择题 | 详细信息 |
“84”消毒液(有效成分为NaClO)可用于消毒和漂白,下列实验现象的分析,不正确的是 ( )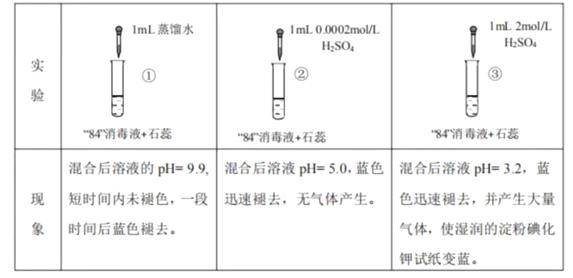 A. 对比实验①和②,②中蓝色迅速褪去的原因是发生了反应ClO−+H+ ===HClO B. 实验③中产生的气体是Cl2,由HClO分解得到:2HClO===Cl2↑+H2O C. 对比实验②和③,溶液的pH可能会影响ClO− 的氧化性或Cl− 的还原性 D. 加酸可以提高“84”消毒液的漂白效果,但需要调控合适的pH才能安全使用 |
|
| 8. 选择题 | 详细信息 |
|
下列离子方程式正确的是 ( ) A. H2S气体通入FeCl3溶液中: Fe3++H2S=Fe2++S↓+2 H+ B. 5.6g Fe与200mL2.0mol/L HNO3溶液充分反应:3Fe + 2NO3— + 8H+ = 3Fe2+ + 2NO↑ + 4H2O C. 往明矾溶液中加入氢氧化钡溶液至Al3+完全沉淀: A13++2SO42-+2Ba2++3OH-=A1(0H)3↓+2BaSO4 D. 饱和碳酸钠溶液通入二氧化碳后溶液变浑浊: 2Na++CO32-+CO2+H2O=2NaHCO3↓ |
|
| 9. 选择题 | 详细信息 |
|
己知 Cu2O能与硝酸反应,方程式为:3Cu2O+14HNO3=6Cu(NO3)2+2NO↑+7H2O,若生成NO的体积为0.448 L (标准状况下),下列说法正确的是 A. 被氧化的Cu2O为1.44g B. 作氧化剂的硝酸为0.14 mol C. 至少需0.5 moI/L硝酸140 mL与Cu2O反应 D. 转移的电子总数为0.06 Na |
|
| 10. 选择题 | 详细信息 |
氧化铅( PbO)是黄色固体。实验室用草酸在浓硫酸作用下分解制备CO,其原理为H2C2O4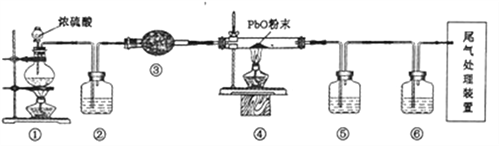 A. 装置②③⑤⑥中的试剂依次为氢氧化钠溶液、碱石灰、银氨溶液、澄清石灰水 B. 实验时,先点燃①处酒精灯,等装置⑥中有明显现象且有连续气泡后再点燃④处酒精灯 C. 实验完毕时,先熄灭①处酒精灯,再熄灭④处酒精灯 D. 尾气处理装置可选用盛NaOH 溶液的洗气瓶 |
|
| 11. 选择题 | 详细信息 |
我国化学家侯德榜根据NaHCO3溶解度比NaCl、Na2CO3、NH4HCO3、NH4Cl都小的性质,运用CO2+NH3+H2O+NaCl=NaHCO3↓+NH4Cl的反应原理制备纯碱.下面是在实验室进行模拟实验的生产流程示意图: 则下列叙述错误的是( ) A. A气体是NH3,B气体是CO2 B. 把纯碱及第Ⅲ步得到的晶体与某些固体酸性物质(如酒石酸)混合可制得发酵粉 C. 纯碱可广泛地用于玻璃、制皂、造纸、纺织等工业中 D. 第Ⅳ步操作是将晶体溶于水后加热、蒸发、结晶 |
|
| 12. 选择题 | 详细信息 |
根据下列各图曲线表征的信息。得出的结论正确的是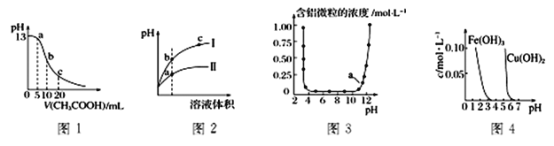 A. 图1表示常温下向体积为10mL0.1 mol•L-1NaOH溶液中逐滴加入0.1 mol•L-1CH3COOH溶液后溶液的pH变化曲线,则b点处有:c(CH3COOH)+c(H+)=c(OH-) B. 图2表示用水稀释pH相同的盐酸和NH4C1溶液时。溶液的pH变化曲线,其中Ⅰ表示盐酸,Ⅱ表示NH4C1溶液,且溶液导电性:b>c>a C. 图3表示的是Al3+与OH-反应时含铝微粒浓度变化曲线,图中a点溶液中大量存在Al3+ D. 由图4得出若除去Fe2(SO4)3溶液中的Cu2+,可采用向溶液中加入适量Fe2O3,调节溶液的pH 至4左右 |
|
| 13. 选择题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||||||||
探究2KMnO4+5H2C2O4+3H2SO4===K2SO4+2MnSO4+10CO2↑+8H2O反应速率的影响因素,有关实验数据如下表所示:下列说法不正确的是( )
|
|||||||||||||||||||||||||||||||||||||||||||||
| 14. 选择题 | 详细信息 |
某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g) 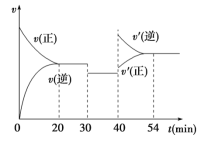 下列说法中正确的是 A. 30~40 min间该反应使用了催化剂 B. 反应方程式中的x=1,正反应为吸热反应 C. 30 min时降低温度,40 min时升高温度 D. 30 min时减小压强,40 min时升高温度 |
|
| 15. 选择题 | 详细信息 |
全钒液流电池充电时间短,续航能力强,其充放电原理为VO2++V3++H2O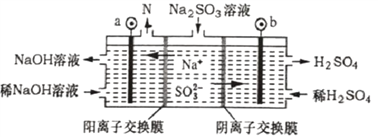 A. 全钒液流电池放电时,正极的电极反应式为VO2++2H++e-=VO2++H2O B. 图中a电极为阴极,N物质是H2 C. 全钒液流电池充电时,V3+被氧化为VO2+ D. 电解时,b电极的反应式为SO32-+H2O-2e-=SO42-+2H+ |
|
| 16. 选择题 | 详细信息 |
相关物质的溶度积常数见下表(25℃): 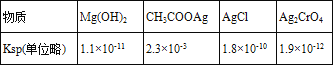 下列有关说法中不正确的是( ) A. 浓度均为0.2 mol•L-1的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 B. 将0.001 mol•L-1的AgNO3溶液滴入0.001 mol•L-1的KCl和0.001 mol•L-1 的K2CrO4混合溶液中,先产生Ag2CrO4沉淀 C. 0.ll mol•L-1的MgCL2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9 D. 在其他条件不变的情况下,向饱和AgCl水溶液中加入NaCl溶液,Ksp(AgCl)不变 |
|
| 17. 推断题 | 详细信息 |
下表为元素周期表的一部分,用化学用语回答下列问题: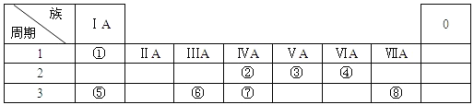 (1)化合物A是由⑤⑧两种元素构成的,用电子式表示其形成过程______________ (2)④、⑦元素形成的化合物中,⑦的原子数与④、⑦间的化学键个数之比___________________ (3)②的最简单氢化物与氧气可以设计成燃料电池,写出在碱性条件下负极的电极方程式_____________________________________ (4)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应: 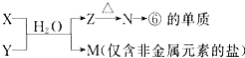 a、⑥的单质与⑤的最高价氧化物对应水化物的水溶液反应的离子方程式为:___________________; b、M中所含化学键的类型___________________________________; c、M中的阳离子的鉴定方法是_______________________________________。 |
|
| 18. 实验题 | 详细信息 |
|
过碳酸钠( Na2CO4)是一种很好的供氧剂,其与稀盐酸反应的化学方程式为:2Na2CO4+4HCl=4NaCl+2CO2 +O2+2H2O.市售过碳酸钠一般都含有碳酸钠,为测定某过碳酸钠样品(只含Na2CO4和Na2CO3)的纯度,某化学兴趣小组采用以下两种方案实施: 方案一: (1)操作①和③的名称分别为 (2)上述操作中,使用到玻璃棒的有 __(填操作序号)。 (3)请简述操作③的操作过程 方案二:按下图安装好实验装置,Q为一塑料气袋,随意取适量样品于其中,打开分液漏斗活塞,将稀盐酸滴入气袋中至充分反应。  (4)为测定反应生成气体的总体积,滴稀盐酸前必须关闭 ,打开 (填“K1”、“K2”或“K3”)。导管a的作用是 。 (5)当上述反应停止后,使K1、K3处于关闭状态,K2处于打开状态,再缓缓打开Kl。 B中装的固体试剂是 ,为何要缓缓打开K1? 。 (6)实验结束时,量筒I中有xmL水,量筒Ⅱ中收集到了ymL气体,则样品中过碳酸钠的质量分数是 。 |
|
| 19. 综合题 | 详细信息 |
工业上用重铬酸钠(Na2Cr2O7)结晶后的母液(含少量杂质Fe3+)生产重铬酸钾 (K2Cr2O7),其工艺流程及相关物质溶解度曲线如下图所示。  (1)向Na2Cr2O7母液中加碱液调pH的目的是_____________________。 (2)通过冷却结晶析出大量K2Cr2O7的原因是________________________________。 (3)固体A的主要成分为__________(填化学式),用热水洗涤固体A,回收的洗涤液转移到母液___________(填“I”“Ⅱ”或“Ⅲ”)中,既能提高产率又可使能耗降低。 (4)测定产品中K2Cr2O7含量的方法如下:称取产品试样2.500 g 配成250 mL溶液,用移液管取出25.00 mL于碘量瓶中,加入10 mL 2 mol·L-l H2SO4溶液和足量KI溶液(铬的还原产物为Cr3+),放置于暗处5 min,然后加入100 mL蒸馏水、3 mL 淀粉指示剂,用0.1200 mol·L-l Na2S2O3标准溶液滴定(已知I2+ 2S2O32-=2I-+S4O62-)。 ①酸性溶液中KI 与K2Cr2O7反应的离子方程式为_____________________________。 ②若实验中共用去Na2S2O3标准溶液40.00 mL,则所得产品中重铬酸钾的纯度为__________%( 保留2 位小数,设整个过程中其他杂质不参与反应)。 |
|
| 20. 综合题 | 详细信息 |
|
综合利用CO2对环境保护及能开发意义重大。 (1)Li2O、Na2O、MgO均能吸收CO2。如果寻找吸收CO2的其他物质,下列建议合理的是______________。 a. 可在碱性氧化物中寻找 b. 可在ⅠA、ⅡA族元素形成的氧化物中寻找 c. 可在具有强氧化性的物质中寻找 (2)Li2O吸收CO2后,产物用于合成Li4SiO4,Li4SiO4用于吸收、释放CO2。原理是:在500℃,CO2与Li4SiO4接触后生成Li2CO3;平衡后加热至700℃,反应逆向进行,放出CO2,Li4SiO4再生,说明该原理的化学方程式是__________________________。 (3)利用反应A可将释放的CO2转化为具有工业利用价值的产品。 反应A:CO2+H2O 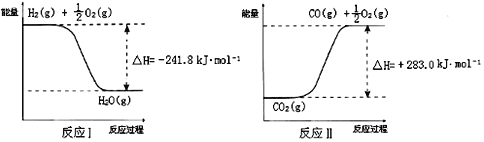 反应A的热化学方程式是___________________________。用稀氨水喷雾捕集CO2最终可得产品NH4HCO3.在捕集时,气相中有中间体NH2COONH4(氨基甲酸铵)生成.现将一定量纯净的氨基甲酸铵置于恒容的密闭真空容器中,分别在不同温度下进行反应:NH2COONH4(s) 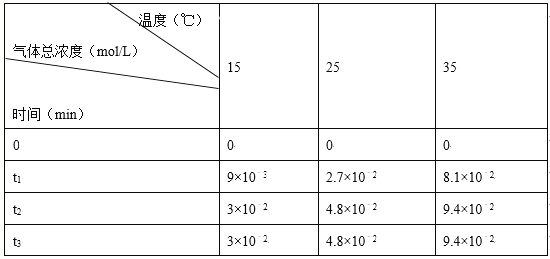 (4)高温电解技术能高效实现(3)中反应A,工作原理示意图如下: 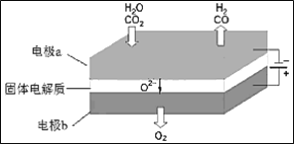 ① 电极b发生______________(填“氧化”或“还原”)反应。 ② CO2在电极a放电的反应式是___________________________。 |
|
| 21. 填空题 | 详细信息 |
离子液体是一类具有很高应用价值的绿色溶剂和催化剂,其中的EMIM+离子由H、C、N三种元素组成,结构如图所示。回答下列问题: (1)碳原子价层电子的轨道表达式为__________,基态碳原子中,核外电子占据的最高能级的电子云轮廓图为_________形。 (2)根据价层电子对互斥理论,NH3、NO3-、NO2-中,中心原子价层电子对数不同于其他两种粒子的是_______。NH3比PH3的沸点高,原因是_________。 (3)氮元素的第一电离能比同周期相邻元素都大的原因是____________。 (4)EMIM+离子中,碳原子的杂化轨道类型为______。分子中的大π键可用符号 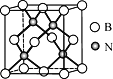 (5)立方氮化硼硬度仅次于金刚石,但热稳定性远高于金刚石,其晶胞结构如图所示。立方氮化硼属于_______晶体,其中硼原子的配位数为_______。已知:立方氮化硼密度为dg/cm3,B原子半径为xpm,N原子半径为ypm,阿伏加德罗常数的值为NA,则该晶胞中原子的空间利用率为________(列出化简后的计算式)。 |
|
| 22. 推断题 | 详细信息 |
[化学—选修5:有机化学基础]A(C2H4)是基本的有机化工原料。用A和常见的有机物可合成一种缩醛类香料。具体合成路线如图(部分反应条件略去):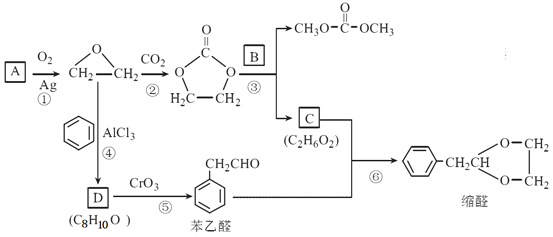 已知以下信息: ① ②D为能与金属钠反应的芳香族化合物 回答下列问题: ⑴A的名称是_________,图中缩醛的分子式是_________。 ⑵B的结构简式为_______。 ⑶以下有关C的说法正确的是_________。 a.易溶于水 b.分子中所有原子可能在同一平面 c.与乙醇互为同系物 d.在一定条件下能发生消去反应生成乙炔 ⑷③、⑤的有机反应类型依次为为______、______,④的化学方程式为_____________。 ⑸写出满足下列条件的苯乙醛的所有同分异构体的结构简式:含有苯环,加入FeCl3溶液显紫色,核磁共振氢谱有5组峰,峰面积之比为2∶2∶2∶1∶1。 ________________ ⑹参照 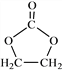 的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备 的合成路线,设计一条由2-氯丙烷和必要的无机试剂制备 的合成路线(注明必要的反应条件)。_________________________________ 的合成路线(注明必要的反应条件)。_________________________________ |
|
最近更新



