2019届上半期期末考试九年级化学考题(江苏省苏州市姑苏区)
| 1. 选择题 | 详细信息 |
|
2018年“世界环境日”中国的主题是“美丽中国,我是行动者”。每位公民都应当具有节能环保意识,成为建设“美丽中国”的行动者。下列做法与之相违背的是 A. 离开房间随手关灯 B. 布袋购物重复利用 C. 生活垃圾分类处理 D. 燃放烟花庆祝节日 |
|
| 2. 选择题 | 详细信息 |
|
下列工艺制作过程包含化学变化的是 A. 刀刻玉石 B. 裁剪窗花 C. 烧制陶瓷 D. 编织竹篮 |
|
| 3. 选择题 | 详细信息 |
|
下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是( ) A. Fe B. H2 C. H D. CO |
|
| 4. 选择题 | 详细信息 |
|
人体缺少下列哪种元素会导致甲状腺疾病 A. 铁 B. 碘 C. 锌 D. 钙 |
|
| 5. 选择题 | 详细信息 |
|
同种元素在不同的物质中可能会表现出不同的化合价,O2、H2O和H2O2三种物质中氧元素的化合价依次为 A. -2、0、-1 B. 0、-2、-1 C. 0、-1、-2 D. -1、0、-2 |
|
| 6. 选择题 | 详细信息 |
|
少量下列物质放入水中充分搅拌后不能形成溶液的是 A. 白糖 B. 白酒 C. 白醋 D. 花生油 |
|
| 7. 选择题 | 详细信息 |
|
下列有关物质的性质与用途不具有对应关系的是 A. 氮气性质稳定,可用作灯泡填充气 B. 铝合金能导电,可用作飞机机身材料 C. 干冰升华吸热,可用于冷藏食品 D. 金刚石质地坚硬,可用于切割玻璃 |
|
| 8. 选择题 | 详细信息 |
我国化学家张青莲精确测定了铈(Ce)等元素的相对原子质量数值。在元素周期表中铈元素的某些信息如图所示。下列有关铈的说法不正确的是 A. 原子序数为58 B. 属于金属元素 C. 原子核内质子数为58 D. 相对原子质量为140.1 g |
|
| 9. 选择题 | 详细信息 |
|
下列关于氧气的说法不正确的是 A. 鱼类能在水中生活,证明氧气易溶于水 B. 通常状况下,氧气是无色无气味的气体 C. 低温加压,氧气可液化成淡蓝色液体 D. 氧气性质活泼,能氧化许多物质 |
|
| 10. 选择题 | 详细信息 |
如下图所示,在烧杯A中加入10 mL浓氨水,烧杯B中加入20 mL蒸馏水并滴入2滴酚酞试液,用一个大烧杯把A、B两个烧杯罩在一起。下列叙述正确的是 A. 大烧杯内壁自下而上逐渐变红 B. 烧杯A中液体自上而下逐渐变红 C. 烧杯B中液体自上而下逐渐变红 D. 烧杯A中液体微粒在运动,烧杯B中液体微粒不运动 |
|
| 11. 选择题 | 详细信息 |
|
下列关于二氧化碳的说法正确的是 A. 光合作用需要二氧化碳,说明人类生活离不开二氧化碳 B. 用排水法能收集到二氧化碳,说明二氧化碳不溶于水 C. 空气中二氧化碳含量达6%以上会致人死亡,说明二氧化碳有毒 D. 水中通入二氧化碳后仍为无色,说明二氧化碳与水未发生反应 |
|
| 12. 选择题 | 详细信息 |
如图所示,向装有水的试管中加入某种固体物质后,U型管左侧液面上升,右侧液面下降。则加入的固体物质可能是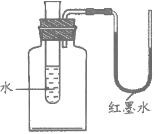 A. 食盐 B. 蔗糖 C. 硝酸铵 D. 氢氧化钠 |
|
| 13. 选择题 | 详细信息 |
|
下列物质中含有大量自由移动离子的是 A. 稀盐酸 B. 氯化钠晶体 C. 酒精 D. 石墨 |
|
| 14. 选择题 | 详细信息 |
|
下列化学用语书写不正确的是 A. 2个钙离子:2Ca2+ B. 钠原子的结构示意图: 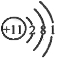 C. 氯化铜:CuCl D. 氧化镁中镁元素显+2价: |
|
| 15. 选择题 | 详细信息 |
|
乙酸乙酯(C4H8O2)是一种有浓郁香味、难溶于水的油状液体,常用作食品或饮料的调香剂。下列有关乙酸乙酷的叙述正确的是 A. 乙酸乙酯属于氧化物 B. 乙酸乙酯中碳、氢、氧元素的质量比为4:8:2 C. 乙酸乙酯是由4个碳原子、8个氢原子、2个氧原子构成的 D. 乙酸乙酯中碳元素的质量分数大于氧元素的质量分数 |
|
| 16. 选择题 | 详细信息 |
|
下列关于燃烧与灭火的说法正确的是 A. 氢气与空气充分混合遇明火一定会爆炸 B. 浸透水的棉花球接触酒精灯火焰立即燃烧 C. 用灯帽能盖灭酒精灯是因为降低了可燃物的温度 D. 关闭燃气灶阀门是为了断绝可燃物的来源 |
|
| 17. 选择题 | 详细信息 |
|
下列说法正确的是 A. 生铁和氧化铁均属于金属材料 B. 合金的硬度一般比各成分金属大 C. 生铁可以完全溶解在足量稀盐酸中 D. 回收利用废金属仅是为了节约资源 |
|
| 18. 选择题 | 详细信息 |
用如图所示装置进行电解水实验(水中加入少量氢氧化钠溶液以增强导电性),反应一段时间。下列说法正确的是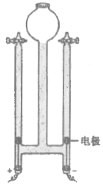 A. 球形容器内液面下降 B. 液体中氢氧化钠的浓度增大 C. 与电源正极相连的玻璃管内产生的气体体积约为负极的两倍 D. 与电源负极相连的玻璃管内产生的气体能使带火星的木条复燃 |
|
| 19. 选择题 | 详细信息 |
|
一种以甲醇为原料的新型电池的反应原理为: 2CH3OH+3X +4NaOH=2Na2CO3+6H2O。则X的化学式为 A. H2 B. O2 C. CO D. CO2 |
|
| 20. 选择题 | 详细信息 |
|
下列实验基本操作的图示正确的是 A. 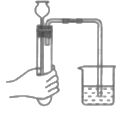 检查气密性 检查气密性B.  读液体体积 读液体体积C.  过滤悬浊液 过滤悬浊液D.  熄灭酒精灯 熄灭酒精灯 |
|
| 21. 选择题 | 详细信息 |
在盛有空气的密闭容器中进行蜡烛燃烧实验。经测定,自燃烧至熄灭过程中,容器内O2和CO含量随时间变化的曲线如图所示。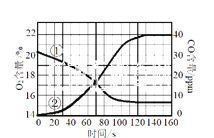 通过分析该图可推理出的结论是 A. 蜡烛由碳、氢元素组成 B. 蜡烛熄灭时,容器内氧气耗尽 C. 曲线①表示CO含量的变化 D. 蜡烛发生了不完全燃烧 |
|
| 22. 选择题 | 详细信息 |
|
下列等量关系一定成立的是 A. 10 g氢氧化钠溶液与10g硫酸铜溶液混合,形成20 g混合溶液 B. 10 mL酒精与10 mL水混合,形成20 mL酒精溶液 C. 1 g碳酸钙粉末与10g水混合,形成11 g溶液 D. 1 g氢气与9g氧气完全反应,形成9g水 |
|
| 23. 选择题 | 详细信息 |
科学家采用“组合转化”技术,可将二氧化碳在一定条件下转化为重要的化工原料乙烯(C2H4),其反应的微观过程如下图所示。下列说法不正确的是 A. 反应生成三种分子 B. 反应前后原子种类、数目均不变 C. 反应中分子发生分解,原子重新组合 D. 参加反应的两种分子的个数比是1:3 |
|
| 24. 选择题 | 详细信息 | |||||||||||||||
区分下表中的各组物质,所选择的方法或试剂不正确的是
|
||||||||||||||||
| 25. 选择题 | 详细信息 |
下列实验方案的设计中,不能达到实验目的的是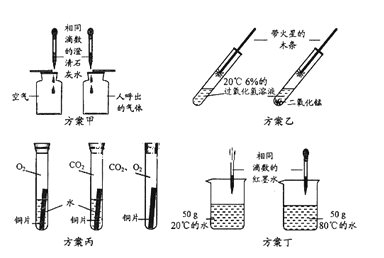 A. 用方案甲比较空气与呼出气体中二氧化碳含量大小 B. 用方案乙研究二氧化锰能加快过氧化氢分解速率 C. 用方案丙研究铜生锈产生铜绿的条件 D. 用方案丁研究温度对微粒运动速率的影响 |
|
| 26. 填空题 | 详细信息 |
|
用“>”、“<”或“=”填空。 (1)沸点:液态氮________液态氧 (2)熔点:武德合金(组成金属是铋、铅、锡、镉)________锡 (3)质子数:氯原子________氯离子 (4)导电性:Ag________Cu (5)微粒总数:100 mL 0.9%的氯化钠溶液_______10 mL 15%的氯化钠溶液 |
|
| 27. 填空题 | 详细信息 |
|
化学与人类生活息息相关。 (1)用洗洁精除去餐具上的油污,是因为洗洁精在水中对油污具有________作用。 (2)家用净水器中装有活性炭,是利用活性炭的________性除去水中的部分杂质。 (3)长期饮用硬水对人体健康不利。生活中降低水的硬度通常采用的方法是________。 (4)水烧开后壶盖被顶开,从微观角度分析其主要原因是___________。 |
|
| 28. 实验探究题 | 详细信息 |
|
回顾学生基础实验“配制50 g溶质质量分数为6%的氯化钠溶液”。 (实验过程) (1)计算:需要氯化钠的质量为3g,需要水的体积为______________mL。 (2)称取氯化钠:在已调节平衡的天平两端托盘上分别放上质量相等的纸片,用镊子移动游码至刻度如________(选填“甲”或“乙”)图所示。 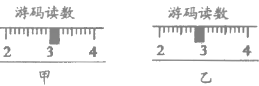 再用药匙往左盘的纸片上加氯化钠,当发现指针向左偏转时,应该____(填字母)至天平平衡,然后将称好的氯化钠倒入烧杯中。 A.增加氯化钠 B.减少氯化钠 C.增加砝码 D.减少砝码 (3)量取水:先向_______(选填“10 mL”、“50 mL”或“100 mL”)的量筒内倾倒水,当液面接近刻度时改用__________加水至所需刻度。 (4)溶解、转移:用玻璃棒搅拌至氯化钠完全溶解,再将其移入指定容器,贴上标签。 (实验反思) (5)经检测,某同学配制的氯化钠溶液的溶质质量分数偏小,原因可能是________(填字母)。 A.在左盘放纸片后再调节天平平衡,整个实验过程中右盘都未放纸片 B.将称量完毕的氯化钠转移到烧杯中时,不慎将少量氯化钠洒落在桌面上 C.氯化钠粉末不纯 D.量筒量取水的体积偏大 E.用蒸馏水洗涤烧杯,未经干燥即用来配溶液 F.转移已配好的溶液时,有少量液体溅出 (拓展计算) (6)列式计算,将所配的50g 6%的氯化钠溶液稀释至0.9%,需加入水的体积_____。 (计算结果精确到0.1 mL) |
|
| 29. 实验探究题 | 详细信息 |
下列装置常用于实验室制取气体.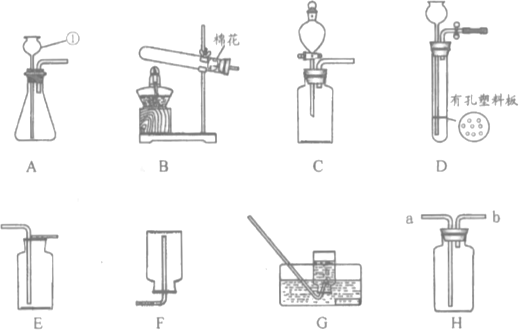 (1)写出上图中指定仪器的名称:①______________。 (2)用高锰酸钾制取并收集纯度相对较大的氧气,可以选择的装置是________(填字母)。该反应的化学方程式为____________________________,属于________(填基本反应类型)反应。 (3)制取二氧化碳时,如需控制产生气体的速率,发生装置最好选用____________(填字母),使用装置H进行排空气法收集二氧化碳,气体应从________(选填“a”或“b”)端通入。 (4)实验室制取硫化氢气体的原理:室温下,块状不溶性的硫化亚铁(FeS)固体与稀硫酸反应(另一产物为硫酸亚铁)。 ①写出该反应的化学方程式:___________________。 ②若想控制反应的发生和停止,可选用的发生装置为______________(填字母)。 ③已知硫化氢气体有毒,密度比空气大,能溶于水且易与NaOH溶液反应。请在下图方框内补充完整收集硫化氢气体的装置图。_______ 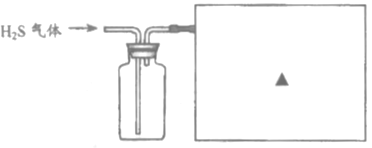 |
|
| 30. 流程题 | 详细信息 |
某工厂从含铜废料中回收铜的生产流程如下.(提示:铜灼烧后的固体可以与稀硫酸反应生成硫酸铜和水;含铜废料中,除铜外其余物质不与氧气或稀硫酸反应且不溶于水。)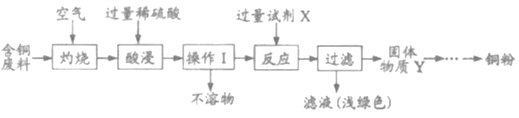 (1)“酸浸”步骤需加热。写出该步骤发生反应的化学方程式____________________。 (2)操作Ⅰ的名称是________,经操作Ⅰ分离所得溶液中含有的微粒有_______(填微粒符号)和H2O。 (3)过量试剂X与操作Ⅰ分离所得溶液发生反应,写出相关的化学方程式:____________。 (4)请补充完整由固体物质Y得到铜粉的实验方案:向固体物质Y中_____________,用水洗涤固体2~3次,干燥得到铜粉。 |
|
| 31. 实验探究题 | 详细信息 |
|
钢铁在生产生活中有广泛应用。工业用铁矿石炼铁,实验室也可模拟炼铁。 Ⅰ.工业炼铁 (1)工业炼铁的主要设备为______________。 (2)上述设备中焦炭生成CO的原理为___________(用化学方程式表示)。 (3)某钢铁公司用960万吨含氧化铁60%的赤铁矿炼铁,最多能得到的含杂质4%的生铁多少万吨__________? Ⅱ.实验室模拟炼铁 (4)实验室模拟炼铁的装置如图1所示。 ①写出仪器a的名称_____________。 ②澄清石灰水的作用______________________(用化学方程式表示)。 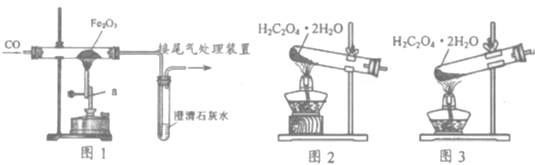 (5)实验室可用加热草酸晶体(H2C2O4·2H2O,熔点为101℃)的方法获得CO。其原理为: |
|
| 32. 实验探究题 | 详细信息 |
|
有关空气组成的研究与发现对化学的发展做出了重要贡献。 Ⅰ.拉瓦锡的研究:用加热汞的方法测定空气中氧气的含量如图4所示,拉瓦锡把少量的汞放在密闭的玻璃容器中连续加热12天后,发现有一部分银白色的液态汞变成红色粉末,容器内空气体积减少了约五分之一。收集汞表面生成的红色粉末(氧化汞),置于另一容器内强热得到了汞和氧气,且氧气的体积恰好等于原来密闭容器里所减少的空气体积。 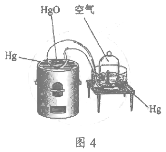 (1)上述实验中,使用汞的优点有______________。 A.汞为液态,在加热的条件下只与氧气反应且生成物为固体 B.时间足够长,能将密闭装置中的氧气几乎耗尽 C.实验过程中没有污染 D.生成的化合物加热分解又能得到汞和氧气 (2)继拉瓦锡研究后,英国科学家瑞利经多次实验发现:从空气分离得到的氮气密度总是略大于纯净氮气密度。造成这一差异主要与空气中的_______________相关。 Ⅱ.兴趣小组A的实验:用红磷燃烧的方法测定空气中氧气的含量(如图5所示) (3)用酒精灯点燃燃烧匙中过量的红磷,观察到的现象有____________________,并放出大量的热。写出该反应的化学方程式:_____________________________。 (4)该兴趣小组同学经多次实验发现:当反应停止并恢复至室温,用氧气浓度传感器测得广口瓶内始终有8%左右的氧气残留。请分析红磷燃烧无法耗尽氧气的原因是________(已排除操作原因引起的实验误差)。  Ⅲ.兴趣小组B的实验:用铁生锈原理测定空气中氧气含量(如图6所示)测得实验数据如下表:  (5)根据表中数据,计算实验测得的空气中氧气的体积分数是___________(计算结果精确到0.1%)。 (6)该实验中NaCl溶液的作用是_______________。 |
|
初中化学 试卷推荐
- 2018届九年级上册化学同步练习:第七单元 燃料及其利用 课题1 燃烧和灭火(人教版)
- 2017-2018年九年级上册化学期末考试题免费试卷(云南省彝良县)
- 江阴初级中学2019年九年级上半年化学月考测验试卷带答案和解析
- 长春东北师范大学附属中学净月实验学校2018年九年级化学上期月考测验在线答题
- 2016-2017年初三化学一模考试专题训练(江西省高安市)
- 2018届九年级上册第二次月考化学在线测验(天津市第一中学)
- 2017-2018年度第一学期12月月考九年级化学考题带答案和解析(江苏省东台市第二教育联盟)
- 2018年至2019年度第一学期科粤版版初三化学上 第3章 维持生命之气 氧气 单元测免费试卷
最近更新



