河北2019年高一化学下册月考测验同步练习
| 1. 选择题 | 详细信息 |
|
绿色能源是指使用过程中不排放或排放极少污染物的能源,如一级能源中的水能、地热、天然气等;二级能源中电能、氢能等。下列能源属于绿色能源的是 ①太阳能 ②风能 ③石油 ④煤 ⑤潮汐能 ⑥木材 A. ①②③ B. ③④⑤ C. ④⑤⑥ D. ①②⑤ |
|
| 2. 选择题 | 详细信息 |
|
下列化学用语书写正确的是 A. 氯离子的结构示意图: B. 作为相对原子质量测定标准的碳核素: C. 氯化镁的电子式: D. 用电子式表示氯化氢分子的形成过程: |
|
| 3. 选择题 | 详细信息 |
|
废电池必须进行集中处理的首要原因是( ) A. 充电后可再使用 B. 回收利用石墨电极和金属材料 C. 防止电池中汞、镉和铅等重金属离子污染土壤和水源 D. 防止电池中的电解质溶液腐蚀其他物品 |
|
| 4. 选择题 | 详细信息 |
|
下列排列顺序正确的是( ) ①热稳定性:HF>HCl>HBr ②原子半径:Na>S>O ③酸性:H3PO4>H2SO4>HClO4 ④还原性:S2->O2->F- A. ①②③ B. ②③④ C. ①②④ D. ①③④ |
|
| 5. 选择题 | 详细信息 |
某分子的球棍模型如图所示。已知分子中所有原子的最外层均达到8电子稳定结构,原子间以单键相连。下列有关说法中错误的是( ) A. X原子可能为第ⅤA族元素 B. Y原子一定为第ⅠA族元素 C. 该分子中既含有极性共价键又含有非极性共价键 D. 从圆球的大小分析,该分子可能为N2F4 |
|
| 6. 选择题 | 详细信息 |
|
W、X、Y、Z为原子序数依次增大的同周期的短周期元素。已知W、Y、Z三种原子的最外层共有11个电子,且这三种元素的最高价氧化物的水化物之间两两皆能反应,均生成盐和水。下列判断正确的是 A. W、Y、Z三种元素的最高价氧化物的水化物可能有两种是强碱、一种是强酸 B. Z元素在第3周期第ⅥA族 C. W、Y、Z三种元素有两种是金属、一种是非金属 D. W、X、Y三种元素最高价氧化物对应水化物的碱性依次增强 |
|
| 7. 选择题 | 详细信息 |
|
下列物质中,属于共价化合物的是( ) A. 氧化钙 B. 氮气 C. 硫化钠 D. 硫化氢 |
|
| 8. 选择题 | 详细信息 |
|
每种物质都既有离子键,又有共价键的一组物质是( ) A. NaOH、H2SO4、(NH4)2SO4 B. MgO、Na2SO4、NH4HCO3 C. Na2O2、NH4Cl、Na2SO4 D. HCl、Al2O3、MgCl2 |
|
| 9. 选择题 | 详细信息 |
|
下列物质中微粒的个数比不是1 : 1的是( ) A. NaHCO3晶体中的阴离子和阳离子 B. Na2O2固体中的阴离子和阳离子 C. 重氢( |
|
| 10. 选择题 | 详细信息 |
|
下列性质中,可以证明某化合物内一定存在离子键的是 A. 可溶于水 B. 具有较高的熔点 C. 水溶液能导电 D. 熔融状态能导电 |
|
| 11. 选择题 | 详细信息 |
|
下列关于化学键的说法正确的是( ) ①含有金属元素的化合物一定是离子化合物 ②第IA族和第VIIA族原子化合时,一定生成离子键 ③由非金属元素形成的化合物一定不是离子化合物 ④活泼金属与非金属化合时,能形成离子键 ⑤离子键就是阴、阳离子间的静电引力 ⑥含有离子键的化合物一定是离子化合物 ⑦离子化合物中可能同时含有离子键和共价键 A. ①②⑤ B. ④⑥⑦ C. ①③④ D. ②③⑤ |
|
| 12. 选择题 | 详细信息 |
|
下列分子中所有原子都满足最外层8电子结构的是( ) A. 水 B. 三氟化硼 C. 四氯化碳 D. 五氯化磷 |
|
| 13. 选择题 | 详细信息 |
|
根据化学反应的实质是旧键的断裂和新键的形成过程,下列变化中不属于化学变化的是( ) A. 白磷在260℃转化为红磷 B. 石墨在高温高压下转化为金刚石 C. 干冰转化为CO2气体 D. 固态S8加热到444.6℃转化为硫蒸气S2 |
|
| 14. 选择题 | 详细信息 |
|
有一种含高能量的正离子N5+的化合物N5AsF6,下列叙述错误的是( ) A. N5+共有34个核外电子 B. N5+中氮原子以共用电子对结合 C. 化合物N5AsF6中As化合价为+1 D. 化合物N5AsF6中F化合价为 |
|
| 15. 选择题 | 详细信息 |
|
已知2SO2+O2 A. O2的能量一定高于SO2的能量 B. SO2和O2的总能量一定高于SO3的总能量 C. SO2的能量一定高于SO3的能量 D. 因该反应为放热反应,故不必加热反应就可发生 |
|
| 16. 选择题 | 详细信息 |
|
已知下列反应的反应热 ( ) (1)CH3COOH(l)+2O2(g)2CO2(g)+2H2O(l) ΔH1=-870.3 kJ·mol-1 (2)C(s)+O2(g)CO2(g) ΔH2=-393.5 kJ·mol-1 (3)H2(g)+1/2O2(g)H2O(l) ΔH3=-285.8 kJ·mol-1 则反应2C(s)+2H2(g)+O2(g)CH3COOH(l)的反应热为 ( ) A.ΔH=+488.3 kJ·mol-1 B.ΔH=-244.15 kJ·mol-1 C.ΔH=-977.6 kJ·mol-1 D.ΔH=-488.3 kJ·mol-1 |
|
| 17. 选择题 | 详细信息 |
|
下列变化一定是吸热反应的是( ) A. 凡需加热后才能发生的反应 B. 所有的分解反应 C. 将热能转变为化学能的反应 D. 生成物总能量大于反应物总能量的反应 |
|
| 18. 选择题 | 详细信息 |
关于如图的说法不正确的是( ) A. 1mol固态碘与 B. 2molHI气体分解生成1mol碘蒸气与 C. 1mol固态碘变为1mol碘蒸气时需要吸收17kJ的能量 D. 碘蒸气与 |
|
| 19. 选择题 | 详细信息 |
|
氢氧燃料电池是将多孔镍电极放置在KOH溶液中,然后分别向两极通入H2和O2,即可产生电流。下列叙述中正确的是( ) A. 通入H2的电极为正极 B. 正极的电极反应式为O2+2H2O+4e-= 4OH- C. 工作时,负极区溶液pH增大 D. 工作时,溶液中的阴离子移向正极 |
|
| 20. 选择题 | 详细信息 |
|
下列说法或表示方法中正确的是( ) A. 等质量的硫蒸气和硫黄分别完全燃烧,后者放出的热量多 B. 氢气的燃烧热为285.5 kJ/mol,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)ΔH=-285.5 kJ/mol C. Ba(OH)2·8H2O(s)+2NH4Cl(s)=BaCl2(s)+2NH3(g)+10H2O(l) ΔH<0 D. 已知中和热为57.3 kJ/mol,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量要大于57.3 kJ |
|
| 21. 选择题 | 详细信息 |
如图所示,烧杯内盛有浓硝酸,在烧杯内放入用铜线连接的铁、铅两个电极,已知,原电池停止工作时,Fe、Pb均有剩余。下列说法正确的是( ) A. Fe比Pb活泼,始终做负极 B. Fe在浓硝酸中钝化始终不溶解。 C. 电池停止工作时,有Fe(NO3)3生成 D. 利用浓硝酸作电解液不符合“绿色化学”的思想 |
|
| 22. 选择题 | 详细信息 |
|
下列说法中错误的是 A. 原子及其离子的核外电子层数等于该元素所在的周期数 B. 元素周期表中从ⅢB族到ⅡB族10个纵列的元素都是金属元素 C. 除氦外的稀有气体原子的最外层电子数都是8 D. 同一元素的各种同位素化学性质几乎完全相同 |
|
| 23. 选择题 | 详细信息 |
|
下列各个装置中能组成原电池的是( ) A. 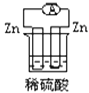 B. B.  C. C.  D. D. 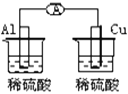 |
|
| 24. 选择题 | 详细信息 |
|
铅蓄电池的两极分别为Pb、PbO2,电解质溶液为H2SO4,工作时的反应为:Pb+PbO2+2H2SO4 =2PbSO4+2H2O,下列结论正确的是( ) A.Pb为正极被氧化 B.溶液的pH不断减小 C.SO42-只向PbO2处移动 D.电解质溶液pH不断增大 |
|
| 25. 选择题 | 详细信息 | ||||||||||||||||||||
若某原电池的离子方程式是Zn+Cu2+=Zn2++Cu,则该原电池的构成是( )
|
|||||||||||||||||||||
| 26. 选择题 | 详细信息 |
某原电池构造如图所示。下列有关叙述正确的是( ) A. 在外电路中,电子由银电极流向铜电极 B. 取出盐桥后,电流计的指针仍发生偏转 C. 外电路中每通过0.2mol电子,铜的质量理论上减小12.8g D. 原电池的总反应式为Cu +2AgNO3 ==== 2Ag +Cu(NO3)2 |
|
| 27. 选择题 | 详细信息 |
最早使用的化学电源是锌锰电池,即大家所熟悉的干电池(dry cell),其结构如下图所示:尽管这种电池的历史悠久,但对它的电化学过程尚未完全了解。一般认为,放电时,电池中的反应如下: E极:2MnO2+2H2O+2e-="==" 2MnO(OH)+2OH- F极:Zn+2NH4Cl -2e-=== Zn(NH3)2Cl2+2H+ 总反应式:2MnO2+Zn+2NH4Cl ="==" 2MnO(OH)+Zn(NH3)2Cl2 下列说法正确的是 A. E极是电池的正极,发生的是氧化反应 B. F极是电池的负极,发生的是氧化反应 C. 从结构上分析,锌锰电池应属于可充电电池 D. 锌锰电池内部发生的氧化还原反应是可逆的 |
|
| 28. 选择题 | 详细信息 |
|
蓄电池在放电时起原电池作用,在充电与放电互为逆过程。下面是爱迪生电池分别在充、放电时发生的反应:Fe(OH)2+Ni(OH)2 A. ①②③ B. ②③④ C. ①③④ D. ①②④ |
|
| 29. 选择题 | 详细信息 | |||||||||||||||||||||||||
有五个系列同族元素的物质,101.3 kPa时测定它们的沸点(℃)如下表所示:
|
||||||||||||||||||||||||||
| 30. 选择题 | 详细信息 |
|
一种新型燃料电池,它是用两根金属做电极插入KOH溶液中,然后向两极上分别通甲烷和氧气,其电池反应为:X极:CH4+10OH- A. 通过甲烷的电极(X)为电池的负极,通过氧气的电极(Y)为电池正极 B. 放电一段时间后,电解质溶液中KOH的物质的量改变 C. 在标准状况下,通过5.6L氧气,完全反应后有1.0mol的电子发生转移 D. 放电时,通过甲烷的一极附近的pH升高 |
|
| 31. 综合题 | 详细信息 |
将纯锌片和纯铜片按图方式插入100 mL相同浓度的稀硫酸中一段时间,请回答下列问题: (1)下列说法正确的是________。 A.甲、乙均为化学能转变为电能的装置 B.乙中铜片上没有明显变化 C.甲中铜片质量减少、乙中锌片质量减少 D.两烧杯中溶液的pH均增大 (2)在相同时间内,两烧杯中产生气泡的速度:甲____乙(填“>”、“<“或“=”)。 (3)当甲中产生1.12L(标准状况)气体时,通过导线的电子数目为__________。 (4)当乙中产生1.12L(标准状况)气体时,将锌、铜片取出,再将烧杯中的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol·L-1(设反应前后溶液体积不变)。试确定原稀硫酸的物质的量浓度为______。 (5)利用下列反应:Fe+2Fe3+=3Fe2+制一个化学电池(给出若干导线和一个小灯泡,电极材料和电解液自选),画出实验装置图,注明电解质溶液名称和正负极材料,标出电流方向,写出电极反应式。___  _______是正极,正极反应式:_____________; ________是负极,负极反应式:____________ (6)1958年世界上第一个心脏起搏器在瑞典植入人体成功,使用寿命长达10年之久。这种能源起搏器中安装寿命最长、可靠性最高的锂一碳电池,这种电池容量大,电压稳定,能在-56.7~71.1℃温度范围内正常工作。现已在火箭、移动电话、笔记本电脑中广泛使用。它采用锂和石墨作电极,四氯化铝锂(LiAlCl4)溶解在亚硫酰氯中(SOCl2)组成电解质溶液。电池总反应为:8Li+3SOCl2=6LiCl+Li2SO3+2S,此电池中__作正极,负极的电极反应为_______。 |
|
| 32. 推断题 | 详细信息 | ||||||||||||||||
现有6种短周期元素的性质或原子结构如下表:
|
|||||||||||||||||
| 33. 综合题 | 详细信息 |
|
氢气是未来最理想的能源之一,科学家最近研制出利用太阳能产生激光,并在二氧化钛(TiO2)表面作用使海水分解得到氢气的新技术:2H2O (1)海水分解生成的氢气用于燃料电池时,实现____能转变为____能。水分解时,断裂的化学键为____键,(填极性共价,非极性共价或离子)分解海水的反应属于_____反应(填“放热”或“吸热”)。 (2)某种氢氧燃料电池是用固体金属氧化物陶瓷作电解质,两极上发生的电极反应分别为:A极:2H2+2O2--4e-===2H2O;B极:O2+4e-===2O2-,则A极是电池的____极;电子从该极_____(填“流入”或“流出”)。电流从该电极_____(填“流入”或“流出”) (3)有人以化学反应:2Zn+O2+4H+===2Zn2++2H2O为基础设计出一种原电池,移入人体内作为心脏起搏器的能源,它们靠人体内血液中溶有一定浓度的O2、H+、Zn2+进行工作。则原电池的负极材料是____,正极上发生反应的电极反应式为____。 |
|



