新疆高一化学2018年上半期期末考试网络考试试卷
| 1. 选择题 | 详细信息 |
|
我国古代科技高度发达,下列古代文献的记载中,涉及化学变化的是 A. 《本草纲目》记载“烧酒非古法也,自元时创始,其法用浓酒精和糟入瓯(指蒸锅),蒸令气上,用器承滴露。” B. 《肘后备急方》记载“青蒿一握,以水二升渍,绞取汁。” C. 《泉州府志》物产条载“初,人不知盖泥法,元时南有黄安长者为宅煮糖,宅坦忽坏,去土而糖白,后人遂效之。” D. 《梦溪笔谈》记载“信州铅山县有苦泉,……挹其水熬之,则成胆矾,熬胆矾铁釜,久之亦化为铜。” |
|
| 2. 选择题 | 详细信息 |
|
下列物质的检验,分离和提纯方法,不正确的是( ) A. 用分液漏斗分离CCl4与水 B. 用AgNO3溶液检验氯化钠中的Cl- C. 用浓硫酸干燥CO2 D. 用蒸馏水区别酒精与苯 |
|
| 3. 选择题 | 详细信息 |
|
下列物质的分类合理的是( ) A. 铵盐:NH4Cl、NH4NO3、(NH4)2SO4、NH3·H2O B. 碱:NaOH、KOH、Ba(OH)2、Na2CO3 C. 氧化物:CO2、NO、SO2、H2O D. 碱性氧化物:Na2O、CaO、CO2、Al2O3 |
|
| 4. 选择题 | 详细信息 |
|
用NA表示阿伏伽德罗常数的值,下列判断正确的是( ) A.常温常压下,11.2 LO2中含有的原子数目为NA B.24 g Mg变为Mg2+时失去的电子数目为NA C.1 L 1 mol·L-1 CaCl2溶液中含有的Cl-离子数目为NA D.1 mol H2含有的分子数目为NA |
|
| 5. 选择题 | 详细信息 |
|
下列反应中必须加入还原剂才能进行的是 A. Cl2→Cl- B. Zn→ Zn2+ C. H2→H2O D. CuO→CuCl2 |
|
| 6. 选择题 | 详细信息 |
|
下列物质中,既能与强酸反应,又能跟强碱反应的是( ) ① A.①②③④⑤ B.②③④ C.①③④ D.①②③④ |
|
| 7. 选择题 | 详细信息 |
|
下列离子方程式中正确的是( ) A.小苏打溶液中加入烧碱溶液: B.氯化铝溶液中加入过量氨水: C.向氯化亚铁溶液中加入氯水: D.氢氧化钡溶液与稀硫酸混合Ba2++OH-+SO42-+H++OH-=BaSO4↓+H2O |
|
| 8. 选择题 | 详细信息 |
|
在3NO2+H2O=2HNO3+NO中,氧化剂与还原剂的分子个数比为 A.2︰1 B.1︰2 C.3︰1 D.1︰3 |
|
| 9. 选择题 | 详细信息 |
|
某无色溶液中,可大量共存的离子组是( ) A. C.Cu2+、NO3-、Cl-、SO42- D. |
|
| 10. 选择题 | 详细信息 |
|
下列化学反应中,不属于氧化还原反应的是( ) A. Mg+2HCl===MgCl2+H2↑ B. 2NO+O2===2NO2 C. CuO+H2 |
|
| 11. 选择题 | 详细信息 |
|
下列分散系中,是胶体的是( ) A. 向NaCl溶液中,加入AgNO3溶液,边加边振荡 B. 向沸水中加入几滴饱和氯化铁溶液,继续煮沸至溶液呈红褐色 C. 将蔗糖加入水中,边加边振荡 D. 将花生油滴加入水中,边加边振荡 |
|
| 12. 选择题 | 详细信息 |
|
在托盘天平的两盘,放上质量相等的A、B两烧杯,调至平衡,然后分别倒入质量相等的足量盐酸,继而在AB两烧杯中放入下述各组物质,结果天平仍保持平衡的是( ) A. 0.5 mol Na和0.5 mol Al B. 0.1 mol Zn和0.1 mol Al C. 8.4 g MgCO3和8.4 g NaHCO3 D. 10 g CaCO3 和10 g Na2CO3 |
|
| 13. 选择题 | 详细信息 |
|
实验室中,要使氯化铝溶液中的铝离子全部沉淀出来,适宜用的试剂是( ) A.氢氧化钠溶液 B.氢氧化钡溶液 C.盐酸 D.氨水 |
|
| 14. 选择题 | 详细信息 |
|
超导材料为具有零电阻及磁性的物质,以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导物质YBa2Cu3Ox。现欲合成0.5 mol此高温超导物,依化学计量数比例需取Y2O3、BaCO3和CuO的物质的量分别为( ) A. 0.50 mol、0.50 mol、0.50 mol B. 0.25 mol、1.0 mol、1.5 mol C. 0.50 mol、1.0 mol、1.5 mol D. 1.0 mol、0.25 mol、0.17 mol |
|
| 15. 选择题 | 详细信息 |
|
把2.3 g钠投入38.8 g水中,发生化学反应。假设水蒸发损失1 g,所得溶液中溶质的质量分数为( ) A. 4.6% B. 7.7% C. 10.0% D. 8.0% |
|
| 16. 选择题 | 详细信息 |
|
在氯化铁、氯化铜和盐酸的混合溶液中加入铁粉,待反应结束,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中阳离子数目最多的是 A. Cu2+ B. Fe3+ C. Fe2+ D. H+ |
|
| 17. 选择题 | 详细信息 |
|
下列各组中的两种物质作用,反应条件(温度或者反应物用量)改变,不会引起产物种类改变的是 ( ) A.Na和O2 B.NaOH和CO2 C.Na2O2和CO2 D.AlCl3和NaOH |
|
| 18. 填空题 | 详细信息 |
|
Fe3O4+4CO |
|
| 19. 计算题 | 详细信息 |
| 用双线桥法表示下列反应的电子转移情况并将其改写成离子方程式:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O,________________________,离子方程式为________________________。当3.84gCu被氧化时,__________gHNO3被还原,产生标准状况下的气体________L,转移电子数为________。 | |
| 20. 填空题 | 详细信息 |
|
(1)在一个充满CO2的铝制易拉罐中加入适量的NaOH溶液,并密封,易拉罐会慢慢变瘪,原因是____________(用化学方程式表示,下同)后又慢慢鼓起来,原因是________________。 (2)写出还原铁粉与水蒸气反应的化学方程式_____________________。 (3)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式:___________;常用澄清石灰水检验CO2气体的离子方程式是__________________________________。将表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是________________________________;反应片刻后,可观察到有气体产生,其离子方程式是________________________。 (4)人体胃液中有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内,当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。 ①用小苏打片(NaHCO3)治疗胃酸过多的离子方程式为___________________________________________。 ②如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为________________________________________________________________________。 |
|
| 21. 填空题 | 详细信息 |
|
下列九种物质:①稀硝酸 ②CO ③氨水 ④熔融NaHSO4 ⑤CaO ⑥Cu ⑦蔗糖 ⑧Fe2(SO4)3 ⑨酒精 (1)用序号填空:属于电解质的是 __________ ;能导电的是_______________ ; (2)写出④、⑧两种物质在水溶液中的电离方程式:④______________;⑧______________ 。 |
|
| 22. 推断题 | 详细信息 |
下列各物质中只有A、B、C三种单质,A的焰色反应为黄色,主要以G形式存在于海水中,F是一种淡黄色的固体,H是一种常见的无色液体,I是造成温室效应的“元凶”,各物质间的转化关系图如下: 回答下列问题: (1)A是:_____,C是:_____,L是:______,I是:____(填化学式)。 (2)写出反应①②③的化学反应方程式: ①:____________________________________; ②:____________________________________; ③:____________________________________; |
|
| 23. 实验题 | 详细信息 |
I.如图所示为常见玻璃仪器的部分结构: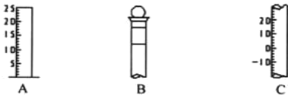 (1)请写出所列仪器的名称:A__________,B____________;C_____________; (2)仪器 B 使用前必须______________________。 (3)仪器 B 上标记有__________________(填序号); ①质量 ②温度 ③刻度线 ④浓度 ⑤容积 II. 某无色工业废水中可能含有Na+、Mg2+、Al3+、Cl-、SO42-中的几种离子。 a.取少许该废水于试管中,加入足量的Ba(NO3)2溶液和稀硝酸,产生白色沉淀,充分反应后过滤,向滤液中加入AgNO3溶液无沉淀产生。 b.另取10mL该废水于试管中,滴加NaOH溶液先产生白色沉淀,后部分沉淀溶解。生成沉淀的物质的量随加入NaOH的物质的量关系如下图所示。  根据上述实验和图中数据: (1)该废水中一定不含有的离子有________________(填离子符号); (2)写出A→B 过程中发生反应的离子方程式:_________________; (3)该废水中,c(Al3+)=________________________; (4)①实验室配制100mL2mol/L的NaOH溶液时,用到的玻璃仪器除烧杯、玻璃棒、量筒外,还需要________(填仪器名称)。 ②下列操作使所配溶液浓度偏大的是(填写字母)________。 A.称量用了生锈的砝码 B.将NaOH放在纸张上称量 C.NaOH在烧杯中溶解后,未冷却就立即转移到容量瓶中 D.往容量瓶转移时,有少量液体贱出 E.未洗涤溶解NaOH的烧杯 F.定容时仰视刻度线 G.容量瓶未干燥即用来配制溶液 |
|
最近更新



