宜宾市高二化学下册月考试卷同步考试检测
| 1. 选择题 | 详细信息 |
|
下列有机物中,实验式相同,且既不是同系物,又不是同分异构体的是( ) A. 1-辛烯和3-甲基-1-丁烯 B. 苯和乙炔 C. 1-氯丙烷和2-氯丙烷 D. 甲苯和乙苯 |
|
| 2. 选择题 | 详细信息 |
|
有机物A的氧化产物甲和还原产物乙都能和金属钠反应放出 A.甲醇 B.甲酸 C.甲醛 D.甲酸甲酯 |
|
| 3. 选择题 | 详细信息 |
苯酚和丙酮都是重要的化工原料,工业上可用异丙苯氧化法生产苯酚和丙酮,其反应和工艺流程示意图如下,下列有关说法正确的是   + +A.a、b、c均属于芳香烃 B.a、d中所有碳原子均处于同一平面上 C.A有9种属于芳香族的同分异构体 D.c、d均能发生氧化反应 |
|
| 4. 选择题 | 详细信息 |
|
下列不属于电离方程式的是 A.2 H2O C.CH3COOH+H2O |
|
| 5. 选择题 | 详细信息 |
|
水质检验中,测定水的硬度时,用到氨-氯化氨 A.将缓冲溶液加水稀释时,pH一定会减小 B.将缓冲溶液升温,pH一定没有变化 C.在缓冲溶液中,水的电离受到抑制 D.在缓冲溶液中,一定有 |
|
| 6. 选择题 | 详细信息 |
|
在一定温度下,向a L密闭容器中加入1 mol O2和2 mol NO,发生如下反应:O2(g)+2NO(g) A.容器内O2、NO、NO2的浓度之比为1∶2∶2 B.容器内压强不随时间变化 C.容器内各物质的浓度不随时间变化 D.单位时间内生成1 mol O2,同时生成2 mol NO2 |
|
| 7. 选择题 | 详细信息 |
|
用Pt电解2mol/L CuCl2溶液的实验中出现了和课本实验不同的现象,阳极产生了黄绿色气体,阴极却观察到白色沉淀、少量的红色固体及棕褐色溶液,下列说法不正确的是 A. 红色固体可能是Cu B. 棕褐色溶液可能和Cu2+、Cu+ 有关 C. 白色固体可能是CuCl D. 棕褐色溶液是由于Cu2+浓度下降引起的 |
|
| 8. 填空题 | 详细信息 |
|
根据下列化合物:①NaOH,②H2SO4,③CH3COOH,④NaCl,⑤CH3COONa,⑥NH4Cl,⑦CH3COONH4,⑧NH4H2SO4,⑨NH3·H2O,请回答下列问题: (1)若浓度均为0.1mol·L-1、等体积的NaOH和NH3·H2O分别加水稀释m倍、n倍, 稀释后两种溶液的pH都变成9,则m_______n (填“>”、“<”或“=”)。 (2)已知水存在如下平衡:H2O+H2O A.向水中加入NaHSO4固体 B.向水中加NaHCO3固体 C.加热至100℃ [其中c (H+) =1×10-6 mol·L-1] D.向水中加入NH4Cl固体 (3)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)=_______;在pH=3的CH3COOH溶液中,水电离出来的c(H+)=_______。 (4)NH4Cl溶液中离子浓度大小顺序为______________。 (5)物质的量浓度相同的⑥、⑦、⑧、⑨四种稀溶液中,NH4+浓度由大到小的顺序是(填序号)_______。 (6)己知t℃时,Kw=1×10-12,在该温度时将pH=9的NaOH溶液a L与pH=2的H2SO4溶液bL混和(忽略混合后溶液体积的变化),若所得混合溶液的pH=3,则出a∶b=_______。 |
|
| 9. 推断题 | 详细信息 |
某有机物甲和A互为同分异构体,经测定它们的相对分子质量小于100;将1mol甲在O2中充分燃烧得到等物质的量的CO2和H2O (g) ,同时消耗112L O2(标准状况);在酸性条件下将1mol甲完全水解可以生成1mol乙和1mol丙;而且在一定条件下,丙可以被连续氧化成为乙。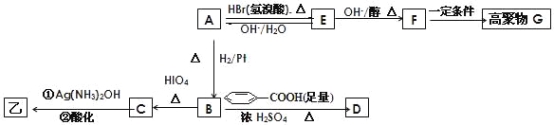 经红外光谱测定,在甲和A的结构中都存在C=O双键和C-O单键,B在HIO4存在并加热时只生成一种产物C,下列为各相关反应的信息和转化关系: 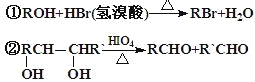 ⑴ 请确定并写出甲的分子式_______;与甲属同类物质的同分异构体共有____种(包含甲)。 ⑵ E→F 的反应类型为_________反应; ⑶ A的结构简式为_________;G 的结构简式为_________; ⑷ B→D的反应化学方程式为_______________________________; ⑸ 写出C在条件①下进行反应的化学方程式___________________。 |
|
| 10. 实验题 | 详细信息 | ||||||||||||||||||
|
滴定实验是化学学科中重要的定量实验。请回答下列问题: I.酸碱中和滴定——用标准盐酸滴定未知浓度的NaOH溶液。 (1)该学生的实验操作如下: a.用碱式滴定管取稀NaOH25.00mL,注入锥形瓶中,加入甲基橙做指示剂。 b.用待测定的溶液润洗碱式滴定管。 c.用蒸馏水洗干净滴定管。 d.取下酸式滴定管用标准的HCl溶液润洗后,将标准液注入滴定管刻度“0”以上2~3cm处,再把滴定管固定好,调节液面至刻度“0”或“0”刻度以下。 e.检查滴定管是否漏水。 f.另取锥形瓶,再重复操作一次。 g.把锥形瓶放在滴定管下面,瓶下垫一张白纸,边滴边摇动锥形瓶直至滴定终点,记下滴定管液面所在刻度。 ①滴定操作的正确顺序是(用序号填写)__→c→__→__→d→__→___。 ②某次滴定前、后的盛放盐酸滴定管中液面的位置。请回答: 仪器A的名称是__;盐酸的体积读数:滴定前读数为__mL,滴定后读数为____mL; 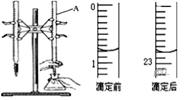 ③在G操作中如何确定终点___。 (2)下列操作造成测定结果偏高的是___(填选项字母) A.滴定终点时,俯视滴定管溶液液面 B.盛装未知液的锥形瓶用蒸馏水洗过,未用未知液润洗 C.酸式滴定管用蒸馏水洗净后,未用标准盐酸润洗 D.滴定前,滴定管尖嘴有气泡,滴定后气泡消失 II.氧化还原滴定—取草酸溶液置于锥形瓶中,加入适量稀硫酸,用浓度为0.1mol/L的高锰酸钾溶液滴定,发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+10CO2↑+2MnSO4+8H2O。表格中记录了实验数据:
|
|||||||||||||||||||
| 11. 填空题 | 详细信息 | |||||||||||||||
|
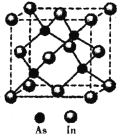
法医常用马氏试砷法检验是否砒霜( As2O3)中毒,涉及的反应如下: I:6Zn+As2O3+12HCl=6ZnCl2+2AsH3(砷烷)↑+3H2O Ⅱ:2AsH3=2As(黑色砷镜)+3H2 (1)写出砷的基态原子价电子排布图______________。 (2)砷烷的空间结构为_______;砷烷中心原子杂化方式为________。 (3)砷烷同族同系列物质相关性质如下表:
|
||||||||||||||||
最近更新