2020届高三化学二轮每周大题必练- -- 无机物制备实验流程
| 1. | 详细信息 |
为了实现资源利用最大化,某化工厂将合成氨、制纯碱和生产尿素 A.增大压强  ,标准状况下 ,标准状况下 |
|
| 2. | 详细信息 |
以明矾 依据上述流程图回答下列问题: 则 |
|
| 3. | 详细信息 |
用硼镁矿 已知: 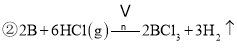 I.回答下列问题:  回答下列问题:  |
|
| 4. | 详细信息 |
金属镓有“电子工业脊梁”的美誉,它与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业制备镓的流程如下图所示: (1)元素Ga位于Al的下一周期,写出镓(Ga)的原子结构示意图为 ____________CO2的电子式为_____________________ (2)下列有关Al、Ga的说法不正确的是______ A.由流程图可知酸性:Al(OH)3>Ga(OH)3 B.Ga2O3可与盐酸反应生成GaCl3 C.Ga(OH)3可由Ga2O3与水反应得到 D.与酸反应的剧烈程度:Al<Ga (3)图中涉及到的Al、Na、O三种元素简单离子半径由大到小的顺序_____________ (4)步骤二中不能通入过量的CO2,理由_________________(用离子方程式表示) (5)工业上通常用电解精炼法提纯镓。某待提纯的粗镓内含Zn、Fe、Cu杂质,以NaOH水溶液为电解质溶液。在电流作用下使粗镓溶解进入电解质溶液,通过某种离子迁移技术到达阴极,并在阴极放电析出高纯镓。(离子氧化性顺序为:Zn2+<Ga3+<Fe2+) ①下列有关电解精炼说法正确的是_______ A.阳极发生氧化反应,其主要电极反应式:Ga-3e- ═ Ga3+ B.电解过程中,阳极质量的减少与阴极质量的增加相等 C.在阴极除了析出高纯度的镓之外,还有H2产生 D.电解后,电解槽底部的阳极泥中只有Cu和Fe ②阴极析出高纯度镓的电极反应式__________________________________ (6)氮化镓在电和光的转化方面性能突出,是迄今理论上光电转化效率最高的材料。氮化镓(GaN)的一种制备方法是采用GaCl3与NH3在一定条件下反应,写出该反应的化学方程式__________________ |
|
| 5. | 详细信息 |
ZnSe是一种光电性能优异的半导体材料,某研究小组用如图1方法制备了ZnSe. |
|
| 6. 综合题 | 详细信息 | ||||||||||||||||||
皮革工业污泥中含较多的Cr,工业采用以下工芝制得M[Cr(OH)(H20)5S04]。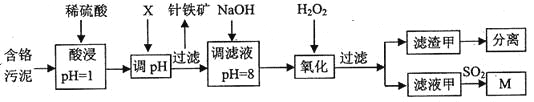 已知:①工艺中硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Cu2+、Mg2+。 ②常温下部分阳离子以氢氧化物沉淀形式存在时溶液的pH见下表:
|
|||||||||||||||||||
| 7. | 详细信息 |
洗煤和选煤过程中排出的煤矸石(主要含Al2O3、SiO2及Fe2O3)会占用大片土地,造成环境污染。某课题组利用煤矸石制备聚合氯化铝流程如下: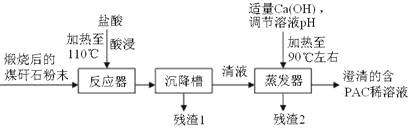 已知:聚合氯化铝([Al2(OH)nCl6-n]m(1≤n≤5,m≤10),商业代号PAC)是一种新型、高效絮凝剂和净水剂。 (1)酸浸的目的是___________________________;实验需要的500mL3.0 mol·L-1的盐酸,配制时所需要的玻璃仪器除量筒、烧杯、玻璃棒外还有______________________。 (2)若m=n=2,则生成PAC的化学方程式是_____________________。 (3)从含PAC的稀溶液中获得PAC固体的实验操作方法是_______、_________、_________。 (4)为了分析残渣2中铁元素的含量,某同学称取5.000g残渣2,先将其预处理使铁元素还原为Fe2+,并在容量瓶中配制成100mL溶液;然后移取25.00mL试样溶液,用1.000×10-2mol·L-1KMnO4标准溶液滴定,消耗标准溶液20.00mL。已知反应式为Fe2++MnO4-+H+—Fe3++Mn2++H2O(未配平)。判断滴定终点的依据是_______________________;残渣2中铁元素的质量分数为________________。 |
|
| 8. 实验题 | 详细信息 |
硫代硫酸钠(Na2S2O3•5H2O)俗名“大苏打”,又称为“海波”,可用于照相业作定型剂,也可用于纸浆漂白作脱氧剂,它易溶于水,难溶于乙醇,加热、遇酸均易分解,工业上常用亚硫酸钠法、硫化碱法等制备,某实验模拟工业硫化碱法制取硫代硫酸钠,其反应装置及所需试剂如图: 实验具体操作步骤为: ①开启分液漏斗,使硫酸慢慢滴下,适当调节分液漏斗的滴速,使反应产生的SO2气体均匀的通入Na2S和Na2CO3的混合溶液中,同时开启电动搅拌器搅动,水浴加热,微沸 ②直至析出的浑浊不再消失,并控制溶液的PH接近7时,停止通入SO2气体 ③趁热过滤,将滤液加热浓缩,冷却析出Na2S2O3•5H2O ④在经过滤、洗涤、干燥.得到所需产品 (1)写出仪器A的名称_____________,步骤④中洗涤时,为了减少产物的损失的试剂可以是_______ (2)为了保证硫代硫酸钠的产量,实验中不能让溶液PH<7,请用离子方程式解释原因_____________ (3)最后得到的产品可能含有反应Na2SO4杂质,请设计实验检测产品中是否存在Na2SO4(已知BaS2O3不溶于水),简要说明实验操作.现象和结论_____________ (4)测定产品纯度 ①准确称取1.00g产品,用适量蒸馏水溶解,以淀粉作指示剂用0.1000mol•L﹣1碘的标准溶液滴定,反应原理为2S2O32﹣+I2=S4O32﹣+2I﹣,滴定起始和终点的滴定管液面位置如图则消耗碘的标准溶液体积为_______mL,产品的纯度为_______%  ②若滴定时振荡不充分,刚看到溶液局部变色就停止滴定,则会使样品中Na2S2O3•5H2O的质量分数的测量结果________(填“偏高”“偏低”或“不变”)。 (5)Na2S2O3常用于脱氧剂,在溶液易被Cl2氧化SO42﹣,该反应的离子方程式为________。 |
|
| 9. 实验题 | 详细信息 | ||||||||||||
四氯化锡可用作媒染剂。利用如图所示装置可以制备四氯化锡(部分夹持装置已略去); 有关信息如下表:
|
|||||||||||||
| 10. 实验题 | 详细信息 |
某同学用下面实验装置设计实验制备SO2并进行相关探究活动。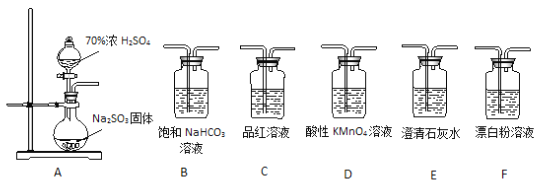 (1)装置A中反应的化学方程式为________________________。 (2)甲同学认为利用上述装置也可证明亚硫酸酸性强于次氯酸,请写出正确的装置连接顺序:A→_________→_________→C→F。 (3)乙同学从上面装置中选择合适的装置验证亚硫酸与碳酸的酸性强弱,其中用到C、D装置。则C装置的作用是________________________,通过______________________现象即可证明亚硫酸酸性强于碳酸。 (4)丙同学将A中产生的足量的SO2通入下图装置G中,G中有白色沉淀生成。该沉淀的化学式为_________。  推测产生沉淀的原因可能是(不考虑空气的影响) 原因一:SO2在酸性条件下被NO3―氧化; 原因二:SO2被Fe3+氧化; 原因三:__________________。 若是原因二,需证明Fe3+的还原产物,其实验操作及现象是________________________。 (5)实验中发现Na2SO3可能部分变质,现需测定Na2SO3的纯度,称15.0 g Na2SO3样品,配成250 mL溶液,取25.00 mL溶液,用0.20 mol·L―1酸性KMnO4溶液进行滴定,达到滴定终点时消耗KMnO4溶液20.00 mL。达到滴定终点时锥形瓶中溶液颜色变化是______________,样品中Na2SO3质量分数是_____________。 |
|
| 11. 实验题 | 详细信息 |
实验室用 已知 |
|



