2019届初三下册中考一模化学在线测验完整版(四川省雅安市芦山中学)
| 1. | 详细信息 |
|
假酒会给人的身体甚至生命带来严重的危害.这是因为假酒中含有过量的( ) A. 乙醇 B. 水 C. 甲醇 D. 碳酸 |
|
| 2. | 详细信息 |
|
下列物质在应用中,只应用其化学性质的是( ) A.将活性炭放入冰箱中除去异味 B.用铅笔芯粉末使锁的开启变的更灵活 C.用二氧化碳灭火 D.用一氧化碳来冶炼生铁 |
|
| 3. | 详细信息 |
如图是硫原子的原子结构示意图,下列对硫原子的叙述正确的是( ) A. 第一电子层有6个电子 B. 原子核内有16个质子 C. 在化学反应中容易失去电子 D. 最外层电子比第二层电子的能量低 |
|
| 4. | 详细信息 |
|
氮元素与氧元素最本质的区别是 A. 相对原子质量不同 B. 中子数不同 C. 中子数与核外电子数之和不同 D. 质子数不同 |
|
| 5. | 详细信息 |
|
某些食物的近似pH为:牛奶6.3~6.6,葡萄3.5~4.5,玉米粥6.8~8.0,苹果2.9~3.3,其中酸性最强的是( ) A. 葡萄 B. 牛奶 C. 苹果 D. 玉米粥 |
|
| 6. | 详细信息 |
法国化学家肖万、美国化学家格拉布斯和施罗克在有机化学领域研究中作出了重要贡献,其研究成果可以简单描述为如下的反应(R1 ~ R8为H–、CH3–、C2H5–……等)。 上述反应类似于无机反应中的 A.置换反应 B.分解反应 C.化合反应 D.复分解反应 |
|
| 7. | 详细信息 |
|
下列客机上使用的物品中,属于合成材料的是( ) A. 合金门把手 B. 真皮椅套 C. 塑料快餐盒 D. 羊毛毯子 |
|
| 8. | 详细信息 |
|
金刚石和石墨都是由碳元素组成的单质,但物理性质差异很大,原因是( ) A. 原子排列方式不同 B. 原子大小不同 C. 原子数目不同 D. 原子种类不同 |
|
| 9. | 详细信息 |
|
下列有关铁的叙述,错误是 ( ) A. 铁具有导电和导热性质 B. 铁与硫酸镁溶液反应得镁 C. 铁在潮湿的空气中会生锈 D. 铁跟盐酸反应生成氯化亚铁和氢气 |
|
| 10. | 详细信息 |
|
天然气的主要成分CH4也是一种会产生温室效应的气体,对于相同分子数的CH4和CO2,CH4产生的温室效应更明显.下面是有关天然气的几种叙述;①天然气与煤、柴油相比是较清洁的能源;②等质量的CH4和CO2产生的温室效应也是前者明显;③燃烧天然气也是酸雨的成因之一.其中正确的是( ) A. ①和② B. 只有① C. 只有③ D. ①②③ |
|
| 11. | 详细信息 |
|
推理是一种重要的化学思维方法,以下推理正确的是( ) A. 阳离子是带正电的粒子,带正电的粒子一定是阳离子 B. 碳酸盐与酸反应放出气体,能与酸反应放出气体的物质不一定是碳酸盐 C. 中和反应一定有盐和水生成,生成盐和水的反应一定是中和反应 D. 氧化物中含有氧元素,含有氧元素的化合物一定氧化物 |
|
| 12. | 详细信息 |
如图是不含结晶水的a、b、c 三种物质的溶解度曲线,下列说法正确的是 ( )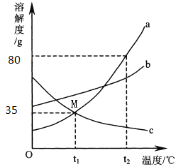 A.t2℃时,将50g a 物质加入到50g 水中充分搅拌,得到100g a的饱和溶液 B.用等质量的a、b、c 三种固体配制成t2℃时的饱和溶液,所得溶液质量的大小关系是:c溶液 > b溶液 > a溶液 C.将t1℃时三种物质的饱和溶液升温到t2℃时,所得溶液中溶质的质量分数的大小关系是: b > a = c D.将t2℃时a、b 两种物质的饱和溶液降温到t1℃时,析出晶体的质量: a > b |
|
| 13. | 详细信息 |
中国2010年上海世博会期间,世博园区内的一些设计概念体现了“城市,让生活更美好”的主题. (1)用“活性炭+超滤膜+紫外线”组合工艺获得直饮水.其中活性炭的作用是_____. (2)餐厅制作美食用到的下列食物中,富含蛋白质的是_____(填序号,下同).  (3)使用的电动观光车,有效减少了CO2、SO2、CO等气体的排放,这些气体中能引起温室效应的是_____,会造成酸雨的是_____. |
|
| 14. | 详细信息 |
构建知识网络,可以帮助我们理解知识间的内在联系。下图是盐酸与不同类别物质之间反应的知识网络。  (1)图中M应为 类物质。 (2)写出盐酸与一种金属氧化物反应的化学方程式 。 |
|
| 15. | 详细信息 |
水在实验室中的应用。 (1)水的电解 ①宏观现象:按如图一所示装置,通电一段时间后,试管A、B中产生气体的体积比约为_____,反应的符号表达式为_____。 ②微观该反应中发生分解的微粒名称是_____。 ③结论:水由_____组成。 (2)水的应用 ①碘与锌在常温下反应速度很慢,若滴入几滴水则反应剧烈,水在此的作用是_____。 ②下列实验中,对水的主要作用分析正确的是_____(填字母,可多选) A a图中的水封住试管及导管中的空气,并便于观察容器内外气压变化 B b图集气瓶中的水排尽空气且便于观察H2何时集满 C c图中的水防止高温熔融物炸裂集气瓶 |
|
| 16. | 详细信息 |
|
味精是主要成分谷氨酸钠,易溶于水,其化学式是C5H8NO4Na,与硝酸银溶液不反应。味精中还含有氯化钠(味精中其他成分不考虑),氯化钠与硝酸银溶液发生复分解反应,生产氯化银白色沉淀。回答下列问题: (1)称取5.0g味精配制成50g溶液,量取蒸馏水的量筒规格是________(填字母)。 A.10mL B.50mL C.100 mL (2)如图是配制过程,正确的操作顺序为________((填序号)。  (3)为测定味精中NaCl的质量分数,进行如下实验: 在其他操作均正确的情况下,若在配制溶液过程中,仰视刻度量取蒸馏水,则所配制溶液的谷氨酸钠质量分数________((填“偏大”、“偏小”或“无影响”) (4)为测定味精中含有氯化钠的质量分数,继续实验: ①向所配制的50g溶液中加入过量的________(溶液(填化学式)充分反应。 ②然后进行________((填操作名称)、洗涤、干燥、称量白色沉淀固体。经精确测定白色沉淀的质量为2.87g,则该味精中氯化钠的质量分数为_________ |
|
| 17. | 详细信息 | ||||||||
工业上以高纯度的二氧化锰为原料制备高锰酸钾的主要流程如下: 已知相关物质的溶解度(20℃)如下表:
|
|||||||||
| 18. | 详细信息 |
|
现代农业发展越来越离不开化肥、农药的支持,但化肥农药的滥用也对环境造成了很大的影响。请你谈谈使用农药、化肥的利与弊。(各一点) ____________________________ |
|
| 19. | 详细信息 |
某粗盐中除NaCl以外还含有少量杂质MgCl2,为了测定粗盐中MgCl2的质量分数。取固体样品50.0g完全溶解于150.0g水中,并向其中逐渐加入一定浓度的NaOH溶液,实验过程中生成沉淀的质量与加入NaOH溶液的质量的关系如图所示: 注:发生反应的化学方程式为:MgCl2+2NaOH=Mg(OH)2↓+2NaCl 请根据相关信息完成下列计算: (1)反应完全时,生成氢氧化镁的质量为_____g; (2)在粗盐中氯化镁的质量分数;_____ (3)恰好完全反应时得到的溶液中溶质的质量分数。_____ |
|
初中化学 试卷推荐
- 初三上学期期末化学在线考试题免费练习(2019-2020年湖南省株洲市茶陵县)
- 2019届初三上学期学业水平考试考前验收化学试卷带参考答案和解析(山东省潍坊市)
- 初三上期期中化学免费试卷完整版(2019-2020年安徽省六安市金安区汇文中学)
- 山东八年级化学月考测验(2019年上半期)试卷带解析及答案
- 2018至2019年中考化学一模考试考试完整版(河北省北京大学附属中学益田同文学校)
- 安徽省滁州市全椒县2020-2021年九年级上半年期末化学题带答案和解析
- 2019-2020年初三上半期开学考试化学(天津市南开区南开翔宇学校)
- 2019-2020年初三上半年期中化学试卷完整版(黑龙江省大庆市龙凤区)
最近更新



