山东2019年高二上册化学月考测验免费检测试卷
| 1. 选择题 | 详细信息 |
化学家格哈德·埃特尔证实了氢气与氮气在固体催化剂表面合成氨的反应过程,示意图如下: 下列关于合成氨反应的叙述中不正确的是 A. 该过程表明,在化学反应中存在化学键的断裂与形成 B. 在催化剂的作用下,反应物的化学键变得容易断裂 C. 过程②需吸收能量,过程③则放出能量 D. 常温下该反应难以进行,是因为常温下生成物的化学键难以形成 |
|
| 2. 选择题 | 详细信息 | ||||||||||
合成氨工业中氢气可由天然气和水反应制备,其主要反应为:CH4(g)+ 2H2O(g)
|
|||||||||||
| 3. 选择题 | 详细信息 |
|
下列热化学方程式书写正确的是(ΔH的绝对值均正确) ( ) A. C(s)+1/2O2(g)=CO(g) ΔH=-110.5kJ·mol-1(燃烧热) B. 2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1(反应热) C. C2H5OH+3O2=2CO2+3H2O ΔH=-1368.8 kJ·mol-1(反应热) D. 2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ·mol-1(中和热) |
|
| 4. 选择题 | 详细信息 |
|
下列有关热化学方程式及其叙述正确的是 ( ) A.H2的燃烧热为285.8 kJ·mol-1,则H2O电解生成H2和O2的热化学方程式为2H2O(l)=2H2(g)+O2(g)ΔH=+285.8 kJ·mol-1 B.1 mol CH4完全燃烧生成CO2(g)和H2O(l)时放出890 kJ的热量,其热化学方程式为 C.已知H2(g)+Cl2(g)=2HCl(g) ΔH=-Q(Q>0) kJ·mol-1,则H2的燃烧热为Q kJ·mol-1 D.HF与NaOH溶液反应:H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol |
|
| 5. 选择题 | 详细信息 |
|
下列关于能量转化的说法中,不正确的是 A. 电解水生成氢气和氧气时,电能转化为化学能 B. 绿色植物进行光合作用时,太阳能转化为化学能 C. 白炽灯工作时,电能全部转化为光能 D. 煤燃烧时,化学能主要转化为热能 |
|
| 6. 选择题 | 详细信息 |
(2013·北江中学月考)将下列物质分别装入有水的锥形瓶里,立即塞紧带U形管的塞子,发现U形管内滴有红墨水的水面呈现如图所示状态。加入的物质不可能是(不考虑加入物质引起的溶液体积的变化)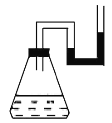 A.固体NaOH B.浓H2SO4 C.Ba(OH)2·8H2O与NH4Cl糊状物 D.CaO固体 |
|
| 7. 选择题 | 详细信息 |
已知:H2(g)+F2(g)=2HF(g),反应过程中的能量变化如图所示,下列说法正确的是( )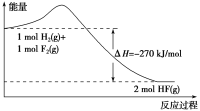 A.1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量为270 kJ B.氟化氢气体分解生成氢气和氟气的反应是放热反应 C.在相同条件下,1 mol H2(g)与1 mol F2(g)的能量总和大于2 mol HF(g)的能量 D.其他条件不变,加入催化剂,该反应的ΔH减小 |
|
| 8. 选择题 | 详细信息 |
N2和H2合成NH3的能量变化如图所示,该反应的热化学方程式是( ) A.N2(g)+3H2(g)=2NH3(l) △H=2(a-b-c)kJ/mol B.N2(g)+3H2(g)=2NH3(g) △H=2(b-a)kJ/mol C.1/2 N2(g)+3/2H2(g)=NH3(l) △H=(b+c-a)kJ/mol D.1/2 N2(g)+3/2H2(g)=NH3(g) △H=(a+b)kJ/mol |
|
| 9. 选择题 | 详细信息 |
|
已知SF6是一种优良的绝缘气体,分子结构中只存在S-F键。1molS(s)转化为气态硫原子吸收能量280kJ,断裂1 mol F-F、S-F键需吸收的能量分别为160kJ、330kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为 A.-1780kJ.mol-1 B.+430kJ.mol-1 C.-450kJ.mol-1 D.-1220kJ.mol-1 |
|
| 10. 选择题 | 详细信息 |
|
反应A+B→C △H <0,分两步进行 ① A+B→X △H>0 ② X→C △H<0 。下列示意图中,能正确表示总反应过程中能量变化的是 A.  B. B. 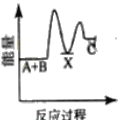 C.  D. D. 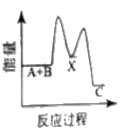 |
|
| 11. 选择题 | 详细信息 |
|
氢气、一氧化碳、辛烷、甲烷的热化学方程式分别为: H2(g)+ CO(g)+ C8H18(l)+ CH4(g)+2O2(g)=CO2(g)+2H2O(l) △H=-89.3kJ/mol 相同质量的氢气、一氧化碳、辛烷、甲烷完全燃烧时,放出热量最少的是( ) A.H2(g) B.CO(g) C.C8H18(l) D.CH4(g) |
|
| 12. 选择题 | 详细信息 |
|
下列关于反应能量的说法正确的是( ) A. Zn(s)+CuSO4(aq)═ZnSO4(aq)+Cu(s)△H=﹣216 kJ•mol﹣1,则反应物总能量>生成物总能量 B. 相同条件下,如果1 mol氢原子所具有的能量为E1,1 mol氢分子所具有的能量为E2,则2E1=E2 C. 101 kPa时,2H2(g)+O2(g)═2H2O(l)△H=﹣571.6 kJ•mol﹣1,则H2的燃烧热为571.6 kJ•mol﹣1 D. H+(aq)+OH﹣(aq)═H2O(l)△H=﹣57.3 kJ•mol﹣1,则含1 mol NaOH的氢氧化钠固体与含0.5 mol H2SO4的稀硫酸混合后放出57.3 kJ的热量 |
|
| 13. 选择题 | 详细信息 |
|
下列各组热化学方程式中,△H1>△H2的是 ( ) ①C(s)+O2(g)=CO2(g) △H1 、C(s)+ ②S(s)+O2(g)=SO2(g) △H1 、S(g)+O2(g)=SO2(g) △H2 ③H2(g)+ ④CaCO3(s)=CaO(s)+CO2(g) △H1 、CaO(s)+H2O(l)=Ca(OH)2(s) △H2 A. ① B. ④ C. ②③④ D. ①②③ |
|
| 14. 选择题 | 详细信息 |
下图是电解CuCl2溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )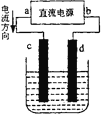 A.a为负极,b为正极 B.a为阳极,b为阴极 C.电解过程中,d电极质量增加 D.电解过程中,氯离子浓度不变 |
|
| 15. 选择题 | 详细信息 |
取一张用饱和的NaCl溶液浸湿的pH试纸,两根铅笔芯作电极,接通直流电源,一段时间后,发现a电极与试纸接触处出现一个双色同心圆,内圈为白色,外圈呈浅红色。则下列说法错误的是( )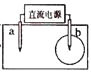 A. b电极是阴极 B. a电极与电源的正极相连 C. 电解过程中水是氧化剂 D. b电极附近溶液的pH变小 |
|
| 16. 选择题 | 详细信息 |
纳米级Cu2O由于具有优良的催化性能而受到关注。采用离子交换膜控制电解液中OH一的浓度制备纳米级Cu2O的装置如图所示,发生的反应为:2Cu+H2O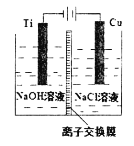 A.钛电极发生氧化反应 B.阳极附近溶液的pH逐渐增大 C.离子交换膜应采用阳离子离子交换膜 D.阳极反应式是:2Cu+2OH一一2e一== Cu2O+H2O |
|
| 17. 选择题 | 详细信息 |
|
下列叙述正确的是( ) A.电解池的阴极上发生失电子的氧化反应 B.用惰性电极电解Na2SO4溶液,阴、阳两极产物的物质的量之比为1∶2 C.用惰性电极电解饱和NaCl溶液,若有1 mol电子发生转移,则生成1 mol NaOH D.酸溶液、碱溶液、盐溶液电解后,溶液的pH都增大 |
|
| 18. 选择题 | 详细信息 |
如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( ) A.逸出气体的体积,a电极的小于b电极的 B.一电极逸出无味气体,另一电极逸出刺激性气味气体 C.a电极附近呈红色,b电极附近呈蓝色 D.a电极附近呈蓝色,b电极附近呈红色 |
|
| 19. 选择题 | 详细信息 |
|
关于镀铜和电解精炼铜,下列说法中正确的是( ) A. 都用粗铜作阳极、纯铜作阴极 B. 电解液的成分都保持不变 C. 阳极反应都只有Cu-2e-=Cu2+ D. 阴极反应都只有Cu2++2e-=Cu |
|
| 20. 填空题 | 详细信息 |
|
依据事实,写出下列反应的热化学方程式。 (1)甲硅烷(SiH4)是一种无色气体,遇到空气能发生爆炸性自燃,生成SiO2和液态水。已知室温下1 g甲硅烷自燃放出热量44.6 kJ,其热化学方程式___________________。 (2)13 g C2H2(g)完全燃烧生成CO2和H2O(l)时,放出659 kJ的热量,该反应的热化学方程式为 ___________________。 (3)2.3 g某液态有机物和一定量的氧气混合点燃,恰好完全燃烧,生成2.7 g水和2.24 L CO2(标准状况),并放出68.35 kJ的热量,则该反应的热化学方程式为 ______________。 (4)盖斯定律在生产和科学研究中有很重要的意义。有些反应的反应热虽然无法直接测得,但可通过间接的方法测定。现根据下列3个热化学反应方程式: Fe2O3(s)+3CO(g)= 2Fe(s)+3CO2(g) △H=-24.8 kJ·mol-1 3Fe2O3(s)+ CO(g)=2Fe3O4(s)+ CO2(g) △H=-47.2 kJ·mol-1 Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.5 kJ·mol-1 写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:_________________。 |
|
| 21. 填空题 | 详细信息 |
电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。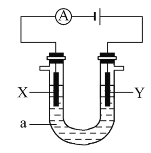 请回答以下问题: (1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则: ①电解池中X极上的电极反应式为_______,在X极附近观察到的现象是_________ ②Y电极上的电极反应式为_____________ 检验该电极反应产物的方法及现象是__________ (2)如要用电解方法精炼粗铜,电解液a选用CuSO4溶液,则: ①X电极的材料是_________________电极反应式是_________________。 ②Y电极的材料是___________电极反应式是__________________。(说明:杂质发生的电极反应不必写出) |
|
| 22. 填空题 | 详细信息 |
如图所示,甲、乙为相互串联的两电解池。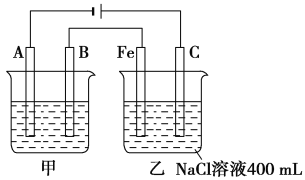 (1)甲池若为用电解原理精炼铜的装置,则A电极名称为________极,电极材料是________,电极反应式为_____________,电解质溶液可以是________。 (2)乙池中Fe极电极反应式为_________,若在乙池中滴入少量酚酞试液,开始通电一段时间,Fe极附近呈________色。 |
|
高中化学 试卷推荐
最近更新
 B.
B. 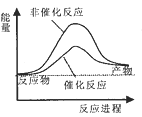 C. C
C. C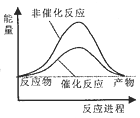 D.
D.