广东2017年九年级化学前半期中考模拟试卷带解析及答案
| 1. | 详细信息 |
|
下列变化中,属于化学变化的是 A. 水结成冰 B. 纸张燃烧 C. 干冰升华 D. 海水晒盐 |
|
| 2. | 详细信息 |
|
下列图形中,可表示塑料包装制品回收标志的是( ) A.  B. B. C. C. D. D. |
|
| 3. | 详细信息 |
某化学反应中,各物质质量随时间变化的曲线如图所示.其中说法一定正确的是( ) A.该反应是分解反应 B.物质c发生还原反应 C.物质b是化合物 D.物质a中元素种类等于b和c中元素种类之和 |
|
| 4. | 详细信息 |
|
党的十八大报告中提出建设“美丽中国”.下列做法不符合这一要求的是( ) A.合理开发洁净能源 B.全面关停化工企业 C.改进汽车尾气净化技术 D.研发易降解的生物农药和塑料 |
|
| 5. | 详细信息 |
|
下列受市民消费者依赖的无公害绿色食品中,富含维生素的是( ) A.草莓 B.大米 C.鲤鱼 D.豆腐 |
|
| 6. | 详细信息 |
|
生活离不开化学,下列认识错误的是( ) A.氦气可用于填充安全气球 B.在管道煤气中添加微量难闻气味的气体是为了及时发现煤气泄漏 C.用洗涤剂除油污是因为洗涤剂能将油污溶解,形成溶液 D.用硬水洗涤衣物,既浪费肥皂也洗不净衣物 |
|
| 7. | 详细信息 | ||||||||
下表中对部分化学知识的归纳完全正确的一组是( )
|
|||||||||
| 8. | 详细信息 |
我国科学家创造性地构建了“单中心铁催化剂”,在甲烷高效转化研究中获得重大突破。下图为该转化的微观示意图,下列有关转化的说法错误的是 A. 反应前后原子的种类发生了变化 B. 生成物之一为C2H4 C. 反应物与生成物均由分子构成 D. 催化剂改变了反应速率 |
|
| 9. | 详细信息 | |||||||||||||||
下列鉴别两种不同物质的方法中不正确的是( )
|
||||||||||||||||
| 10. | 详细信息 |
|
逻辑推理是一种重要的化学思维方法,以下推理合理的是( ) A.因为碱溶液能跟某些非金属氧化物反应,所以碱溶液能吸收 CO 气体 B.因为蜡烛燃烧生成 CO2和 H2O,所以蜡烛组成里一定含有 C 和 H C.因为燃烧需要同时满足三个条件,所以灭火也要同时控制这三个条件 D.因为酸溶液呈酸性,所以呈酸性的溶液一定都是酸溶液 |
|
| 11. | 详细信息 |
|
分别将下列各组物质同时加到足量的水中,能得到无色透明溶液的是( ) A. NaNO3NaCl H2SO4 B. CaCO3NaOH Na2SO4 C. BaCl2NaNO3CuSO4 D. AgNO3Na2SO4NaCl |
|
| 12. | 详细信息 | |||||||||||||||
下列对一些事实的解释中,不合理的是( )
|
||||||||||||||||
| 13. | 详细信息 |
|
如图分别与相应的操作过程相对应,其中正确的是( ) A. 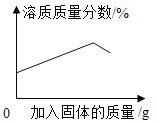 向一接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化) 向一接近饱和的硝酸钾溶液中不断加入硝酸钾晶体(不考虑温度变化)B. 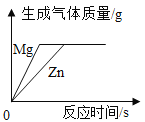 向等质量、等溶质质量分数的稀硫酸中分别加入足量的镁片和锌片 向等质量、等溶质质量分数的稀硫酸中分别加入足量的镁片和锌片C.  向 pH=10 的氢氧化钙溶液中不断加水稀释 向 pH=10 的氢氧化钙溶液中不断加水稀释D. 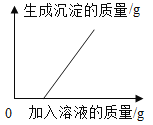 向含有硫酸的硫酸铜溶液中加入过量的氢氧化钠溶液 向含有硫酸的硫酸铜溶液中加入过量的氢氧化钠溶液 |
|
| 14. | 详细信息 |
|
已知镉(Cd)的金属活动性与铁、锌相近,镉元素在化合物中常显+2价. (1)将镉丝插入下列溶液有明显现象的是______(填序号). ①NaCl溶液 ②HCl溶液 ③AgNO3溶液 ④NaOH溶液 (2)镍镉电池应用广泛,为了防止污染环境,从废旧镍镉电池中回收镉的一种方法如下: 步骤1:将废旧电池破碎成细颗粒后焙烧,将镉转化为氧化镉(CdO); 步骤2:将含氧化镉的细颗粒和炭粉混合后,隔绝空气加热至1200℃,可得镉蒸气和一氧化碳. 步骤2中氧化镉变成镉的化学方程式是______. |
|
| 15. | 详细信息 |
根据溶解度受温度影响的信息和溶解度曲线(如图1)回答下列问题:已知硝酸钾的溶解度受温度影响比较大,食盐的溶解度受温度影响较小,熟石灰的溶解度随温度升高而减少.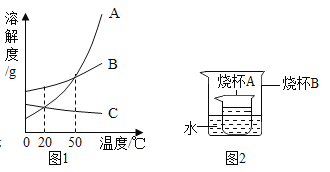 (1)A是_____的溶解度曲线. (2)50℃时,硝酸钾的溶解度_____(大于小于或等于)氯化钠的溶解度. (3)欲使硝酸钾的不饱和溶液转化为饱和溶液,可以采取的方法之一是_____. (4)如图2所示,烧杯A中是饱和的氢氧化钙溶液,向烧杯B中加入生石灰后,烧杯A中变浑浊,可能的原因是_____(填序号). A 反应放热,温度升高,氢氧化钙溶解度降低 B 反应消耗水,氢氧化钙析出 C 生石灰与水反应生成的氢氧化钙不再溶解. |
|
| 16. | 详细信息 |
以化合价为纵坐标,以物质的类别为横坐标所绘制的图像叫价类图。如图为铁的价类图,例如E点可表示+2价的亚铁盐。请回答: (1)A点表示的物质所属的物质类别是_________。 (2)请写出B点表示的物质化学式_________。 (3)已知C点表示的化合物在常温下能与氧气、水发生化合反应生成D,写出相应的化学方程式___________________。 |
|
| 17. | 详细信息 |
如图是初中化学常见物质之间的转化关系,A 是一种常用的食品干燥剂,E、F 均为氧化物,B、C、D 三种物质分别是酸、碱、盐中的一种,其中有一种是胃液的主要成分(“﹣”表示相互反应,“→”表示相互转化.部分反应的反应物、生成物和反应条件未标出). 请回答: (1)A、C、D 的化学式是_____、_____、_____. (2)B 和 D 反应的化学方程式为_____,该反应属于基本反应类型中的_____反应. (3)若 F 为黑色固体,写出 F 转化为 E 的化学方程式:_____. |
|
| 18. | 详细信息 |
黄铜矿(主要成分 CuFeS2)经初步处理后,所得溶液中的溶质为Fe2(SO4)3、CuSO4及 H2SO4. 某同学通过废铁屑与所得溶液反应,制取还原铁粉并回收铜. 主要步骤如图所示: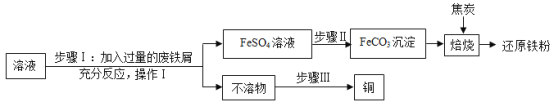 (1)Fe2(SO4)3与铁反应的化学方程式:x Fe2(SO4)3+y Fe═z FeSO4,其中 x、y、z 为化学计量数,z 的值为_____. (2)操作Ⅰ的名称是_____,此操作中起到引流作用的仪器是_____. (3)步骤Ⅰ中,生成铜的化学方程式:_____. (4)步骤Ⅰ中,废铁屑含有少量铁锈,对产物的成分没有影响,原因是_____. (5)步骤Ⅱ中加入一种可溶性试剂可实现其转化,从复分解反应发生的条件分析,该试剂可以是_____(填化学式). (6)隔绝空气进行“焙烧”,铁元素的转化途径是FeCO3 ①FeCO3 ②_____. |
|
| 19. | 详细信息 | ||||||||
|
某校化学研究性学习小组探究气体制取的实验原理与方法. (1)甲同学将课本的基础知识进行整理如图,请你帮助他完成相关内容. 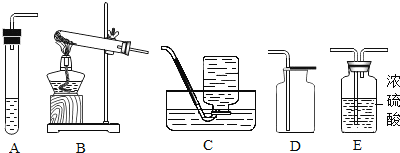
|
|||||||||
| 20. | 详细信息 |
化学兴趣小组对某工业废水(含有H2SO4、Na2SO4)中H2SO4的含量进行测定.甲、乙两同学各提出不同的测定方法,请回答有关问题: (1)甲同学:取50g废水于烧杯中,逐渐滴入溶质质量分数为20%的NaOH 溶液,反应过程溶液pH变化如图. ①当加入 30gNaOH溶液时,烧杯中的溶质为______(填化学式)。 ②50g废水中 H2SO4的质量分数是_______?(写出计算过程)。 (2)乙同学:改用BaCl2溶液代替NaOH溶液测定废水中的H2SO4的含量,结果可能会_____(填“偏高”、“偏低”、“不变”),理由是_______。 |
|




