哈尔滨市高一化学单元测试(2019年下学期)免费检测试卷
| 1. 选择题 | 详细信息 |
|
下列有关乙酸的化学用语错误的是 A. 实验式:CH2O B. 比例模型: C. 甲基的电子式: |
|
| 2. 选择题 | 详细信息 |
|
将等质量的下列各烃,完全燃烧生成CO2和H2O,耗氧量最大的是 A.CH4 B.C2H4 C.C6H6 D.C10H8 |
|
| 3. 选择题 | 详细信息 |
|
下列各组中的物质均能发生加成反应的是 A. 乙烯和乙醇 B. 苯和氯乙烯 C. 乙酸和溴乙烷 D. 丙烯和丙烷 |
|
| 4. 选择题 | 详细信息 |
|
下列物质不属于天然高分子化合物的是( ) A. 淀粉 B. 纤维素 C. 蛋白质 D. 塑料 |
|
| 5. 选择题 | 详细信息 |
|
在四个不同的密闭容器中,采用不同条件进行反应N2(g)+3H2(g) A.v(N2)=0.2mol/(L∙s) B.v(NH3)=0.8mol/(L∙min) C.v(H2)=0.3mol/(L∙s) D.v(H2)=1.3mol/(L∙min) |
|
| 6. 选择题 | 详细信息 |
|
已知H2(g)、C2H4(g)和C2H5OH(1)的燃烧热分别是-285.8kJ·mol-1、-1411.0kJ·mol-1和-1366.8kJ·mol-1,则由C2H4(g)和H2O(l)反应生成C2H5OH(l)的△H为( ) A. -44.2kJ·mol-1 B. +44.2kJ·mlo-1 C. -330kJ·mol-1 D. +330kJ·mlo-1 |
|
| 7. 选择题 | 详细信息 |
|
分子式为 A.3种 B.4种 C.5种D.6种 |
|
| 8. 选择题 | 详细信息 |
|
苯乙烯是重要的化工原料。下列有关苯乙烯的说法错误的是 A. 与液溴混合后加入铁粉可发生取代反应 B. 能使酸性高锰酸钾溶液褪色 C. 与氯化氢反应可以生成氯代苯乙烯 D. 在催化剂存在下可以制得聚苯乙烯 |
|
| 9. 选择题 | 详细信息 |
|
丁烷(C4H10)广泛应用于家用液化石油气,也用于打火机中作燃料,下列关于丁烷叙述不正确的是 A.在常温下,C4H10是气体 B.C4H10与CH4互为同系物 C.丁烷有正丁烷与异丁烷两种同分异构体 D.C4H10进行一氯取代后生成两种沸点不同的产物 |
|
| 10. 选择题 | 详细信息 |
|
下列变化,是通过取代反应来实现的是 A. CH3CH2OH ─→CH3CHO B. CH2=CH2─→CH3-CH2Br C. |
|
| 11. 选择题 | 详细信息 |
在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是 A. A B. B C. C D. D |
|
| 12. 选择题 | 详细信息 |
普通水泥在固化过程中自由水分子减少并产生Ca(OH)2,溶液呈碱性。根据这一物理化学特点,科学家发明了电动势法测水泥初凝时间。此方法的原理如图所示,反应的总方程式为:2Cu+Ag2O=Cu2O+2Ag,下列有关说法正确的  A.Cu为正极,Ag2O为负极 B.电池工作时,OH—向正极移动 C.正极的电极反应为:2Cu+2OH——2e—=Cu2O+H2O D.外电路中每通过2mol电子,正极质量减少16g |
|
| 13. 选择题 | 详细信息 |
|
苯环结构中,不存在单双键交替结构,可以作为证据的事实是( ) ①苯不能使酸性KMnO4溶液褪色 ②苯分子中碳原子间的距离均相等 ③苯能在一定条件下跟H2加成生成环己烷 ④经实验测得间二甲苯仅一种结构 ⑤苯在FeBr3存在条件下与液溴发生取代反应,但不因化学变化而使溴水褪色 A. ②③⑤ B. ①②④ C. ①②⑤ D. ①③④ |
|
| 14. 选择题 | 详细信息 |
|
新版人民币的发行引发了人们对有关人民币中化学知识的关注,下列表述错误的是 A.制造人民币所用的棉花、优质针叶木等原料的主要成分是纤维素 B.用于人民币票面文字等处的油墨中所含有的Fe3O4是一种磁性物质 C.防伪荧光油墨由颜料与树脂连接料等制成,其中树脂属于有机高分子材料 D.某种验钞笔中含有碘酒溶液,遇假钞呈现蓝色,其中遇碘变蓝的是葡萄糖 |
|
| 15. 选择题 | 详细信息 | |||||||||||||||
下列实验现象或图像信息不能充分说明相应的化学反应是放热反应的是
|
||||||||||||||||
| 16. 选择题 | 详细信息 |
氨硼烷(NH3·BH3)电池可在常温下工作,装置如图所示。未加入氨硼烷之前,两极室质量相等,电池反应为NH3·BH3+3H2O2==NH4BO2+4H2O 。已知H2O2足量,下列说法正确的是( ) A. 正极的电极反应式为2H++2e-===H2↑ B. 电池工作时,H+通过质子交换膜向负极移动 C. 电池工作时,正、负极分别放出H2和NH3 D. 工作足够长时间后,若左右两极室质量差为1.9 g,则电路中转移0.6 mol电子 |
|
| 17. 选择题 | 详细信息 |
|
已知(b) A. b的同分异构体只有d和p两种 B. b、d、p的二氯代物均只有三种 C. b、d、p均可与酸性高锰酸钾溶液反应 D. b、d、p中只有b的所有原子处于同一平面 |
|
| 18. 选择题 | 详细信息 |
|
分子式为C6H12Cl2的有机物,分子中只含有一个甲基的结构有(不包括立体异构) A.7种 B.8种 C.9种 D.10种 |
|
| 19. 选择题 | 详细信息 | |||||||||||||||
下列由实验得出的结论正确的是
|
||||||||||||||||
| 20. 选择题 | 详细信息 |
|
在实验室里,下列除去杂质的方法正确的是 ①溴苯中混有溴:加入KI溶液,用汽油萃取出溴;②除去乙烷中少量的乙烯:通过盛有足量酸性高锰酸钾溶液的洗气瓶;③除去溴苯中的溴:将其倒入浓烧碱溶液中,充分反应,静置,然后分液;④除去乙酸乙酯中的少量乙酸:加入浓氢氧化钠溶液,充分反应,静置,然后分液;⑤乙烯中混有CO2:将其通入浓氢氧化钠溶液洗气后干燥;⑥除去乙醇中少量的乙酸:加足量生石灰,蒸馏 A.①③⑤ B.②④⑥ C.③⑤⑥ D.④⑤⑥ |
|
| 21. 推断题 | 详细信息 |
物质A是来自石油的重要有机化工原料,A的产量可以用来衡量一个国家石油化工发展水平。E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料。 (1)A的结构式为________,F的结构简式为__________。 (2)写出下列反应的反应类型:①________;③_________; (3)写出反应②的化学方程式____________________; |
|
| 22. 综合题 | 详细信息 | ||||||||||||||||
如图所示的过程是目前直接利用太阳能的研究热点。人们把通过人工光化学手段合成燃料的过程叫做人工光合作用。 (1)在上图构想的物质和能量循环中太阳能最终转化为__________能。 (2)人工光合作用的途径之一就是在催化剂和光照条件下,将CO2和H2O转化为CH3OH,该反应的化学方程式为:2CO2(g)+4H2O(g)
|
|||||||||||||||||
| 23. 综合题 | 详细信息 |
Ⅰ.下图表示4个碳原子相互结合的几种方式。小圆球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都与氢结合。 (1)在上图的有机化合物中,碳原子与碳原子之间不仅可以形成共价单键,还可以形成________和三键;不仅可以形成碳链,还可以形成碳环。 (2)上图中互为同分异构体的是:A与____;D与____,与B互为同分异构体但不属于同种类的物质的是_____。(填编号) (3)写出F与溴水加成的反应方程式_________________。 Ⅱ.某有机物气体含碳82.7%,含氢17.3%,在标准状况下它的密度是2.59g/L。则该有机物可能的结构简式为______。 |
|
| 24. 综合题 | 详细信息 |
|
乳酸最初就是从酸牛奶中得到并由此而得名的。近年来,乳酸成为研究热点之一。利用乳酸 (1)请写出乳酸分子中官能团的名称_________、__________。 (2)乳酸发生下列变化: 所用的试剂是a__________,b_______(填写化学式)。 (3)乳酸在浓硫酸作用下,两分子相互反应生成环状结构的物质,写出此生成物的结构简式______。 (4)请写出乳酸与乙醇反应的化学方程式__________________________________。 (5)乳酸聚合成的纤维非常适合做手术缝合线,其原因是________________________。 |
|
| 25. 实验题 | 详细信息 |
|
实验室制备硝基苯实验装置和步骤如下: (实验步骤) 取100 mL烧杯,用20 mL浓硫酸与18 mL浓硝酸配制混合液,将混合酸小心加入B中,把18 mL(15.84 g)苯加入A中。向室温下的苯中逐滴加入混酸,边滴边搅拌,混合均匀,在50~60℃下发生反应,直至反应结束。 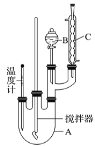 将反应液冷却至室温后倒入分液漏斗中,依次用少量水、5% NaOH溶液和水洗涤。分出的产物加入无水CaCl2颗粒,静置片刻,弃去CaCl2,进行蒸馏纯化,收集205~210 ℃馏分,得到纯硝酸基苯18.00 g。请回答: (1)装置B的名称是________,装置C的作用是________________。 (2)实验室制备硝基苯的化学方程式是____________________________。 (3)配制混合液时,_____(填“能”或“不能”)将浓硝酸加入到浓硫酸中,说明理由_________。 (4)为了使反应在50~60 ℃下进行,常用的方法是__________。 (5)在洗涤操作中,第二次水洗的作用是____________________。 |
|
最近更新







