广西2020年高三化学前半期网上考试练习
| 1. 选择题 | 详细信息 |
|
化学与生活、生产密切相关。下列叙述不正确的是( ) A.高纯硅可用于制作光导纤维 B.碳酸钠热溶液呈碱性,可用于除去餐具上的油污 C.利用太阳能蒸发海水的过程属于物理变化 D.淀粉和纤维素水解的最终产物均为葡萄糖 |
|
| 2. 选择题 | 详细信息 |
|
短周期元素W、X、Y、Z的原子序数依次增加,W原子的核外电子数等于电子层数,X2-和Y+的核外电子排布相同,X与Z同族。下列叙述正确的是( ) A.原子半径:Z>X>Y B.X的简单氢化物的稳定性比Z的强 C.Y的氢化物为共价化合物 D.Z的最高价氧化物对应的水化物是一种强酸 |
|
| 3. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数的值。下列关于常温下0.1mol/LNa2S2O3溶液与pH=1的H2SO4溶液的说法正确的是( ) A.1LpH=1的H2SO4溶液中,含H+的数目为0.2NA B.98g纯H2SO4中离子数目为3NA C.含0.1molNa2S2O3的水溶液中阴离子数目大于0.1NA D.Na2S2O3与H2SO4溶液混合产生22.4L气体时转移的电子数为2NA |
|
| 4. 选择题 | 详细信息 |
|
化合物 A.X、Y、Z均能使酸性高锰酸钾溶液褪色 B.Z的同分异构体只有X和Y两种 C.Z的二氯代物只有两种(不考虑立体异构) D.Y分子中所有碳原子均处于同一平面 |
|
| 5. 选择题 | 详细信息 | |||||||||||||||
下列所示的实验方案正确,且能达到实验目的的是( )
|
||||||||||||||||
| 6. 选择题 | 详细信息 |
室温下,用0.100mol·L−1的NaOH溶液分别滴定均为20.00mL0.100mol·L−1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是 A.Ⅰ表示的是滴定醋酸的曲线 B.pH=7时,滴定醋酸消耗的V(NaOH)>20.00mL C.V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-) D.V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |
|
| 7. 选择题 | 详细信息 |
我国科学家设计了一种智能双模式海水电池,满足水下航行器对高功率和长续航的需求。负极为Zn,正极放电原理如图。下列说法错误的是( )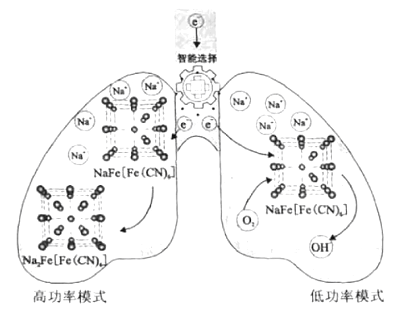 A. 电池以低功率模式工作时,NaFe[Fe(CN)6]作催化剂 B. 电池以低功率模式工作时,Na+的嵌入与脱嵌同时进行 C. 电池以高功率模式工作时,正极反应式为:NaFe[Fe(CN)6]+e-+Na+=Na2Fe[Fe(CN)6] D. 若在无溶解氧的海水中,该电池仍能实现长续航的需求 |
|
| 8. 实验题 | 详细信息 | ||||||||||||||||
实验室用乙醇、浓硫酸和溴化钠反应来制备溴乙烷,其反应原理为H2SO4(浓)+NaBr
|
|||||||||||||||||
| 9. | 详细信息 |
2019年诺贝尔化学奖颁给了日本吉野彰等三人,以表彰他们对锂离子电池研发的卓越贡献。工业中利用锂辉石(主要成分为LiAlSi2O6,还含有FeO、CaO、MgO等)制备钴酸锂(LiCoO2)的流程如图: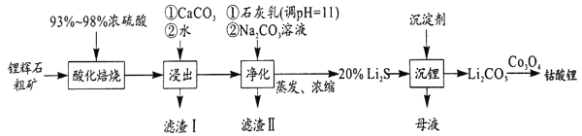 已知:Ksp[Mg(OH)2]=10-11,Ksp[Al(OH)3]=10-33,Ksp[Fe(OH)3]=10-38 回答下列问题: (1)为鉴定某矿石中是否含有锂元素,可以采用焰色反应来进行鉴定,当观察到火焰呈__,可以认为该矿石中存在锂元素。 a.紫红色 b.紫色 c.黄色 (2)锂辉石的主要成分为LiAlSi2O6,其氧化物的形式为__。 (3)为提高“酸化焙烧”效率,常采取的措施是__。 (4)向“浸出液”中加入CaCO3,其目的是除去“酸化焙烧”中过量的硫酸,控制pH使Fe3+、A13+完全沉淀,则pH至少为__。(已知:完全沉淀后离子浓度低于1×l05)mol/L) (5)“滤渣Ⅱ”的主要化学成分为___。 (6)“沉锂”过程中加入的沉淀剂为饱和的__溶液(填化学式);该过程所获得的“母液”中仍含有大量的Li+,可将其加入到“__”步骤中。 (7)Li2CO3与Co3O4在敞口容器中高温下焙烧生成钴酸锂的化学方程式为__。 |
|
| 10. 综合题 | 详细信息 |
|
随着石油资源的日益枯竭,天然气的廾发利用越来越受到重视。CH4/CO2催化重整制备合成气(CO和H2)是温室气体CO2和CH4资源化利用的重要途径之一,并受了国内外研究人员的高度重视。回答下列问题: (1)已知:①CH4(g)+H2O(g) ②CO(g)+H2O(g) CH4/CO2催化重整反应为CH4(g)+CO2(g) 该催化重整反应的△H=______kJ·mol-1。要缩短该反应达到平衡的时间并提高H2的产率可采取的措施为_____。 (2)向2L刚性密闭容器中充入2molCH4和2mol CO2进行催化重整反应,不同温度下平衡体系中CH4和CO的体积分数(  已知b>a>c,则T1______T2(填“>”“<”或“=”)。T1下该反应的平衡常数K=_______(mol2·L-2) (3)实验硏究表明,载体对催化剂性能起着极为重要的作用,在压强0.03MPa,温度750℃条件下,载体对镍基催化剂性能的影响相关数据如下表:  由上表判断,应选择载体为_______(填化学式),理由是________。 (4)现有温度相同的I、Ⅱ、Ⅲ三个恒压密闭容器,均充入2mol CH4(g)和2 molCO2(g)进行反应,三个容器的反应压强分别为p1atm、p2atm、p3atm,在其他条件相同的情况下,反应均进行到tmin时,CO2的体积分数如图所示,此时I、Ⅱ、Ⅲ个容器中一定处于化学平衡状态的是_______。  (5)利用合成气为原料合成甲醇,其反应为CO(g)+2H2(g)  该反应速率的通式为ν正=k正cm(CO)·cn(H2)(k正是与温度有关的速率常数)。由表中数据可确定反应速率的通式中n=____(取正整数)。若该温度下平衡时组别1的产率为25%,则组别1平衡时的v正=______(保留1位小数)。 |
|
| 11. 综合题 | 详细信息 | ||||||||||||||
|
氟代硼酸钾(KBe2BO3F2)是激光器的核心材料,我国化学家在此领域的研究走在了世界的最前列。回答下列问题: (1)氟代硼酸钾中非金属元素原子的电负性大小顺序是__。基态K+的电子排布式为__。 (2)NaBH4是有机合成中常用的还原剂,其中的阴离子空间构型是__,中心原子的杂化方式为__。NaBH4中存在__(填标号)。 a.离子键 b.氢键 c.σ键 d.π键 (3)BeCl2中的化学键具有明显的共价性,蒸汽状态下以双聚分子存在的BeCl2的结构式为__,其中Be的配位数为__。 (4)第三周期元素氟化物的熔点如下表:
|
|||||||||||||||
| 12. 综合题 | 详细信息 |
M是一种合成香料的中间体。其合成路线如下: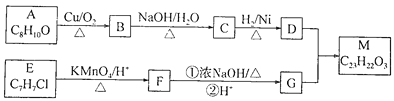 已知:①有机化合物A~M均为芳香族化合物,B能发生银镜反应,E的核磁共振氢谱有3组峰,D与G通过酯化反应合成M。 ② ③2RCH2CHO 回答下列问题: (1)A所含官能团的名称为________,F→G反应①的反应类型为________,M的结构简式为________。 (2)E的名称是________;E→F与F→G的顺序不能颠倒,原因是________。 (3)G的同分异构体中,遇FeCl3溶液显紫色且能发生银镜反应的有________种,其中苯环上的一氯代物只有2种且能发生水解反应的是________(填结构简式)。 (4)参照上述合成路线,以CH3CH2OH为原料(无机试剂任用),设计制备CH3CH2CH2CH2OH的合成路线________________。 |
|




