普洱市高一化学上册期末考试题带答案和解析
| 1. 选择题 | 详细信息 |
|
据报道:“染色”馒头中添加柠檬黄铬酸铅(PbCrO4)会使人体致癌,已被明文禁用。已知铬元素(Cr)化合价为+6价,则铅元素(Pb)的化合价为( ) A.+1 B.+2 C.+3 D.+4 |
|
| 2. | 详细信息 |
|
下列离子方程式正确的是( ) A. 向FeCl3溶液中加入过量铁粉:Fe3++Fe═2Fe2+ B. 铜溶于稀硝酸:3Cu+8H++2NO3﹣═3Cu2++2NO↑+4H2O C. 向稀硫酸中加入 Ba(OH)2 溶液:Ba2++OH﹣+H++SO42﹣═BaSO4↓+H2O D. 向Na2SiO3溶液中滴加稀盐酸:Na2SiO3+2H+═H2SiO3↓+2Na+ |
|
| 3. 选择题 | 详细信息 |
|
吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”。中国科学家尝试用Na2SeO3清除人体内活性氧,Na2SeO3的作用是( ) A.还原剂 B.氧化剂 C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂 |
|
| 4. 选择题 | 详细信息 |
|
硫酸厂有一辆存放过浓硫酸的铁槽车。某工人违反规程,边吸烟边用水冲洗铁槽车,结果发生了爆炸。下列对引起爆炸的原因说法正确的是 ( ) A.浓硫酸遇明火爆炸 B.浓硫酸遇水发热爆炸 C.铁与水(常温下)反应产生的氧化物爆炸 D.稀释后的硫酸与铁反应产生的氢气在空气中遇明火而爆炸 |
|
| 5. 选择题 | 详细信息 |
一定质量的镁和铝分别与等浓度、等体积的过量稀硫酸反应,产生气体的体积(V)与时间(t)关系如右图。下列关于反应的说法错误的是 A.镁和铝的物质的量之比为3∶2 B.镁和铝转移电子数之比为1∶1 C.镁和铝的摩尔质量之比为8∶9 D.镁和铝反应所用时间之比为3∶2 |
|
| 6. 选择题 | 详细信息 |
|
下列关于氯化铁溶液和氢氧化铁胶体的叙述中,正确的是( ) A.氯化铁溶液是电中性的,氢氧化铁胶体带有正电荷 B.通电时,氯化铁溶液溶质粒子不发生移动,氢氧化铁胶体分散质粒子向某一极移动 C.氯化铁溶液长时间静置易产生浑浊,氢氧化铁胶体长时间静置不产生浑浊 D.一束光线通过氯化铁溶液时没有明显现象,而通过氢氧化铁胶体时会出现光亮的通路 |
|
| 7. 选择题 | 详细信息 |
|
进行化学实验必须注意安全,下列操作及原理中正确的组合是 ( ) ①点燃氢气前要检验氢气的纯度,以免发生爆炸 ②CO气体有毒,处理CO气体时可将其点燃,转化为无毒的CO2 ③在盛O2的集气瓶中进行铁丝燃烧实验时,先在集气瓶底部铺上一层沙子 ④用氢气还原氧化铜时,先加热再通入氢气,以免浪费氢气 A. ①②③④ B. ①②③ C. ①②④ D. ③④ |
|
| 8. 选择题 | 详细信息 |
|
瓦斯中甲烷与氧气的质量比为1:4时极易爆炸,此时甲烷与氧气的体积比为( ) A. 1:4 B. 1:2 C. 1:1 D. 2:1 |
|
| 9. 选择题 | 详细信息 |
|
将0.3 mol钠、0.1 mol铁分别加入到各盛有500 mL 0.2 mol·L-1稀硫酸的两个烧杯中,下列说法正确的是( ) A. 两个烧杯中金属沉在液面下 B. 两个烧杯中都没有金属剩余 C. 两个烧杯中都有金属剩余 D. 两个烧杯中产生氢气的质量相同 |
|
| 10. 选择题 | 详细信息 |
|
可以说明二氧化硅是酸酐的是( ) A.它溶于水得到相应的酸 B.它对应的水化物是可溶性强酸 C.它与强碱反应只生成盐和水 D.它是非金属氧化物 |
|
| 11. 选择题 | 详细信息 |
|
有两瓶失去标签的无色液体,一瓶是饱和氯化钠溶液,一瓶是蒸馏水。为了把它们区分开,同学们提出了以下方法:①蒸发、②测密度、③测导电性、④测pH、⑤加入氯化钠、⑥加入食醋。你认为可行的是( ) A. ①②③⑤ B. ①③④⑤ C. ②③④⑥ D. ②③⑤⑥ |
|
| 12. 选择题 | 详细信息 |
|
在Cl2+H2O=HCl+HClO中,水是( ) A.只作氧化剂 B.只作还原剂 C.既作氧化剂又作还原剂 D.既不是氧化剂又不是还原剂 |
|
| 13. 选择题 | 详细信息 |
|
将12.4克氧化钠溶于87.6克水中,所得溶液溶质的质量分数是( ) A. 8.0% B. 12.4% C. 16% D. 32% |
|
| 14. 选择题 | 详细信息 |
|
检验某一溶液中是否含有氯离子,可选用的试剂是( ) A.硝酸银溶液 B.稀盐酸酸化的硝酸银溶液 C.稀硝酸酸化的硝酸银溶液 D.稀硫酸酸化的硝酸银溶液 |
|
| 15. 选择题 | 详细信息 |
|
下列变化过程中属于氧化反应的是 ( ) A. MnO2→Mn2+ B. CuO →CuCl2 C. Ag+→Ag2O D. Sn2+→Sn4+ |
|
| 16. 选择题 | 详细信息 |
|
下列物质中,既能与盐酸反应又能与氢氧化钠溶液反应的是 A. AlCl3 B. Al(OH)3 C. Al2(SO4)3 D. NaAlO2 |
|
| 17. 选择题 | 详细信息 |
|
关于下列反应的叙述正确的是( ) A.由SiO2+2C B.由CaCO3+SiO2 C.由Na2SiO3+CO2+H2O=Na2CO3+H2SiO3↓可推知碳的非金属性比硅强 D.由Na2CO3+SiO2 |
|
| 18. 选择题 | 详细信息 |
|
使5.16 g 二氧化碳和水蒸气的混合气体通过足量的过氧化钠,固体增重1.96 g,则参加反应的过氧化钠质量为( ) A. 7.8 g B. 3.9 g C. 3.2 g D. 15.6 g |
|
| 19. 选择题 | 详细信息 |
如图所示是氨催化氧化制备硝酸的实验装量,下列有关叙述正确的是( ) A.烧杯中的紫色石蕊溶液不变色 B.圆底烧瓶中的气体一定为无色 C.加热后,通过三氯化二铬的气体由无色变为红棕色 D.三氯化二铬起氧化剂的作用 |
|
| 20. 选择题 | 详细信息 |
|
已知:2NaOH+Cl2===NaCl+NaClO+H2O,关于该反应的说法正确的是( ) A. 氯气是氧化剂,氢氧化钠是还原剂 B. 氯气既是氧化剂又是还原剂 C. 氯化钠是氧化产物,次氯酸钠是还原产物 D. 1 mol氯气参加反应时转移2 mol电子 |
|
| 21. 选择题 | 详细信息 |
|
下列说法中不正确的是 A. 碳酸钠比碳酸氢钠易溶于水 B. 碳酸钠比碳酸氢钠稳定 C. 碳酸钠和碳酸氢钠能跟石灰水反应得到白色沉淀 D. 等质量的碳酸钠和碳酸氢钠分别与足量盐酸反应,得到相同质量的二氧化碳 |
|
| 22. 选择题 | 详细信息 |
|
“家庭小实验”是利用家庭生活中常见的物质,进行化学实验探究活动,下列实验不能用“家庭小实验”完成的是( ) A. 检验自来水中是否含有氯离子 B. 用闻气味的方法鉴别酒精和水 C. 检验食盐和纯碱 D. 探究铁在潮湿的空气中是否生锈 |
|
| 23. 选择题 | 详细信息 |
|
与硅酸盐改写成氧化物表达相似,四氧化三铅(Pb3O4)可改写成2PbO·PbO2,若把它看成一种盐,又可以写成Pb2[PbO4]。根据这种书写规则,如四氧化三铁(Fe3O4)用上述氧化物和盐的表示形式是( ) A. 2FeO·FeO2,Fe2[FeO4] B. FeO·Fe2O3,Fe2[FeO4] C. FeO·Fe2O3,Fe[FeO2]2 D. 2FeO·FeO2,Fe2[FeO2]2 |
|
| 24. 选择题 | 详细信息 |
|
固体氢氧化钠必须密封保存的原因是( ) ①氢氧化钠有毒 ②氢氧化钠有腐蚀性 ③氢氧化钠易吸收水分而潮解 ④氢氧化钠有挥发性 ⑤氢氧化钠能与空气中的二氧化碳反应 A.①② B.②③④ C.②③⑤ D.③⑤ |
|
| 25. 选择题 | 详细信息 |
|
密度为0.910 g·cm-3氨水,质量分数为25.0%,该氨水用等体积的水稀释后,所得溶液的质量分数为( ) A.等于12.5% B.大于12.5% C.小于12.5% D.无法确定 |
|
| 26. 选择题 | 详细信息 |
|
下列关于铁矿石的说法正确的是 ( ) A. 赤铁矿的主要成分是Fe3O4 B. 铁矿石的主要成分与铁锈的主要成分相同 C. 磁铁矿粉末溶于盐酸后,加入KSCN溶液,溶液变红色 D. FeO俗称铁红 |
|
| 27. 选择题 | 详细信息 |
|
下列物质转化过程中硫元素化合价降低的是( ) A.H2SO4→SO2 B.H2S→SO2 C.S→SO2 D.SO2→SO3 |
|
| 28. 选择题 | 详细信息 |
|
下列混合物能用过滤法分离的是( ) A.酒精和水 B.食盐和蔗糖 C.泥沙和食盐 D.铜粉和铝粉 |
|
| 29. 填空题 | 详细信息 |
有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。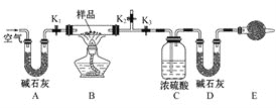 (1)实验步骤: ①按图(夹持仪器未画出)组装好实验装置后,首先进行的操作是__________。 ②称取样品,并将其放入硬质玻璃管中,称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。 ③打开活塞K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是________。 ④关闭活塞K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为________、________。 ⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。 (2)关于该实验方案,请回答下列问题。 ①若加热反应后不鼓入空气,对测定结果的影响是_______________。 ②E处干燥管中盛放的药品是碱石灰,其作用是_____________,如果实验中没有该装置,则会导致测量结果NaHCO3的质量_____________(填“偏大”“偏小”或“无影响”)。 ③若样品质量为w g,反应后C、D装置增加的质量分别为m1g、m2g,则混合物中Na2CO3·10H2O的质量分数为________(用含w、m1、m2的代数式表示)。 |
|
| 30. 实验题 | 详细信息 |
硫酸亚铁晶体(FeSO4·7H2O)在医药上作补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下: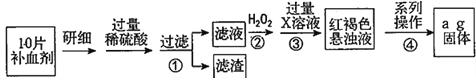 请回答下列问题: (1)向操作①的滤液中滴加KSCN 溶液后变为红色,则该滤液中含有______(填离子符号)。 (2)操作②中反应的离子方程式:__________________________________。 (3)操作③中反应的离子方程式:__________________________________。 (4)操作④中一系列处理的操作步骤:过滤、______、灼烧、_______、称量。 (5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为______g。(用含a的代数式表示) |
|
| 31. 综合题 | 详细信息 |
A、B、C、D是中学化学常见的单质,甲、乙、丙为化合物,乙在常温常压下为无色无味的液体,元素A有可变化合价。它们之间存在如下图的所示的转化关系。由此推断: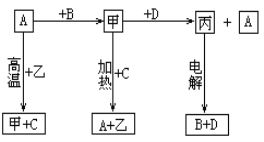 (1)甲的化学式为_____________,丙的化学式为______________。 (2)写出甲和D反应的化学方程式___________________________________________。 (3)为检验化合物甲中元素的化合价,需要用到的药品有_________________________。 A.稀硫酸 B.盐酸 C.硫氰化钾溶液 D.高锰酸钾溶液 (4)为测定A和乙高温反应后所得固体中化合物甲的质量分数。取反应后所得固体并设计以下实验: 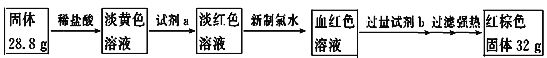 化合物甲的质量分数为________________。 |
|
| 32. 推断题 | 详细信息 |
|
有A、B、C、D四种元素,它们的原子序数依次增大,但均小于18,A和B在同一周期,A的电子式为· (1)写出A、B、C、D元素的名称:A________,B______,C________,D________。 (2)D元素在周期表中属于第________周期______族。 (3)用电子式表示A的气态氢化物的形成过程:____________。 (4)A和B的单质充分反应生成的化合物的结构式是___________。 (5)B与C形成的化合物是离子化合物还是共价化合物?如何证明?_________。 |
|
| 33. 实验题 | 详细信息 |
利用如图装置可以验证非金属性的变化规律。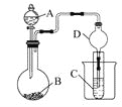 (1)仪器A的名称为________,干燥管D的作用是________________。 (2)已知在常温下,高锰酸钾和浓盐酸反应能生成氯气。实验室中现有药品Na2S溶液、KMnO4、浓盐酸、MnO2,请选择合适药品设计实验验证氯的非金属性大于硫的;装置A、B、C中所装药品分别为________、________、________,装置C中的实验现象为_________________,离子方程式为______。 (3)若要证明非金属性:S>C>Si,则A中加________、B中加Na2CO3、C中加________。 |
|
| 34. 填空题 | 详细信息 |
常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示: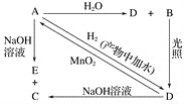 (1)请分别写出下列物质的化学式(如为溶液请填溶质的化学式):A________、B________、D________。 (2)写出下列反应的化学方程式或离子方程式(请注明反应条件):A+H2O(离子方程式):_________;A+NaOH(离子方程式):_______________;D→A(化学方程式):____________________。 |
|
最近更新



