大连市2018年高三化学上半期期末考试完整试卷
| 1. 选择题 | 详细信息 |
|
化学与生产、生活、社会密切相关,下列说法错误的是 A. 中国古代利用明矾溶液淸除铜镜表面的铜锈,是利用了明矾溶液的酸性 B. 碘是人体内必须的微量元素,所以富含高碘酸钾的食物适合所有人群 C. “光化学烟雾”“臭氧空洞”、“硝酸型酸雨”的形成都与氮氧化合物有关 D. 高纯度的二氧化硅广泛用于制作光导纤维,光导纤维遇强碱会“断路” |
|
| 2. 选择题 | 详细信息 |
|
设NA表示阿伏加德罗常数的值,下列判断正确的是 A. 常温下,pH=1的盐酸溶液中,由水电离的H+个数为10-13NA B. 标准状况下,氧原子总数为0.2NA的CO2和NO2的混合气体,其体积为2.24L C. 常温下,5.6g铁分别与足量氯气和浓硝酸反应,转移的电子数目均为0.3NA D. 100g46%(质量分数)乙醇溶液中所含O-H数目为7NA |
|
| 3. 选择题 | 详细信息 | |||||||||||||||
下列实验操作和实验结论均正确的是
|
||||||||||||||||
| 4. 选择题 | 详细信息 |
|
W、X、Y、Z是原子序数依次增大的短周期主族元素。已知W原子的最外层电子数是电子层数的2倍,Y原子次外层电子数与其它各层电子总数相等,W和X的原子序数之和等于Z的原子序数。下列说法正确的是 A. 含氧酸的酸性:Z>W B. 在一定条件下W的单质能与Y的最高价氧化物对应的水化物反应 C. 四种元素均能与氢元素形成共价键 D. 简单离子半径:X>Y>Z |
|
| 5. 选择题 | 详细信息 |
X、Y、Z、W四种物质在一定条件下具有如下图所示的转化关系,下列判断错误的是 A. 若图中反应均为非氧化还原反应,当W为一元强碱时,则Z可能是NaAlO2 B. 若图中反应均为氧化还原反应,当W为非金属单质时,则Z可能是CO2 C. 若图中反应均为非氧化还原反应,当W为一元强酸时则X可能是NH3 D. 若图中反应均为氧化还原反应,当W为金属单质时,则Z可能是FeCl2 |
|
| 6. 选择题 | 详细信息 |
2016年7月报道,南开大学科研团队在“可充室温钠-二氧化碳电池”的研究中取得突破进展,该电池放电时工作情况如图所示。下列说法错误的是 A. 金属Na为电池的负极 B. 放电时,电解液中Na+向碳电极移动 C. 充电时,碳电极发生的反应为:4Na++4e-+3CO2== 2Na2CO3+C D. 放电时,每转移2 mol电子,消耗标准状况下的CO2 33.6 L |
|
| 7. 选择题 | 详细信息 |
亚氯酸钠(NaClO2)在溶液中会生成ClO2、HClO2、ClO2-、Cl-等,其中HClO2和ClO2都是具有漂白作用。已知pOH=-lgc(OH-),经测定25℃时各组分含量随pOH变化情况如图所示(Cl-没有画出),此温度下,下列分析正确的是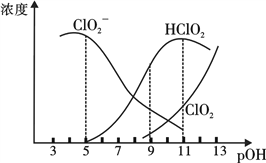 A. HClO2的电离平衡常数的数值Ka=10-8 B. pOH=11时,ClO2-部分转化成ClO2和Cl-离子的方程式为:5ClO2-+2H2O=4ClO2+ Cl-+4OH- C. pH=7时,溶液中含氯微粒的浓度大小为:c(HClO2)>c(ClO2-)>c(ClO2)>c(Cl-) D. 同浓度的HClO2溶液和NaClO2溶液等体积混合,则混合溶液中有:c(Na+)+c(OH-)=c(H+)+ c(HClO2) |
|
| 8. 实验题 | 详细信息 |
|
焦亚硫酸钠(Na2S2O5)是常用的食品抗氧化剂之一。某研究小组进行如下实验: 实验一 焦亚硫酸钠的制取 采用如图装置(实验前已除尽装置内的空气)制取Na2S2O5。装置Ⅱ中有Na2S2O5晶体析出,发生的反应为:Na2SO3+SO2=Na2S2O5 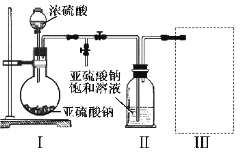 (1)装置I中产生气体的化学方程式为__________________。 (2)要从装置Ⅱ中获得已析出的晶体,可采取的分离方法是_________。 (3)装置Ⅲ用于处理尾气,可选用的最合理装置(夹持仪器已略去)为________(填序号)。 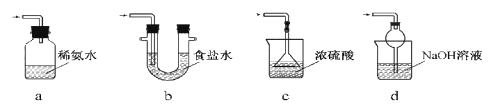 实验二 焦亚硫酸钠的性质 Na2S2O5溶于水即生成NaHSO3。 (4)证明NaHSO3溶液中HSO3-的电离程度大于水解程度,可采用的实验方法是________(填序号)。 a.测定溶液的pH b.加入Ba(OH)2溶液 c.加入盐酸 d.加入品红溶液 e.用蓝色石蕊试纸检测 (5)检验Na2S2O5晶体在空气中已被氧化的实验方案是____________。 实验三 葡萄酒中抗氧化剂残留量的测定 (6)葡萄酒常用Na2S2O5作抗氧化剂。测定某葡萄酒中抗氧化剂的残留量(以游离SO2计算)的方案如下:  (已知:滴定时反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI) ①按上述方案实验,消耗标准I2溶液25.00 mL,该次实验测得样品中抗氧化剂的残留量(以游离SO2计算)为________________g·L-1。 ②在上述实验过程中,若有部分HI被空气氧化,则测得结果____(填“偏高”“偏低”或“不变”)。 |
|
| 9. 填空题 | 详细信息 |
|
利用氢气对废气进行脱碳处理可实现绿色环保、废物利用,对于减少雾霾也具有重要意义。 (1)汽车尾气的主要污染物为NO,用H2催化还原NO可以达到消除污染的目的。 已知:2NO(g) 2H2O(l)===2H2(g)+O2(g) ΔH=+571.6 kJ·mol-1 写出H2(g)与NO(g)反应生成N2(g)和H2O(l)的热化学方程式是______________。 (2)某研究小组模拟研究如下:向2 L恒容密闭容器中充入2 mol NO发生反应2NO(g)  ①T2下,在0~5 min内,v(O2)=______________mol·L-1·min-1;该温度下反应N2(g)+O2(g) ②该反应进行到M点放出的热量______________进行到W点放出的热量(填“>”、“<”或“=”)。 M点时再加入一定量NO,平衡后NO的转化率______________(填“变大”、“变小”或“不变”)。 ③反应开始至达到平衡的过程中,容器中下列各项发生变化的是______________(填序号)。 a.混合气体的密度 b.逆反应速率 c.单位时间内,N2和NO的消耗量之比 d.气体的平均相对分子质量 (3)氢气作为一种理想燃料,但不利于贮存和运输。利用氢能需要选择合适的储氢材料,镧镍合金在一定条件下可吸收氢气形成氢化物:LaNi5(s)+3H2(g) A.增加LaNi5H6(s)的量 B.升高温度 C.使用催化剂 D.减小压强 |
|
| 10. 综合题 | 详细信息 |
工业上可用软锰矿(主要成分是MnO2)和黄铁矿(主要成分是FeS2)为主要原料制备高性能磁性材料碳酸锰(MnCO3)。其工业流程如下: 回答下列问题: (1)为了提高溶浸工序中原料的浸出率,除了可以搅拌、将矿石研磨粉碎以外,可以采取的措施有(写两条)________________。 (2)副产品A的化学式是________________。 (3)净化工序的目的是除去溶液中的Cu2+、Ca2+等杂质。若测得滤液中c(F-)=0.01 mol·L-1,则滤液中残留的c(Ca2+)=________________〔已知:Ksp(CaF2)=1.46×10-10〕。 (4)沉锰工序中,加入NH4HCO3后有无色无味的气体放出,同时有浅红色的沉淀生成,发生反应的离子方程式是________________;沉锰工序中判断沉淀已经洗涤干净的实验操作是________________。 (5)已知MnCO3难溶于水和乙醇,潮湿时易被空气氧化,100℃开始分解。工业上一般用少量C2H5OH洗涤的原因是________________。 (6)溶浸过程中发生的主要反应如下,请完成并配平该反应的离子方程式:_____________ FeS2+_____________ MnO2+_____________ =_____________ Fe3++_____________ Mn2++_____________ SO42-+_____________ ,___________________ |
|
| 11. 填空题 | 详细信息 |
|
前四周期元素A、B、C、D、E、F原子序数依次递增。已知:A、B、D、C的价电子数依次增多,A、B、C同周期且C是该周期中电负性最大的元素;A有两个单电子,E的未成对电子数是前四周期中最多的,且其价电子数与D相同, F的最外层电子数为2,内层全部排满。请用对应的元素符号回答下面的问题: (1)写出E的价电子排布式:______________。 (2)在A形成的化合物中,A采取sp2杂化,且分子量最小的化合物为(写化学式)______________。 (3)下列物质的性质与氢键有关的是______________。 A. 可燃冰的形成 B. A的氢化物的沸点 C. B的氢化物的热稳定性 (4)E3+可以与AB—形成配离子,其中E3+以d2sp3方式杂化,杂化轨道全部用来与AB—形成配位键,则E3+的配位数为______________,1mol该配离子中含有______________molσ键。 (5)F与D形成的化合物晶胞如图,F的配位数为______________,晶体密度为a g/cm3,NA为阿伏加德罗常数,则晶胞边长为______________pm。(1pm=10-10cm)  |
|
最近更新



