江苏省镇江正兴学校2020-2021年高一上半期期中考试化学网上检测无纸试卷带答案和解析
| 1. 选择题 | 详细信息 |
|
古诗词很浪漫且充满了艺术魅力,成语俗语等脍炙人口,都是中华民族文化中的瑰宝。下列诗词、语句中包含的化学反应既是离子反应又是氧化还原反应的是( ) A. 粉身碎骨浑不怕,要留清白在人间。 B. 曾青得铁则化为铜 C. 春蚕到死丝方尽,蜡炬成灰泪始干。 D. 水滴石穿 |
|
| 2. 选择题 | 详细信息 |
|
下列物质中,属于纯净物的是 A.氯水 B.液氯 C.盐酸 D.漂白液 |
|
| 3. 选择题 | 详细信息 |
|
A. C. |
|
| 4. 选择题 | 详细信息 |
|
下列是对某溶液进行离子检测的方法和结论,其中正确的是( ) A.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液 B.加入足量的 BaCl2 溶液,产生白色溶液,则溶液中一定含有大量的 SO C.加入 NaOH 溶液后加热产生能使湿润红色石蕊试纸变蓝的气体,则溶液中一定含有大量的 NH D.先加入适量的盐酸酸化,再加入AgNO3溶液,产生白色沉淀,则溶液中一定含有大量的 Cl- |
|
| 5. 选择题 | 详细信息 |
完成下列实验所需选择的装置或仪器都正确的是( ) A.分离植物油和氯化钠溶液选用① B.除去氯化钠晶体中混有的氯化铵晶体选用② C.分离四氯化碳中的溴单质选用③ D.除去二氧化碳气体中的氯化氢气体选用④ |
|
| 6. 选择题 | 详细信息 |
|
有关氧化还原反应的说法正确的是 A.在氧化还原反应中,金属单质只体现还原性,金属阳离子只体现氧化性 B.物质所含元素化合价变化是判断氧化还原反应的依据 C.在一个氧化还原反应中,有一种元素被氧化,必有另一种元素被还原 D.某元素在反应中由化合物转化为单质,该元素一定被氧化 |
|
| 7. 选择题 | 详细信息 |
|
下列说法正确的是 ( ) A.氯气不具有漂白性,不能使鲜花褪色 B.NH3、CO2的水溶液均能导电,所以NH3、CO2均是电解质 C.用玻璃棒蘸取氯水滴到pH试纸的中央然后与标准比色卡对照读出pH值 D.分散系中分散质粒子的直径:Fe(OH)3 悬浊液>Fe(OH)3 胶体>FeCl3 溶液 |
|
| 8. 选择题 | 详细信息 |
|
关于钠及其化合物性质的叙述,正确的是 ( ) A.工业上用金属钠制备烧碱 B.氧化钠和过氧化钠都能与二氧化碳反应,生成物完全相同 C.过氧化钠是淡黄色固体,可用于呼吸面具中作为氧气的来源 D.碳酸钠可用于治疗胃酸过多 |
|
| 9. 选择题 | 详细信息 |
|
下列有关Na2CO3和 NaHCO3说法正确的是( ) A.相同温度下,同浓度的Na2CO3溶液与NaHCO3溶液相比较,后者碱性强 B.Na2CO3的热稳定性小于 NaHCO3 C.常温下,Na2CO3的溶解度大于 NaHCO3 D.用Ca(OH)2溶液可鉴别Na2CO3溶液和 NaHCO3溶液 |
|
| 10. 选择题 | 详细信息 |
|
用NA表示阿伏加德罗常数的值。下列说法正确的是 ( ) A.钠在空气中燃烧,23g钠充分燃烧时转移电子数为NA B.1.8g的NH4+中含有的电子数为1.1NA C.标准状况下,22.4 L水中含有的分子数目为NA D.1mol/LMgCl2溶液中含有2mol Cl- |
|
| 11. 选择题 | 详细信息 |
|
漂白粉的使用原理:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,该反应属于 A. 分解反应 B. 复分解反应 C. 化合反应 D. 置换反应 |
|
| 12. 选择题 | 详细信息 |
|
某溶液中存在大量的Na+、OHˉ、Clˉ、 A. |
|
| 13. 选择题 | 详细信息 |
|
我国“四大发明”在人类发展史上起到了非常重要的作用,其中黑火药的爆炸反应为:2KNO3+S+3C =K2S+N2↑+3CO2↑,有关该反应说法正确的是:( ) A.只有 KNO3 是氧化剂 B.C 是氧化剂 C.KNO3 和 S 都发生了还原反应 D.每生成1.5molCO2,该反应转移 12 mol 电子 |
|
| 14. 选择题 | 详细信息 |
|
将一小块钠投入盛硫酸铜溶液的试管里,不可能观察到的现象是( ) A.熔成小球并在液面上游动 B.有气体生成 C.溶液底部有银白色物质生成 D.生成蓝色沉淀 |
|
| 15. 选择题 | 详细信息 |
|
下列关于氯气的叙述,不正确的是( ) A. 氯气是黄绿色,有刺激性气味的气体 B. 氯气、液氯和氯水是同一种物质 C. 氯气能溶于水 D. 氯气是一种有毒的气体 |
|
| 16. 选择题 | 详细信息 |
|
ClO2是一种消毒杀菌效率高、二次污染小的水处理剂。实验室可通过以下反应制得 ClO2:2KClO3+H2C2O4+H2SO4 =2ClO2↑+K2SO4+2CO2↑+2H2O。下列说法正确的是( ) A.KClO3在反应中得到电子 B.KClO3被氧化 C.H2C2O4在反应中被还原 D.2molKClO3参加反应有 1mol 电子转移 |
|
| 17. 选择题 | 详细信息 |
|
下列各组离子在指定溶液中一定能大量共存的是( ) A.强碱性溶液: Na+ 、 Mg2+、Cl-、SO B.无色溶液: K+、H+、SO C.含大量SO D.强碱溶液: K+ 、 Al3+、Cl-、 NO |
|
| 18. 选择题 | 详细信息 |
|
能正确表示下列化学反应的离子方程式的是 A.氢氧化钡溶液与硫酸反应Ba2++OH-+H++ B.澄清的石灰水与稀盐酸反应 Ca(OH)2+2H+=Ca2++2H2O C.铜片插入硝酸银溶液中 Cu+Ag+=Cu2++Ag D.碳酸钙溶于稀盐酸中CaCO3+2H+=Ca2++H2O+CO2↑ |
|
| 19. 选择题 | 详细信息 |
|
为了除去硝酸钾晶体中所含的硫酸钙和硫酸镁,先将它配成溶液,然后加入KOH、K2CO3、Ba(NO3)2等试剂,配以过滤、蒸发结晶等操作,制成纯净的硝酸钾晶体,其加入试剂的顺序正确的是( ) A.Ba(NO3)2—KOH—K2CO3—HNO3 B.Ba(NO3)2—KOH—HNO3—K2CO3 C.KOH—K2CO3—Ba(NO3)2—HNO3 D.K2CO3—Ba(NO3)2—KOH—HNO3 |
|
| 20. 选择题 | 详细信息 |
|
现有24 mL浓度为0.05 mol·L-1的Na2SO3溶液恰好与20 mL浓度为0.02 mol·L-1的K2Cr2O7溶液完全反应,已知Na2SO3可被K2Cr2O7氧化为Na2SO4,则元素Cr在还原产物中的化合价为( ) A.+2 B.+3 C.+4 D.+5 |
|
| 21. | 详细信息 |
由中学常见的含钠元素的物质 A、B、C、D,存在如图转化关系(部分生成物和反应条件已略去)。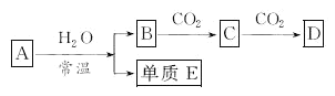 (1)若A为金属钠,则E为_____,A与水反应的离子方程式为_____。 (2)若A为过氧化钠,则 E 为_____,A 与水反应的化学方程式为_____。 (3)过氧化钠是碱性氧化物吗?_____(填“是”或“不是”),过氧化钠中氧元素化合价是_____。 (4) A不论是Na还是Na2O2,依据转化关系判断物质 C 是_____, 物质 D 是_____。 |
|
| 22. 实验题 | 详细信息 |
某校化学实验兴趣小组为了探究在实验室制备 Cl2 的过程中有水蒸气和 HCl 挥发出来,同时证明 Cl2的某些性质。甲同学设计了如图所示的实验装置(部分支撑用的铁架台省略)。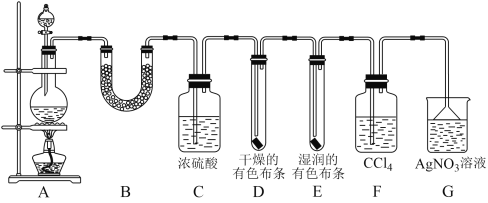 按要求回答下列问题。 (1)若用浓盐酸与足量的 MnO2反应制取 Cl2,写出 A 中化学反应方程式_____。 (2)①装置 B 中盛放的试剂名称为_____,作用是_____,现象是_____。 ②装置 D 和 E 中出现的不同现象说明的问题是_____。 ③装置 F 的作用是_____。 ④写出装置 G 中发生反应的离子方程式_____。 (3)乙同学认为甲同学设计的实验有缺陷,不能确保最终通入 AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入 AgNO3 溶液中的气体只有一种,乙同学提出在某两个装置之间再加一个装置。你认为该装置应加在_____与_____之间(填装置 字母序号),装置中应放入_____(填试剂或用品名称)。 |
|
| 23. 实验题 | 详细信息 |
|
某次实验需用480mL、0.5mol/L 的稀H2SO4溶液,某同学用98%的浓H2SO4(ρ=1.84g/cm3)进行配制,请回答下列问题: (1)实验需要的玻璃仪器除了烧杯、量筒、玻璃棒,还有________________________; (2)计算:98%的浓H2SO4(ρ=1.84g/cm3)的物质的量浓度为__________,配制本次实验需要的稀硫酸需用量筒量取上述98%的浓H2SO4___________________ mL (3)配制过程:①用量筒量取所需的浓硫酸 ②将浓硫酸缓缓注入盛有适量蒸馏水的烧杯中,边加边搅拌 ③用玻璃棒引流将烧杯中的溶液转移到已经检漏的合适规格的容量瓶中 ④洗涤烧杯和玻璃棒2~3次,洗涤液也注入容量瓶中.轻轻摇动容量瓶,使溶液混合均匀 ⑤向容量瓶中加入蒸馏水,在距离刻度1~2cm时,改用胶头滴管加蒸馏水至刻度线 ⑥盖好瓶塞,反复上下颠倒,摇匀 ⑦将配制好的溶液转移至试剂瓶中待用。 上述配置溶液的步骤存在缺失,缺少的步骤是_____________________,应放在步骤_____之前进行(填“序号”)。 (4)在横线上填写下列各种情况对所配制溶液浓度的影响(选填“偏高”、“偏低”或“无影响”). ①所用的浓硫酸长时间放置在密封不好的容器中_________; ②量取浓硫酸所用量筒有蒸馏水_________; ③定容时,俯视液面_________; ④用量筒量取浓硫酸时仰视液面___________。 |
|
最近更新



