2019-2020年高一12月月考化学题开卷有益(湖南省邵阳市双清区十一中)
| 1. 选择题 | 详细信息 |
|
以下是一些常用危险化学品的标志,加油站应贴的危险化学品标志是( ) A.  遇湿易燃物品 B. 遇湿易燃物品 B. 氧化剂 C. 氧化剂 C. 剧毒品 D. 剧毒品 D. 易燃液体 易燃液体 |
|
| 2. 选择题 | 详细信息 |
|
下列仪器不能直接用于加热的是 ( ) A.试管 B.蒸发皿 C.容量瓶 D.坩埚 |
|
| 3. 选择题 | 详细信息 |
|
为检验某溶液中是否含有Fe3+,可以选择的试剂是( ) A. KSCN溶液 B. AgNO3溶液 C. 酸性KMnO4溶液 D. BaCl2溶液 |
|
| 4. 选择题 | 详细信息 |
|
下列分散系中,分散质粒子大小在1~100nm之间的是( ) A. 泥水 B. 油水 C. Fe(OH)3胶体 D. CuSO4溶液 |
|
| 5. 选择题 | 详细信息 |
|
下列物质中,不属于电解质的是 A. NaOH B. H2SO4 C. 蔗糖 D. NaCl |
|
| 6. 选择题 | 详细信息 |
|
下列物质中,属于钾盐的是( ) A.K B.K2O C.KOH D.K2SO4 |
|
| 7. 选择题 | 详细信息 |
|
Fe2O3+3CO A.Fe B.CO C.Fe2O3 D.CO2 |
|
| 8. 选择题 | 详细信息 |
|
下列各组中的离子,能在溶液中大量共存的是( ) A. K+、H+、SO42-、OH- B. Na+、Cu2+、Cl-、SO42- C. Na+、H+、Cl-、CO32- D. Na+、Ca2+、CO32-、NO3- |
|
| 9. 选择题 | 详细信息 |
|
0.5 mol Na2CO3中所含的Na+数约为( ) A.3.01×1023 B.6.02×1023 C.0.5 D.1 |
|
| 10. 选择题 | 详细信息 |
|
将30 mL 0.5mol/L的NaOH溶液加水稀释到500 mL,稀释后NaOH的物质的量浓度为( ) A.0.3 mol/L B.0.03 mol/L C.0.05 mol/L D.0.04 mol/L |
|
| 11. 选择题 | 详细信息 |
|
下列各组物质混合后,不能生成NaOH的是 A.Na和H2O B.Ca(OH)2溶液和NaCl溶液 C.Na2O2和H2O D.Ca(OH)2溶液和Na2CO3溶液 |
|
| 12. 选择题 | 详细信息 |
|
下列电离方程式中,正确的是 A. Na2SO4=2Na++S04-2 B. Ba(OH)2=Ba2++OH-2 C. Al2(SO4)3=2A13++3SO42- D. Ca(N03)2=Ca2++2(N03) 2- |
|
| 13. 选择题 | 详细信息 |
|
下列离子方程式中,正确的是( ) A.稀盐酸滴在铜片上:Cu + 2H+ = Cu2+ + H2↑ B.稀盐酸滴在石灰石上:CO32— + 2H+= H2O + CO2↑ C.铁片插入硫酸铜溶液中:Fe + Cu2+ = Fe3+ + Cu+ D.稀盐酸滴入氢氧化钠中:H+ + OH- = H2O |
|
| 14. 选择题 | 详细信息 |
|
把铁片放入下列溶液中,铁片溶解,溶液质量增加,但没有气体放出的是( ) A.稀硫酸 B.Fe2(SO4)3溶液 C.CuSO4溶液 D.AgNO3溶液 |
|
| 15. 选择题 | 详细信息 |
|
物质的量浓度相同的 A.1:1:1 B.3:2:1 C.1:2:3 D.3:4:3 |
|
| 16. 选择题 | 详细信息 |
|
下列各组物质中,所含分子数相同的是( ) A.10g H2 和10g O2 B.9g H2O 和0.5mol Br2 C.5.6L N2(非标准状况)和11g CO2 D.224mLH2 (标准状况)和0.1mol N2 |
|
| 17. 选择题 | 详细信息 |
|
检验某无色透明溶液中是否含有SO42-时,先加入( )再加入BaCl2溶液。 A.HNO3 B.HCl C.H2SO4 D.AgNO3 |
|
| 18. 选择题 | 详细信息 |
|
当光束通过下列分散系: ①有尘埃的空气 ②稀硫酸 ③蒸馏水 ④墨水,能观察到有丁达尔效应的是( ) A. ①② B. ②③ C. ①④ D. ②④ |
|
| 19. 选择题 | 详细信息 |
|
在SiO2+3C A.36∶30 B.60∶36 C.2∶1 D.1∶2 |
|
| 20. 选择题 | 详细信息 |
|
少量的金属钠长期暴露在空气中,它的最终产物是( ) A.Na2O2 B.NaHCO3 C.Na2CO3 D.Na2CO3·10H2O |
|
| 21. 选择题 | 详细信息 |
|
把下列金属投入0.1 mol·L-1盐酸中,能发生反应且反应最剧烈的是( ) A.Na B.Fe C.Mg D.Al |
|
| 22. 选择题 | 详细信息 |
|
下列说法中正确的是 ( ) A.NaHSO4显强酸性,因此从组成上分类它应该属于酸 B.含Fe元素质量分数为70%的Fe2O3是纯净物 C.CuSO4·5H2O是混合物 D.显碱性的物质一定为碱 |
|
| 23. 选择题 | 详细信息 |
|
下列有关胶体的说法中正确的是( ) A.胶体都是均匀透明的液体 B.胶体粒子很小,可以透过半透膜 C.利用丁达尔效应可以鉴别胶体和溶液 D.纳米材料的粒子直径一般从几纳米至几十纳米,因此纳米材料是胶体 |
|
| 24. 选择题 | 详细信息 |
|
下列关于阿伏加德罗常数(NA)的说法中正确的是( ) A.1 mol任何物质都含有NA个分子 B.0.5 mol H2O中含有的原子数目为1.5NA C.32 g O2和O3的混合气体中含有的氧原子数无法确定 D.1 mol氖气中含有2NA个氖原子 |
|
| 25. 选择题 | 详细信息 |
|
把一定量铁粉放入氯化铁溶液中,完全反应后,所得溶液中Fe2+和Fe3+的溶度恰好相等,则已反应的Fe3+和未反应的Fe3+的物质的量的比为( ) A.2:1 B.2:3 C.3:2 D.1:2 |
|
| 26. 填空题 | 详细信息 |
|
物质的性质决定了物质的用途,下面列出了金属的几种性质,请在下列金属用途后的横线上填上金属性质对应的序号。 ①导热性 ②导电性 ③还原性 ④延展性 ⑤具有金属光泽 (1)用铝锭制成包装用的铝箔________________________。 (2)用铝制成的高压铝锅____________________________。 (3)用铁粉回收照相业废液中的银____________________。 (4)电信业中大量使用的铜丝、金属电缆________________。 |
|
| 27. 填空题 | 详细信息 |
2015年“探险队员”——盐酸,不小心走进了化学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或者是水溶液),盐酸必须避开它们,否则就无法通过。 (1)请你帮助它走出迷宫:(请用图中物质前的序号连接起来表示所走的路线)______________。 (2)在能“吃掉”盐酸的化学反应中,属于酸碱中和反应的有______个,属于氧化还原反应的有____个。其中能“吃掉”盐酸的盐是__________(填物质名称),写出该反应的离子方程式_______________; (3)在不能与盐酸反应的物质中,属于电解质的是___________(填写物质序号)。 |
|
| 28. 计算题 | 详细信息 |
|
有一镁铝合金共51 g,把其加入到1 L 5 mol·L-1的盐酸中,恰好反应完。 (1)关于合金的下列说法正确的有________。 A.合金只能由两种或两种以上的金属组成 B.合金的硬度一般比其组成成分金属的硬度大 C.镁铝熔成合金的过程是一个化学过程 D.合金的熔点一般比其组成成分的熔点低 E.合金具备金属的特性 (2) 该合金中镁铝的质量分别为________g、________g。 (3) 反应中共收集到标况下的氢气的体积为___________L。 (4)向反应后的溶液中逐滴加入5 mol·L-1的NaOH溶液,若要使沉淀恰好达到最大值,需要加入NaOH________L。 |
|
| 29. 推断题 | 详细信息 |
|
有4种钠的化合物W、X、Y、Z,它们之间存在如下关系: ①W ②Z+CO2→X+O2 ③Z+H2O→Y+O2↑ ④X+Ca(OH)2→Y+CaCO3↓ 试回答下列问题: (1) W、X、Y、Z的化学式分别是:W:________,X:________,Y:________,Z:________。 (2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是________(写化学式)。 (3)若④反应在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化学反应的化学方程式: ①离子方程式:______________________________________________。 ②化学方程式:________________________________________________。 |
|
| 30. 实验题 | 详细信息 |
以下为配制250 mL 0.2 mol·L-1 Na2CO3溶液的示意图。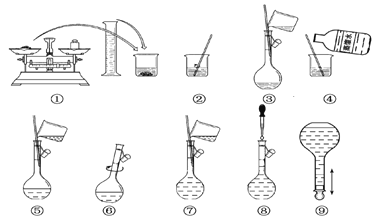 回答下列问题: (1)在容量瓶的使用方法中,下列操作不正确的是________。 A.使用容量瓶前检查它是否漏水 B.容量瓶用蒸馏水洗净后,再用待配溶液润洗 C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2 cm处,用滴管滴加蒸馏水到标线 D.配制溶液时,如果试样是液体,用量筒量取试样后直接倒入容量瓶中,缓慢加入蒸馏水到接近标线1~2 cm处,用滴管滴加蒸馏水到标线 E.盖好瓶塞,用食指顶住瓶塞,用另一只手的手指托住瓶底,把容量瓶倒转并摇动多次 (2)①中称得Na2CO3________g。 (3)玻璃棒在②、③两步中的作用分别是________、________。 (4)若出现如下情况,所配溶液浓度偏低的有:________ A.某同学在第⑧步观察液面时仰视; B.没有进行操作步骤④和⑤; C.在第⑤步不慎有少量液体流到容量瓶外; D.在步骤①中,药品放在右盘,砝码放在左盘(使用游码)。 |
|
最近更新



