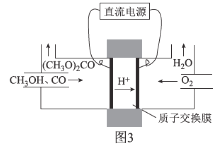
辽宁省葫芦岛市2020届高三第一次模拟考试(全国II)理综化学试卷
| 1. 选择题 | 详细信息 |
|
在2020年抗击新型冠状病毒肺炎的战役中,化学品发挥了重要作用。下列说法中错误的是 A.医用消毒酒精中乙醇的浓度为75% B.“84”消毒液、二氧化氯泡腾片可用作环境消毒 C.生产医用防护口罩的原料聚丙烯纤维属于有机高分子材料 D.洗手液都能够杀死病毒起到消毒作用 |
|
| 2. 选择题 | 详细信息 |
已知有机物M在一定条件下可转化为N。下列说法正确的是 A.该反应类型为取代反应 B.N分子中所有碳原子共平面 C.可用溴水鉴别M和N D.M的一氯代物共7种 |
|
| 3. 选择题 | 详细信息 |
|
设NA表示阿伏加德罗常数的值。下列说法正确的是 A.Na2S2O3与H2SO4溶液混合产生22.4 L气体时转移电子数为2NA B.标准状况下,22.4 L环丙烷和丙烯的混合气体中所含共用电子对数为9NA C.常温下,1 L 0.5 mol/L CH3COONH4溶液的pH=7,则溶液中CH3COO-与NH4+的数目均为0.5NA D.50g质量分数为46%的乙醇溶液与足量的钠反应,放出H2的分子数目为0.25NA |
|
| 4. 选择题 | 详细信息 |
|
已知 A、B、C、D、E 是短周期中原子序数依次增大的五种元素,A、B 形成的简单化合物常用作制冷剂,D 原子最外层电子数与最内层电子数相等,化合物 DC 中两种离子的电子层结构相同,A、B、C、D 的原子序数之和是 E 的两倍。下列说法正确的是( ) A.原子半径:C>B>A B.气态氢化物的热稳定性:E>C C.最高价氧化对应的水化物的酸性:B>E D.化合物 DC 与 EC2 中化学键类型相同 |
|
| 5. 选择题 | 详细信息 | ||||||||||||||||||||
下列实验的现象与结论相对应的是
|
|||||||||||||||||||||
| 6. 选择题 | 详细信息 |
磷酸铁锂电池在充放电过程中表现出了良好的循环稳定性,具有较长的循环寿命,放电时的反应为:LixC6+Li1—xFePO4=6C+LiFePO4 。某磷酸铁锂电池的切面如下图所示。下列说法错误的是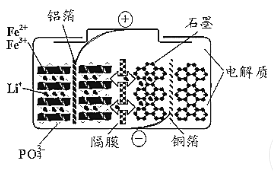 A.放电时Li+脱离石墨,经电解质嵌入正极 B.充电时电子从电源经铝箔流入正极材料 C.隔膜在反应过程中只允许Li+ 通过 D.充电时电池正极上发生的反应为:LiFePO4-xe-== Li1-xFePO4+xLi+ |
|
| 7. 选择题 | 详细信息 |
298K时,向20mLcmol·L-1KOH溶液中滴加0.1mol·L-1HCOOH溶液,混合溶液中水电离的氢氧根离子浓度与滴加甲酸(弱酸)溶液体积(V)的关系如图所示。下列说法正确的是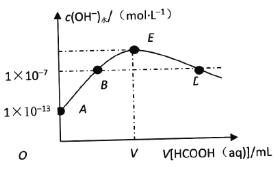 A. 上述KOH溶液的浓度c=0.01mol·L-1 B. B点对应的溶液中:c(K+)=c(HCOO-) C. E点对应的溶液中:c(OH-)>c(H+)=c(HCOOH) D. 若D点对应的甲酸溶液体积为V1mL,则HCOOH电离平衡常数 |
|
| 8. 综合题 | 详细信息 | ||||||
|
工业上可用一氧化碳合成可再生能源甲醇。 (1)已知:Ⅰ.3CO(g)+6H2(g) Ⅱ.3CH3OH(g) 则CO与H2合成气态甲醇的热化学方程式为___________________________________ (2)某科研小组在Cu2O/ZnO作催化剂的条件下,在500℃时,研究了n(H2)∶n(CO)分别为2∶1、5∶2时CO的转化率变化情况(如图1所示),则图中表示n(H2)∶n(CO)=2∶1的变化曲线为________(填“曲线a”或“曲线b”),原因是_________________。 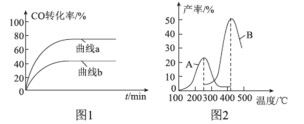 (3)某科研小组向密闭容器中充入一定量的CO和H2合成气态甲醇,分别在A、B两种不同催化剂作用下发生反应,一段时间后测得CH3OH的产率与温度的关系如图2所示。下列说法正确的是____________(填选项字母)。 a.使用催化剂A能加快相关化学反应速率,但催化剂A并未参与反应 b.在恒温恒压的平衡体系中充入氩气,CH3OH的产率降低 c.当2v(CO)正=v(H2)逆时,反应达到平衡状态 (4)一定温度下,在容积均为2L的两个恒容密闭容器中,按如下方式加入反应物,一段时间后达到平衡。
|
|||||||
| 9. | 详细信息 |
2019年诺贝尔化学奖颁给了为锂电池发展作出突出贡献的三位科学家。某废旧锂电池正极主要由LiFePO4、铝箔、炭黑等组成,Fe、Li、P具有极高的回收价值,具体流程如下: (1)过程ⅰ生成NaAlO2溶液的离子方程式是__。 (2)过程ⅱ中HCl/H2O2的作用是__。 (3)浸出液X的主要成分为 Li+、Fe3+、H2PO4-等。过程ⅲ控制碳酸钠溶液浓度20%、温度85 ℃、反应时间3 h条件下,探究pH对磷酸铁沉淀的影响,如图所示。 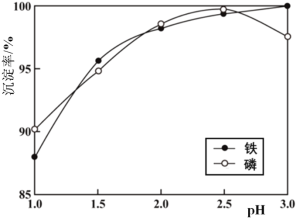 ①综合考虑铁和磷沉淀率,最佳pH为__。 ②结合平衡移动原理,解释过程ⅲ中pH增大,铁和磷沉淀率增大的原因__。 ③当pH>2.5后,随pH增加,磷沉淀率出现了减小的趋势,解释其原因__。 (4)LiFePO4可以通过(NH4)2Fe(SO4)2、H3PO4与LiOH溶液发生共沉淀反应制取,共沉淀反应的化学方程式为__。 |
|
| 10. 实验题 | 详细信息 | |||||||||||||||||
二氯化二硫(S2Cl2)是一种重要的化工原料,常用作橡胶硫化剂,改变生橡胶受热发黏、遇冷变硬的性质。查阅资料可知S2Cl2具有下列性质:
|
||||||||||||||||||
| 11. 综合题 | 详细信息 |
|
锌及锌的化合物应用广泛。例如,测定铜合金中的铅、锌时要利用锌配离子的下列反应: [Zn(CN)4]2-+4HCHO+4H2O==Zn2++4HOCH2CN+4OH-,回答下列问题: (1)基态Zn2+ 的电子排布式为_____________,基态 C原子核外电子占据_____个不同原子轨道。 (2)C、N、O三种元素的第一电离能由大到小的顺序为___________,HOCH2CN分子中含有的σ键与π键数目之比为_________。 (3)HCHO分子中碳原子轨道的杂化类型是________,福尔马林是HCHO的水溶液,HCHO极易与水互溶的主要原因是_________________________。 (4)[Zn(CN)4]2-中Zn2+与CN-之间的化学键称为_________,提供孤电子对的成键原子是________。 (5)Zn与S形成某种化合物的晶胞如图所示。 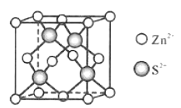 ①Zn2+填入S2-组成的___________空隙中; ②已知晶体密度为d g/cm3,该晶胞的边长表达式为______pm(写计算表达式)。 |
|
| 12. 综合题 | 详细信息 |
用于汽车刹车片的聚合物 Y 是一种聚酰胺纤维,合成路线如图: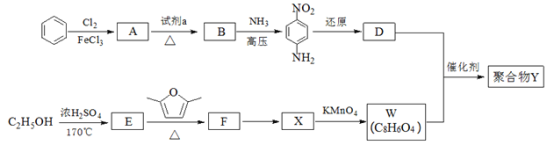 已知: (1)生成 A 的反应类型是_____。 (2)试剂 a 是_____。 (3)B 中所含的官能团的名称是_____。 (4)W、D 均为芳香化合物,分子中均只含两种不同化学环境的氢原子。 ①F 的结构简式是_____。 ②生成聚合物 Y 的化学方程式是_____。 (5)Q 是 W 的同系物且相对分子质量比 W 大 14,则 Q 有______种,其中核磁共振氢谱有4 组峰,且峰面积比为 1∶2∶2∶3 的为___________(写一种结构简式即可)。 (6)试写出由 1,3﹣丁二烯和乙炔为原料(无机试剂及催化剂任用)合成 |
|