上海2020年九年级化学上半年中考模拟在线答题
| 1. 选择题 | 详细信息 |
|
硅是制成光伏电池的重要材料,硅的元素符号是( ) A.Se B.Si C.Sl D.Sn |
|
| 2. 选择题 | 详细信息 |
|
70 周年庆典活动中属于化学变化的是( ) A.变化的队形 B.雄壮的军乐 C.行进的检阅车 D.威武的礼炮 |
|
| 3. 选择题 | 详细信息 |
|
属于可回收垃圾的是( ) A.饮料瓶 B.废弃的树叶 C.烟头 D.废旧荧光灯 |
|
| 4. 选择题 | 详细信息 |
|
将下面调味品加入水中,不能形成溶液的是 ( ) A. 食盐 B. 蔗糖 C. 味精 D. 芝麻油 |
|
| 5. 选择题 | 详细信息 |
|
属于氧化物的是( ) A.空气 B.液氧 C.水 D.碳酸钙 |
|
| 6. 选择题 | 详细信息 |
|
互为同素异形体的物质是( ) A.干冰与冰 B.金刚石和石墨 C.水银与银 D.氢气与液氢 |
|
| 7. 选择题 | 详细信息 |
|
触摸屏的材料之一是氧化铟。氧化铟(In2O3)中铟元素(In)的化合价为 A.0 B.+2 C.+3 D.+6 |
|
| 8. 选择题 | 详细信息 |
|
化学符号中“3”的含义表述正确的是( ) A.3H:3 个氢元素 B.O3:3 个氧原子 C.3N2:3 个氮分子 D.CO3:三氧化碳 |
|
| 9. 选择题 | 详细信息 |
|
用途利用其物理性质的是( ) A.金刚石作钻探机钻头 B.氧气用于炼钢 C.稀有气体用作保护气 D.二氧化碳用作气体肥料 |
|
| 10. 选择题 | 详细信息 |
|
氧气变成液氧时,分析正确的是( ) A.分子从运动到静止 B.分子间隔变小 C.分子种类发生变化 D.分子体积增小 |
|
| 11. 选择题 | 详细信息 | ||||||||||||
实验操作和目的对应关系错误的是( )
|
|||||||||||||
| 12. 选择题 | 详细信息 |
|
不随水的质量改变的是( ) A.物质的溶解度 B.溶质质量分数 C.溶液的 pH 值 D.饱和溶液的状态 |
|
| 13. 选择题 | 详细信息 |
|
具有启普发生器工作原理的装置是( ) A.  B. B.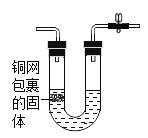 C.  D. D.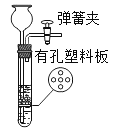 |
|
| 14. 选择题 | 详细信息 |
|
有关柠檬酸(C6H8O7)的说法正确的是( ) A.式量为 192g B.该物质中碳元素的质量分数最大 C.分子中碳、氢、氧三种原子的物质的量之比是 6:8:7 D.该物质由 6 个碳原子、8 个氢原子和 7 个氧原子构成 |
|
| 15. 选择题 | 详细信息 | |||||||||||||||
不能达到实验目的是( )
|
||||||||||||||||
| 16. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.0.5mol O2 含 6.02×1023 个氧 B.0.5mol NH3 中含 1.204×1023 个原子 C.等物质的量的 O3 比 O2 多 1 个氧原子 D.等质量的 CO 和 N2 所含原子数一样 |
|
| 17. 选择题 | 详细信息 |
在室温下将少量氧化钙加入到一定量的饱和氢氧化钙溶液中,搅拌并恢复到室温。图像中 x 代表时间,则 y 代表的是( )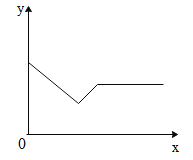 A.溶剂的质量 B.溶质的溶解度 C.溶质的质量 D.溶质的质量分数 |
|
| 18. 选择题 | 详细信息 |
|
已知某物质的以下数据,不能计算出该物质摩尔质量的是( ) A.微粒个数和质量 B.一个分子的真实质量 C.物质的量和质量 D.物质的量和微粒个数 |
|
| 19. 选择题 | 详细信息 |
|
有关“不一定”的说法正确的是( ) ①冷却热饱和溶液,不一定有晶体析出 ②在一定的条件下碳与氧气反应,不一定生成二氧化碳 ③能使紫色石蕊试液变蓝色的溶液,不一定是碱性溶液 ④化合物中的某种元素转变为单质,不一定要通过分解反应 A.①②④ B.①②③ C.②③④ D.①②③④ |
|
| 20. 填空题 | 详细信息 | ||||||||||||||||||
|
要使世界更美好,必须学好好学。 Ⅰ.化学使生活更健康。 (1)自来水往往通过沉淀、_____、吸附、消毒杀菌等方法净化获得。 (2)为了预防碘缺乏症的发生,我国提倡食用加碘食盐,其中的“碘”是指_____。 A单质 B分子 C原子 D元素 (3)柚子皮可以吸附室内异味,写出一种具有同样性质的化学物质的名称_____。 Ⅱ.化学使能源更环保。 (1)绿色能源氢气可由如图电解水实验装置得到。该反应的化学方程式是_____,基本反应类型_____。通电后观察到的现象_____;a中气体的检验方法是_____;保持氢气化学性质的最小微粒是_____(写名称);  常温常压下,氢气和氧气的密度分别为1、2,则生成氢气和氧气的物质的量之比为_____(列出1、2的关系式)。 (2)当前,世界已经迈向了“低碳”时代,公交系统推广使用节能减排的双燃料公交车这种公交车以天然气为主要燃料。 a.下图为天然气的主要成分甲烷完全燃烧的化学反应的微观示意图。 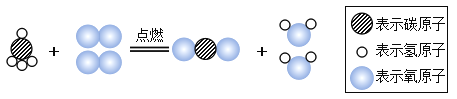 请根据示意图回答下列问题:从微粒观点分析,上述反应前后_____一定不变。反应的化学方程式是_____。 b.甲烷在一定量的氧气中燃烧,测得反应前后各物质的质量如下表所示:
|
|||||||||||||||||||
| 21. 填空题 | 详细信息 |
硝酸钾、氯化钾的溶解度曲线如图1所示。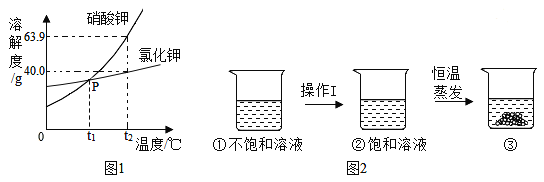 (1)P点的含义是_____。 (2)当温度_____℃时,硝酸钾的溶解度小于氯化钾的溶解度。 (3)t2℃时,分别将30g硝酸钾和氯化钾加入到50g水中,充分溶解后一定形成饱和溶液的是_____,其溶液的溶质质量分数为_____(精确到0.1%)。 (4)图2是有关硝酸钾溶液的实验操作及变化情况。若保持溶液的质量不变,操作Ⅰ为_____,操作Ⅱ“蒸发”还需的仪器有铁架台、酒精灯、_____。 (5)根据图1、图2,有关说法正确的是_____。 A①与②的溶质质量可能相等 B②与③的溶质质量分数一定相等 C等温度、等质量的硝酸钾和氯化钾饱和溶液,降低相同的温度,析出的晶体质量:硝酸钾>氯化钾 D等温度、等质量的硝酸钾和氯化钾饱和溶液,恒温蒸发等质量的水,析出的晶体质量:硝酸钾>氯化钾 |
|
| 22. 实验探究题 | 详细信息 |
为探究电解水产生的氢气化学性质,设计了如下实验: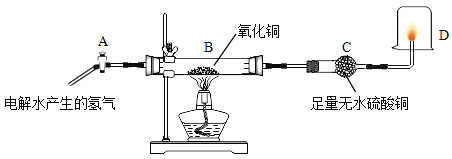 (1)用氢气还原氧化铜开始时的操作顺序是_____。 a.点燃B处酒精灯加热 b.检验氢气的纯度 c.打开A处活塞 (2)B处反应的化学方程式是_____;C处现象是_____,反应的化学方程式_____。 (3)点燃D处尖嘴导管口的气体,并在火焰上方罩一个冷而干燥的烧杯。则D处的现象是_____。 (4)该实验中体现了氢气的化学性质是_____。 (5)若要计算生成铜的质量,需测定的数据是_____。 a.通入的氢气质量 b.反应前后B装置的质量 c.反应前后C装置的质量 d.反应前后D装置的质量 |
|
| 23. 简答题 | 详细信息 |
利用下图提供的仪器装置回答问题: (1)若使用仪器A、D、E、F、_____(填字母)组装了一套制取氧气的装置,还需要添加_____(仪器名称)才能达到实验目的,该反应化学方程式是_____。实验过程中发现试管爆裂,可能的原因是_____(填以下字母)。 a.组装仪器时试管口略向上倾斜 b.先预热试管再对固体加热 c.加热时试管外壁有水珠 d.实验结束先导管移出水面再熄灭酒精灯 (2)若用大理石和稀盐酸制取较多量的二氧化碳,并能随时添加液体,组装一套制取装置所需的仪器是_____(填字母)。 (3)利用数据传感技术可以比较不同形状的碳酸钙与稀盐酸反应的速率。如图所示,某同学倾斜锥形瓶,使试管内稀盐酸流入瓶中与固体发生反应,瓶内气压随反应时间的变化如曲线所示,说法正确的是_____。  A曲线①的反应适合实验室制取CO2 B曲线②中b点溶液的溶质是CaCl2 C对比曲线中a、b两点可知,粉末状碳酸钙产生CO2更多 D对比曲线中c、d两点可知,粉末状碳酸钙产生CO2更多 (4)称取50g大理石放入烧杯中,然后向烧杯中加入50g的稀盐酸,大理石充分反应后烧杯中剩余物的质量为96.48g(假设大理石中的杂质不参与反应)。计算: a.产生二氧化碳的质量_____g; b.大理石中碳酸钙的物质的量_____mol(写出计算过程)。 |
|
| 24. 科学探究题 | 详细信息 | ||||||||||||||||||||||
|
兴趣小组在探究物质燃烧条件时,用一个集气瓶罩住燃着的小蜡烛,小蜡烛一会儿熄灭了。它为什么会熄灭呢? (提出猜想)甲同学说:蜡烛燃烧耗尽了瓶内的氧气,所以蜡烛熄灭。乙同学说:蜡烛燃烧后瓶内可能还有少量氧气,但有CO2浓度过高导致蜡烛熄灭。 (实验验证) 
|
|||||||||||||||||||||||
| 25. 实验探究题 | 详细信息 | |||||||||
兴趣小组用如下装置,进行有关碳及其氧化物的化学性质研究(图中夹持仪器已略)。
|
||||||||||



