2019届初三上半年段考化学考题(黑龙江省大庆五十五中)
| 1. 选择题 | 详细信息 |
|
如图所示的变化中,属于物理变化的是() A.  浓盐酸开口有白雾 B. 浓盐酸开口有白雾 B.  做分子运动实验 做分子运动实验C.  石墨制金刚石 D. 石墨制金刚石 D.  钟乳石的形成 钟乳石的形成 |
|
| 2. 选择题 | 详细信息 |
|
下列有关实验操作正确的是 A. 称量氢氧化钠固体时,将氢氧化钠固体直接放在纸上进行称量 B. 蒸发食盐水后,将蒸发皿立即直接放于实验桌上 C. 用10mL量筒量取7.5mL的蒸馏水 D. 稀释浓硫酸时将蒸馏水沿烧杯壁慢慢注入浓硫酸中,并用玻璃棒不断搅拌 |
|
| 3. 选择题 | 详细信息 |
|
掌握物质的分类是学好化学的基础,下列物质中都属于碱的是() A. NaCl、NaOH B. KOH、氨水 C. MgO、CuO D. Cu(OH)2、Cu2(OH)2CO3 |
|
| 4. 选择题 | 详细信息 |
|
下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是() A. 用过氧化氢溶液和二氧化锰制氧气2H2O2 B. 用天然气作燃料CH4+2O2 C. 用铁制容器盛放稀盐酸Fe+2HCl═FeCl2+H2↑ 置换反应 D. 用熟石灰制生石灰CaO+H2O═Ca(OH)2 化合反应 |
|
| 5. 选择题 | 详细信息 |
|
久置于空气中的石灰水,其表面会形成一层白膜.此时溶液的pH比变化前溶液的pH() A. 偏大 B. 偏小 C. 一样 D. 无法比较 |
|
| 6. 选择题 | 详细信息 |
|
将含有水蒸气和二氧化硫的空气依次通过氢氧化钠溶液、浓硫酸和灼热的铜网,剩下的气体是() ① 氮气 ② 二氧化碳 ③ 水蒸气 ④ 二氧化硫 ⑤ 氧气 ⑥ 惰性气体. A. ① ⑥ B. ① ② ⑥ C. ① ② ⑤ D. ① ② ③ ④ |
|
| 7. 选择题 | 详细信息 |
|
中和反应在生产和生活中有着广泛的应用.下列应用与中和反应原理一定无关的是( ) A. 服用含氢氧化铝的药物治疗胃酸过多症 B. 用稀硫酸处理印染厂的碱性废水 C. 在工业上,用熟石灰和纯碱制取烧碱 D. 在蚊虫叮咬处涂抹稀氨水可以减轻蚊虫分泌出的蚁酸造成的痛痒 |
|
| 8. 选择题 | 详细信息 |
|
有下列四组物质的转化关系:① Al→Al2(SO4)3② Fe2O3→FeSO4③ NaHCO3→Na2SO4④ Cu→CuSO4.其中加入稀硫酸能一步实现的共有() A. 1个 B. 2个 C. 3个 D. 4个 |
|
| 9. 选择题 | 详细信息 |
|
下列叙述中,不符合实验事实的是() A. 在K2CO3、K2SO4、AgNO3三种溶液中滴入BaCl2溶液,都有白色沉淀生成 B. 将CO2加入到滴有石蕊试液的蒸馏水中,溶液显红色 C. 未密封保存的苛性钠遇盐酸有气体生成 D. 将Cu(OH)2加入到滴有酚酞试液的蒸馏水中,溶液显红色 |
|
| 10. 选择题 | 详细信息 |
如图中甲、乙、丙是3种不同类别的物质,且均能与X发生化学反应.若X为稀盐酸,则甲、乙、丙3种物质可能为()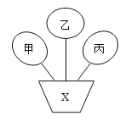 A. Fe、CuO、Cu(OH)2 B. Fe、CaCO3、Na2CO3 C. Zn、Fe2O3、Na2SO4 D. Cu、Ca(OH)2、CaCO3 |
|
| 11. 选择题 | 详细信息 |
取实验室中部分变质的NaOH样品配成溶液,向其中滴加稀盐酸,绘制出生成的CO2的质量与加入的盐酸的质量关系如图所示,下列有关说法正确的是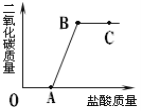 A.OA段没有发生任何化学反应 B.A点溶液中的溶质只有NaCl C.B点表示加入的盐酸与原溶液中的溶质恰好完全反应 D.C点的溶液的pH=7 |
|
| 12. 选择题 | 详细信息 | |||||||||||||||
某研究性学习小组为了探究氢氧化钠溶液与稀硫酸是否恰好完全反应,分别取少量反应后的溶液于试管中,用下表中的不同试剂进行实验。下列选项错误的是()
|
||||||||||||||||
| 13. 选择题 | 详细信息 |
|
下列有关溶液(固体溶质)的叙述,正确的是() A. 某物质的饱和溶液变为不饱和溶液,溶质的质量分数一定变小 B. 在一定温度下,同一物质的饱和溶液一定比不饱和溶液溶质的质量分数大 C. 任何物质的饱和溶液,当温度降低时一定会析出溶质 D. 饱和溶液析出晶体后,剩余溶液中溶质的质量分数一定变小 |
|
| 14. 选择题 | 详细信息 |
|
下列各组溶液,不用其他试剂就能鉴别出来的是() A. HCl、Na2CO3、CaCl2、HNO3 B. FeCl3、NaOH、MgSO4、HCl C. NaCl、NaOH、K2SO4、BaCl2 D. KNO3、AgNO3、KCl、NaCl |
|
| 15. 选择题 | 详细信息 |
|
向AgNO3溶液中加入一定质量的Al和Fe的混合粉末,充分反应后过滤,得到滤渣和浅绿色滤液。关于该滤渣和滤液有下列四种说法: ① 向滤渣中加入稀盐酸,一定有气泡产生。 ② 向滤液中加入稀盐酸,一定有沉淀产生。 ③ 滤渣中一定含有Ag。 ④ 滤液中一定含有Fe(NO3)2,一定不含AgNO3,可能含有Al(NO3)3 以上说法正确的个数为() A. 0个 B. 1个 C. 2个 D. 3个 |
|
| 16. 填空题 | 详细信息 |
|
用化学符号或化学方程式表示: (1)氨气________; (2)烧碱_________; (3)4个氢分子________; (4)澄清石灰水中溶质的化学式________; (5)氯化铁中的阳离子________; (6)碳酸钠和氢氧化钙反应_______; (7)一氧化碳还原氧化铁________; (8)硫酸铜和氢氧化钠反应________。 |
|
| 17. 简答题 | 详细信息 |
如图是氢氧化钠溶液和盐酸用滴加方式反应时,溶液pH随滴入溶液体积变化的曲线。 (1)氢氧化钠和盐酸恰好完全反应时,溶液的pH_____7(填“大于”或“小于”或“等于”)。 (2)根据曲线判断,该反应是将_____(填“氢氧化钠溶液”或“盐酸”,下同)滴入_____中,理由是_____。 (3)当滴入溶液的体积为5mL时,所得溶液中的溶质为_____(写化学式),若在此溶液中滴入石蕊试液,溶液显_____色。 |
|
| 18. 综合题 | 详细信息 |
|
氢氧化钠溶液久置在空气中会变质。 (1)其变质的原因是____________。(用化学方程式表示) (2)若要除去其中的杂质你会选择以下适量的 _______。 ①氯化钙溶液 ②氯化钡溶液 ③氢氧化钡溶液 |
|
| 19. 填空题 | 详细信息 |
|
如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同.结合此图回答下列问题: (1)稀硫酸中阳离子的符号是 ; (2)反应①中石蕊溶液变为 色; (3)反应⑤的化学方程式为 ; (4)图中只生成盐和水的反应有 (填序号); (5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、Na2CO3)中的 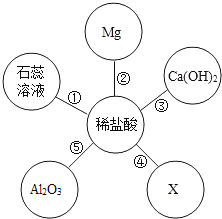 |
|
| 20. 填空题 | 详细信息 |
根据如图A、B、C三种固体的溶解度曲线回答: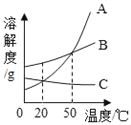 (1)20℃时,欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是A________B(填写“>”、“<”或“=”). (2)要在不改变溶质的质量分数的前提下使50℃时C的饱和溶液成为不饱和溶液,可采用的方法是________. (3)将50℃时三种物质的饱和溶液分别都降温到20℃,此时溶液中溶质的质量分数从大到小是________. (4)甲、乙两烧杯中分别装有50℃的100克和200克A的饱和溶液,若将两份溶液都降低到20℃,析出晶体质量的关系是甲________乙(填写“>”、“<”或“=”),若将两份溶液都恒温蒸发10克水,析出晶体质量的关系是甲________乙. (5)欲从混有少量A的B物质的饱和溶液中得到纯净的B晶体,应该采用的方法是________. |
|
| 21. 流程题 | 详细信息 |
有一包固体,可能含有碳酸钙、氧化铜、氧化铁、炭粉(炭粉的化学性质和一氧化碳相似)中的一种或几种.现做如图实验: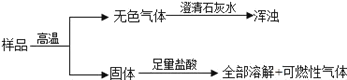 则原固体一定有________,一定没有________,可能有________. |
|
| 22. 科学探究题 | 详细信息 | ||||||||
|
实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂。此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究。 (1)写出该中和反应的化学方程式________。 (2)探究烧杯内溶液中溶质的成分: (提出问题)该烧杯内的溶液中溶质是什么? (进行猜想)(A)溶质可能是CaCl2与Ca(OH)2 (B)溶质可能只是CaCl2 (C)溶质可能是________。 (实验探究)①小明从烧杯中取了少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液。振荡。观察到酚酞试液不变色。于是他排除了猜想(A),你认为他排除猜想(A)的理由是________②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
|
|||||||||
| 23. 科学探究题 | 详细信息 | ||||||||||||
|
某化学兴趣小组在实验室里进行以下实验: 他们首先取溶质质量分数30%、密度为1.15g/mL的较浓盐酸40mL与60mL蒸馏水混合配制稀盐酸,跟石灰石反应制得气体,将此气体通入澄清石灰水,一直未见浑浊出现。为此,他们请教老师,老师建议他们为弄明原因进行实验探究。下面是他们探究的过程,请你帮助填答补充完整。 (提出问题)为什么制得的气体不能使石灰水变浑浊? (实验探究)
|
|||||||||||||
| 24. 计算题 | 详细信息 |
|
向100g硫酸铜溶液中,逐滴加入NaOH溶液,加入NaOH溶液的质量与生成沉淀的质量之间的关系如图所示,请回答下列问题。 (1)生成Cu(OH)2的质量为________g。 (2)将A点所对应的混合物过滤,滤液中所含溶质为________; (3)计算硫酸铜溶液中溶质的质量分数。________(请写出计算过程)  |
|