湖南省邵阳市邵东创新实验学校2020-2021年高二上学期期末考试化学免费试卷带答案和解析
| 1. 选择题 | 详细信息 |
贴有如图所示标志的容器中,可能装有 A.氯气 B.汽油 C.天然气 D.酒精 |
|
| 2. 选择题 | 详细信息 |
|
考古中常利用 A.6 B.8 C.14 D.20 |
|
| 3. 选择题 | 详细信息 |
我国科学家屠呦呦因提取抗疟药青蒿素而获得诺贝尔生理学或医学奖。已知青蒿素的结构如图所示,其分子式为C15H22O5,则青蒿素属于 A.单质 B.氧化物 C.无机物 D.有机物 |
|
| 4. 选择题 | 详细信息 |
|
含氮、磷的大量污水任意排放,会导致 A.水华、赤潮 B.雾霾 C.酸雨 D.光化学烟雾 |
|
| 5. 选择题 | 详细信息 |
|
下列烧杯中的液体,用激光笔照射时能产生丁达尔效应的是( ) A.蒸馏水 B.Fe(OH)3胶体 C.CuSO4溶液 D.NaCl溶液 |
|
| 6. 选择题 | 详细信息 |
|
下列气体溶于水,所得溶液呈酸性且电解质的是 A.SO2 B.CO2 C.HCl D.NH3 |
|
| 7. 选择题 | 详细信息 |
|
下列气体呈黄绿色的是 A.Cl2 B.H2 C.NO D.NO2 |
|
| 8. 选择题 | 详细信息 |
|
实验室里,下列物质常常保存在煤油中的是( ) A.Na B.Na2O2 C.NaOH D.NaCl |
|
| 9. 选择题 | 详细信息 |
|
下列过程所发生的反应中,属于吸热反应的是 A.木炭燃烧 B.酸碱中和 C.炸药爆炸 D.Ba(OH)2·8H2O和NH4Cl混合搅拌 |
|
| 10. 选择题 | 详细信息 |
|
已知:CH2=CH2+ Br2 A.取代反应 B.酯化反应 C.加成反应 D.氧化反应 |
|
| 11. 选择题 | 详细信息 |
|
工业上常用电解法治炼的金属是 A.Mg B.Fe C.Cu D.Ag |
|
| 12. 选择题 | 详细信息 |
|
下列物质中,含有离子键的是 A.O2 B.Na2O C.H2O D.HC1 |
|
| 13. 选择题 | 详细信息 |
|
为检验FeCl2溶液中是否含有Fe3+,可选择的试剂是 A.稀盐酸 B.AgNO3溶液 C.KSCN溶液 D.H2O2 |
|
| 14. 选择题 | 详细信息 |
根据反应:M+H2SO4 =MSO4+H2 ↑,可设计成如图所示的原电池,则电极材料M可选用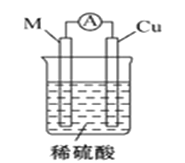 A.Cu B.Mg C.Ag D.石墨 |
|
| 15. 选择题 | 详细信息 |
|
已知合成氨的反应:N2+3H2 A.正逆反应速率相等 B.N2的转化率为100% C.H2的浓度为0 D.反应停止了 |
|
| 16. 选择题 | 详细信息 |
下列实验操作中,用于配制一定物质的量浓度的溶液操作是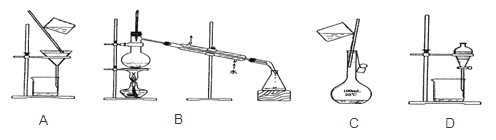 |
|
| 17. 选择题 | 详细信息 |
|
下列离子方程式中,正确的是 A.稀盐酸滴在碳酸钙上:CO B.稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ C.氯气通入氯化亚铁溶液中:Fe2++Cl2=Fe3++2Cl- D.钠与水的反应:2Na+2H2O=2Na++2OH-+H2↑ |
|
| 18. 选择题 | 详细信息 |
|
下列关于1molNH3的说法中,正确的是(NA表示阿伏加德罗常数的值) A.NH3的摩尔质量为17g B.含分子数为NA C.常温常压下的体积约为22.4L D.溶于1L水,所得溶液的物质的量浓度为1 mol·L-1 |
|
| 19. 填空题 | 详细信息 |
|
化学是一门实用性很强的科学。请根据题意填空: (1)钠有多种化合物,其中俗称“小苏打”的是___________ (填“Na2CO3”或“NaHCO3”) (2)铁有多种氧化物,其中可用做颜料、油漆的是___________ (填“Fe2O3”或“Fe3O4”) (3)铝制餐具不宜长时间存放酸性、碱性食物,但常温下铝制容器可以盛装___________(填“浓硫酸”或“浓盐酸”)。 |
|
| 20. 填空题 | 详细信息 |
|
化学与人类生活、生产密切相关。请根据题意填空: (1)我国5G通信技术处于世界领先地位,高速通信离不开光导纤维。用于制造光导纤维的基本原料是___________(填“SiO2”或“Si”) (2)“84”消毒液在新冠肺炎疫情防控中发挥了很大的作用。已知“84”消毒液的制备原理为Cl2 + 2NaOH=NaCl+NaClO + H2O,则“84”消毒液的有效成分为___________(填“NaCl”或“NaClO”) (3)在汽车排气管上安装催化转化装置,可使尾气中的NO和CO反应转化为无污染的物质。请完成一定条件该反应的化学方程式: 2CO + 2NO  N2 +2 ___________。 N2 +2 ___________。 |
|
| 21. | 详细信息 |
|
有机物A是常用来衡量一个国家石油化工发展水平的标志性物质,在一定条件下可发生下列转化: 请根据题意填空: (1)D中的官能团为___________(填“羟基”或“羧基”) (2)既能使溴的四氯化碳溶液褪色,又能使酸性高锰酸钾溶液褪色的_________ (填“A”或“B”) (3)C→D的反应类型为___________(填“氧化”或“还原”)反应。 |
|
| 22. 填空题 | 详细信息 | ||||||||||||||||||||||||||||||||||||||
下表是元素周期表的一部分,除标出的元素外,表中的每个编号代表一种元素。请根据要求回答问题:
(1)②的元素符号是___________ |
|||||||||||||||||||||||||||||||||||||||
| 23. 实验题 | 详细信息 |
海带中含有丰富的碘元素,某化学兴趣小组设计如下流程图提取碘: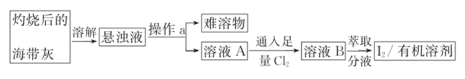 请回答下列问题: (1)操作a的名称是___________(填“过滤”或“蒸发”) (2)溶液A中通入足量Cl2的目的是将I-氧化为I2,也能达到该目的的物质是___________(填“双氧水”或“稀盐酸”) (3)在萃取时,可选用的萃取剂为___________(填“酒精”或“四氯化碳”) (4)已知I2与H2发生反应:I2(g)+H2(g) (5)当其他条件不变时,升高温度,该反应速率将___________(填“增大”或“减小”)。 |
|
| 24. 实验题 | 详细信息 |
已知反应:Cu+ 2H2SO4(浓)  请回答下列问题: (1)仪器a的名称是___________ (2)C中石蕊溶液变为___________(填“蓝色”或“红色”) (3)B中品红溶液褪色,说明SO2具有___________(填“漂白性”或“还原性”) (4)为防止SO2污染环境,D中可选用___________(填“NaOH”或“H2SO4”)溶液 (5)D中倒置漏斗的作用是___________。 |
|
最近更新



