汉中市免费检测试卷
| 1. 选择题 | 详细信息 |
|
关于粗盐提纯的下列说法正确的是 A. 溶解粗盐时,应多加水尽量使溶液稀些,防止食盐溶解不完全 B. 滤去不溶性杂质以后,将滤液移至坩埚内加热浓缩 C. 当蒸发到有大量晶体析出,剩有少量溶液时,停止加热,利用余热将液体蒸干 D. 将制得的晶体转移到新制过滤器中用大量水进行洗涤 |
|
| 2. 选择题 | 详细信息 |
|
设NA为阿伏加德罗常数,下列说法正确的是 ( ) A.2.4g金属镁变成镁离子时失去的电子数目为0.1 NA B.16g CH4所含原子数目为NA C.17g NH3所含电子数目为10 NA D.1.8g水所含质子数目为10 NA |
|
| 3. 选择题 | 详细信息 | ||||||||||||||||||||
下列实验中,所采取的分离方法与对应原理都正确的是 ( )
|
|||||||||||||||||||||
| 4. 选择题 | 详细信息 |
|
下列对于“摩尔”的理解正确的是 ( ) A. 摩尔是国际科学界建议采用的一种物理量 B. 摩尔是物质的量的单位,简称摩,符号为mol C. 摩尔可以把物质的宏观数量与微观粒子的数量联系起来 D. 国际上规定,0.012kg碳原子所含有的碳原子数目为1摩 |
|
| 5. 选择题 | 详细信息 |
|
下列示意图中,白球代表氢原子,黑球代表氦原子,方框代表容器,容器中间有一个可以上下滑动的隔板(其质量可忽略不计)。其中能表示等质量的氢气与氦气的是 A. 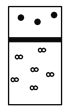 B. B.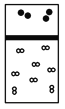 C. C. D. D. |
|
| 6. 选择题 | 详细信息 |
|
在两个容积相同的容器中,一个盛有氯化氢气体,另一个盛有氢气和氯气的混合气体。在同温同压下,两容器内的气体一定具有相同的( ) A.原子数 B.密度 C.质量 D.质子数 |
|
| 7. 选择题 | 详细信息 |
下列实验操作中,不合理的是( )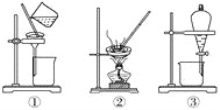 A. 洗涤沉淀时(如图①),向漏斗中加适量水,搅拌并滤干 B. 用CCl4提取碘水中的碘,选③ C. 蒸馏时蒸馏烧瓶中液体的体积不能超过容积的2/3,液体也不能蒸干 D. 粗盐提纯,选①和② |
|
| 8. 选择题 | 详细信息 |
|
同温同压下,两种气体的体积如果不同,其主要原因是 A.气体的分子大小不同 B.气体分子间的平均距离不同 C.气体的物质的量不同 D.气体的性质不同 |
|
| 9. 选择题 | 详细信息 |
|
某一K2SO4 和 Al2(SO4)3 的混合溶液,已知其中 Al3+的物质的量浓度为 0.4 mol/L, A.0.1 mol/L B.0.15 mol/L C.0.2 mol/L D.0.25 mol/L |
|
| 10. 选择题 | 详细信息 |
|
下列关于气体摩尔体积的说法正确的是( ) A. 22.4 L任何气体的物质的量均为1 mol B. 非标准状况下,1 mol任何气体不可能占有22.4 L体积 C. 0.1 mol H2、0.2 mol O2、0.3 mol N2和0.4 mol CO2组成的混合气体在标准状况下的体积约为22.4 L D. 标准状况下,1 mol CO和1 mol CO2的体积比为1∶2 |
|
| 11. 选择题 | 详细信息 |
|
设NA代表阿伏加德罗常数说法不正确的是( ) A.醋酸的摩尔质量(单位:g/mol)与NA个醋酸分子的质量在数值上相等 B.NA个氧分子和NA个氢分子的质量比等于16:1 C.28克氮气所含的原子数目为NA D.在标准状况下,0.5NA个氯气分子所占体积约为11.2L |
|
| 12. 选择题 | 详细信息 |
|
将下列溶液分别稀释到100 mL,稀释后的溶液中氯离子浓度最大的是 A. 15 mL 1 mol•L﹣1的AlCl3 B. 50 mL 1 mol•L﹣1的KCl C. 20 mL 2 mol•L﹣1的NH4Cl D. 10 mL 2 mol•L﹣1的CaCl2 |
|
| 13. 选择题 | 详细信息 |
|
在一定温度下,某饱和氢氧化钠溶液体积为 V mL,溶液密度为 d g•cm-3,质量分数为 w,物质的量浓度为 c mol•L-1,溶液中含氢氧化钠的质量为 m g。下列叙述错误的是( ) A.该温度下氢氧化钠的溶解度(S)为 B.溶液中溶质的物质的量浓度数值(c)为 C.溶液中溶质的物质的量浓度数值(c)为 25dw D.溶液中溶质的质量分数为 |
|
| 14. 选择题 | 详细信息 |
|
下列溶液中Cl-浓度与150 mL 1 mol·L-1 AlCl3溶液中Cl-浓度相等的是 A.100mL 1 mol·L-1的FeCl3溶液 B.75 mL 2 mol·L-1 NH4Cl溶液 C.100 mL 1.5mol·L-1的NaCl溶液 D.150 mL 1 mol·L-1的KCl溶液 |
|
| 15. 选择题 | 详细信息 |
|
在标准状况下①6.72L CH4 ②3.01×1023个HCl分子 ③13.6g H2S ④0.2mol NH3,下列对这四种气体的关系从大到小表示正确的是( ) a.体积:②>③>①>④ b.密度:②>③>④>① c.质量:②>③>①>④ d.氢原子个数:①>③>④>② A.abc B.bcd C.abcd D.acd |
|
| 16. 选择题 | 详细信息 | ||||||||||||||||||||
为除去下列物质中所含的杂质,所选用的试剂或操作方法不正确的是
|
|||||||||||||||||||||
| 17. 填空题 | 详细信息 |
|
(1)在标准状况下,由 CO 和 CO2组成的混合气体 8.96L,质量是 16g。此混合物中 CO 和 CO2的物质的量比是 ______________ ,CO 的体积分数是 __________,CO 的质量分数是 ___________,C 和 O 的原子个数比是 _____________,混合气体的平均摩尔质量是 _____________。 (2)19g 某二价金属的氯化物 ACl2中含有 0.4mol Cl-离子,ACl2的摩尔质量是 _____,相对分子质量是____________,A 的相对原子质量是 __________。 |
|
| 18. 实验题 | 详细信息 |
海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海洋植物植物中提取碘的流程如图: 某化学兴趣小组将上述流程②③设计成如图所示: 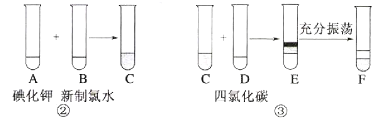 已知氯水中含有Cl2,②中发生反应的化学方程式为Cl2+2KI=2KCl+I2。 回答下列问题: (1)写出提取过程①③中实验操作的名称:①_____,③_____。 (2)四氯化碳是_____色、比水_____的液体。F中下层液体的颜色为______色,上层液体中溶质的主要成分为_____。 (3)从F中得到固态碘还需进行的操作是______。 (4)在灼烧过程中,将使用到的(除泥三角外)实验仪器有(________) A.试管 B.瓷坩埚 C.坩埚钳 D.蒸发皿 E.酒精灯 |
|
| 19. 实验题 | 详细信息 |
|
实验室欲用NaOH固体配制1.0mol•L﹣1的NaOH溶液240mL: (1)配制溶液时,一般可以分为以下几个步骤:①称量②计算③溶解④倒转摇匀⑤转移⑥洗涤⑦定容⑧冷却.其正确的操作顺序为_____,本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、还有_____。 (2)某同学欲称量一定量的NaOH固体,他先用托盘天平称量烧杯的质量,天平平衡后的状态如图.烧杯的实际质量为_____g,要完成本实验该同学应称出_____g NaOH。 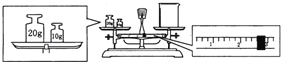 (3)使用容量瓶前必须进行的一步操作是_____。 (4)在配制过程中,其他操作都是正确的,下列操作会引起浓度偏高的是_____。 ①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面 ③容量瓶不干燥,含有少量蒸馏水 ④定容时俯视刻度线 ⑤未冷却到室温就将溶液转移到容量瓶并定容 ⑥定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线 |
|
| 20. 计算题 | 详细信息 |
|
常温下,在27.5g水中溶解12.5g CuSO4·5H2O,恰好达到饱和,该溶液密度为1.21g /cm3,求: (1)该溶液中CuSO4的物质的量浓度 (2)取出20.0 ml该溶液,配成浓度为1.00 mol/L的稀溶液,则稀释后溶液的体积是多少毫升? |
|
最近更新



