新乡市高一化学下册月考试卷摸底考试题
| 1. 选择题 | 详细信息 |
|
Se是人体必需微量元素,下列关于 A. C. |
|
| 2. 选择题 | 详细信息 |
|
一种比黄金贵百倍的818O2气体,不久前在兰州近代物理研究所制备成功。1mol818O2气体中所含中子的物质的量为 A.16mol B.18mol C.20mol D.24mol |
|
| 3. 选择题 | 详细信息 |
已知最外层电子数相等的元素原子具有相似的化学性质。氧元素原子的核外电子分层排布示意图为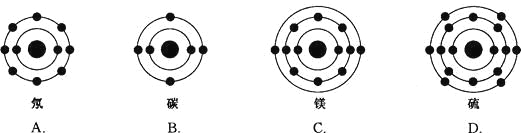 |
|
| 4. 选择题 | 详细信息 |
|
现有xMm- 和yNn+ 两种简单离子,它们的电子层结构相同。则表示M元素质子数的正确表达式是( ) A.x=y+n+m B.x=y-n-m C.x=y+n-m D.x=y-n+m |
|
| 5. 选择题 | 详细信息 |
|
A、B为同主族的两元素,A在B的上一周期,若A的原子序数为n,则B 的原子序数不可能为( ) A. n+8 B. n+18 C. n+32 D. n+20 |
|
| 6. 选择题 | 详细信息 |
|
已知碳有三种核素 12C、13C、14C,氧元素也有三种核素 16O、17O、18O,则由以上核素形成的不同CO2分子的分子量有( ) A.10种 B.8种 C.9种 D.7种 |
|
| 7. 选择题 | 详细信息 |
|
a、b、c、d、e是同周期的五种元素,a和b的最高价氧化物的水化物显碱性,且碱性b>a,c和d的气态氢化物的还原性d>c,五种元素的原子,得失电子后所形成的简单离子中,e的离子半径最小,则它们的原子序数由小到大的顺序是 A. b、a、e、d、c B. e、d、a、b、c C. a、b、d、c、e D. c、d、e、a、b |
|
| 8. 选择题 | 详细信息 |
|
已知X+、Y2+、Z―、W2―四种离子均具有相同的电子层结构。下列关于X、Y、Z、W四种元素的描述,不正确的是 A.原子半径:X>Y>Z>W B.原子序数:Y>X>Z>W C.原子最外层电子数:Z>W>Y>X D.还原性:X>Y,W2―>Z― |
|
| 9. 选择题 | 详细信息 | ||||||||||
已知下列元素的原子半径
|
|||||||||||
| 10. 选择题 | 详细信息 |
|
下列说法正确的是( ) A.含有共价键的化合物可能是共价化合物 B.在共价化合物中可能存在离子键 C.含有离子键的化合物中一定是没有共价键 D.难失电子的原子,获得电子的能力一定强 |
|
| 11. 选择题 | 详细信息 |
|
已知SO2和O2反应生成4mol SO3时放出的热量为Q kJ,那么2mol SO2和1mol O2在一有催化剂的密闭容器中发生反应时,放出的热量为( ) A.大于Q kJ B.等于Q kJ C.小于0.5Q kJ D.无法确定 |
|
| 12. 选择题 | 详细信息 |
|
人造地球卫星上使用的一种高能电池(银锌蓄电池),其电池的电极反应式为:Zn+2OH--2e-=ZnO+H2O,Ag2O+H2O+2e-=2Ag+2OH-。据此判断氧化银是( ) A. 负极,被氧化 B. 正极,被还原 C. 负极,被还原 D. 正极,被氧化 |
|
| 13. 选择题 | 详细信息 |
|
等物质的量的主族金属A、B、C分别与足量的稀盐酸反应,所得氢气的体积依次为VA、VB、VC,已知VB=2VC,且VA=VB+VC,则在C的生成物中,该金属元素的化合价为( ) A.+1 B.+2 C.+3 D.+4 |
|
| 14. 选择题 | 详细信息 |
一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列说法正确的是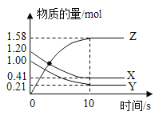 A.反应开始到10s,用Z表示的反应速率为 B.反应开始到10s,X的物质的量浓度减少了 C.反应开始到10s时,Y的转化率为 D.反应的化学方程式为: |
|
| 15. 选择题 | 详细信息 |
右图是一种检验某气体化学性质的实验装置,图中B为开关。 如先打开B,在A处通入干燥氯气,C中红色布条颜色无变化;当关闭B时,C处红色布条颜色褪去。则D瓶中盛有的溶液是( )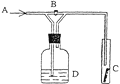 A.浓H2SO4 B.饱和食盐水 C.浓NaOH溶液 D.KI溶液 |
|
| 16. 选择题 | 详细信息 |
|
取一定量的甲烷与少量氧气混合点燃,生成CO、CO2和水蒸气的混合物49.6g,将燃烧混合物缓缓通过无水氯化钙并吸收完全,氯化钙的质量增加25.2g,由此可知甲烷不完全燃烧所得产物中碳的氧化物的总质量是( ) A.11.2g B.28g C.13.2g D.24.4g |
|
| 17. 选择题 | 详细信息 |
|
烷烃分子可以看作由以下基团组合而成:-CH3 -CH2- A.6 B.7 C.8 D.10 |
|
| 18. 填空题 | 详细信息 |
|
某简单微粒的结构示意图为 (1)若该微粒一般情况下不与其它元素的原子反应,这种微粒的符号是_______ (2)若该微粒有很强的氧化性,且只需得到一个电子就能达到稳定结构,这种微粒的结构示意图为________ (3)若该微粒为一价阳离子,且对应的碱为可溶性强碱,则x=_____y=_____。 |
|
| 19. 填空题 | 详细信息 | ||||||||||||
A、B、C均为短周期元素,在周期表中的位置如图所示:
|
|||||||||||||
| 20. 填空题 | 详细信息 |
(1)表中的实线是元素周期表部分边界,请在表中用实线补全元素周期表边界________。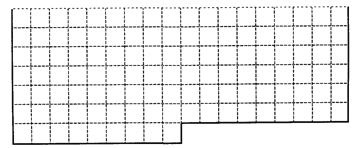 (2)元素甲是第三周期ⅥA族元素,请在方框中按氦元素的式样(如图)  写出元素甲的原子序数、元素符号、元素名称、相对原子质量。 ____ (3)元素乙的M层上有3个电子,则乙原子半径与甲原子半径比较:________>________(用元素符号表示),甲、乙的最高价氧化物水化物相互反应的离子方程式为:________ (4)元素周期表体现了元素周期律,即元素的性质随着_________的递增呈现____的变化。 |
|
| 21. 实验题 | 详细信息 |
某研究小组为制备消毒液(主要成分是NaClO)设计了下列装置,并查阅下列资料:在温度较高情况下卤素单质和碱溶液能发生如下反应:3X2+6OH-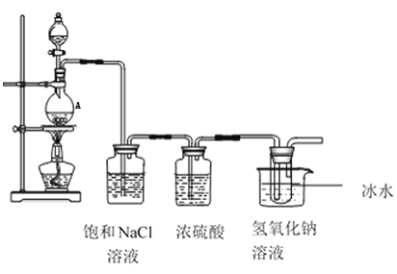 回答下列问题: (1)仪器 A的名称为_______发生装置中反应的离子方程式为:____。 (2)饱和NaCl溶液的作用是______,能否省去盛有浓硫酸的洗气瓶_____,理由是______ (3)能否省去冰水冷却________,用化学方程式表示原因是:_______,大试管内发生反应的离子方程式为________。 |
|
| 22. 填空题 | 详细信息 | |||||||||||||||
对于反应:2SO2+O2
|
||||||||||||||||
| 23. 填空题 | 详细信息 |
|
A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。 A. 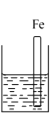 B. B. 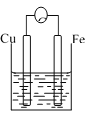 C. C. 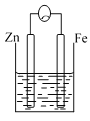 (1)A中反应的离子方程式为_____,B中Cu极电极反应式为______。 (2)C中被腐蚀的金属是____________,总反应方程式为____________, (3)A、B、C中铁被腐蚀的速率,由大到小的顺序是__________。 |
|
| 24. 填空题 | 详细信息 |
|
(227℃,1个大气压时),1.5L某烃蒸汽能在aL氧气中完全燃烧,体积增大到(a+3)L(相同条件下),问: (1)该烃在组成上必须满足的基本条件是____________________ (2)当a=10L时,该烃可能的分子式__________________ (3)当该烃的分子式为C7H8时,a的取值范围为____________________ |
|
最近更新



